
VII Всероссийский симпозиум с международным участием «Актуальные вопросы тканевой и клеточной трансплантологии»
Тезисы докладов участников от ФГБУ Всероссийский центр глазной и
пластической хирургии МЗ РФ
27-28 апреля 2017 года, Астрахань

Масса мышечной ткани у взрослого человека достигает 40-45% от общего веса человека. При этом, роль мышечной системы заключается не только в двигательной сократительной деятельности, но и в осуществлении метаболических процессов в организме. Поэтому, глубокие повреждения мышечной ткани могут способствовать не только к снижению качества жизни и инвалидизации, но и привести к тяжелым летальным последствиям, связанных с обменными процессами.

Многопрофильный тканевой банк Всероссийского центра глазной и пластической хирургии изготавливает широкий спектр биоматериалов Аллоплант для стимуляции репаративной регенерации самых различных тканей и анатомических образований и в том числе структур опорного аппарата. Для экспериментального обоснования трансплантационных материалов, стимулирующих репарацию элементов мягкого остова, на базе Центра были проведены многочисленные морфологические исследования.
В ФГБУ ВЦГПХ Минздрава России разработан и внедрен в клинику ряд операций с применением губчатых аллотрансплантатов с дренирующими свойствами. Они успешно используются как при глаукоме, часто возникающей в результате нарушения тока внутриглазной жидкости, так и при невритах зрительного нерва, где необходимо усиление кровообращения в заднем отрезке глазного яблока.
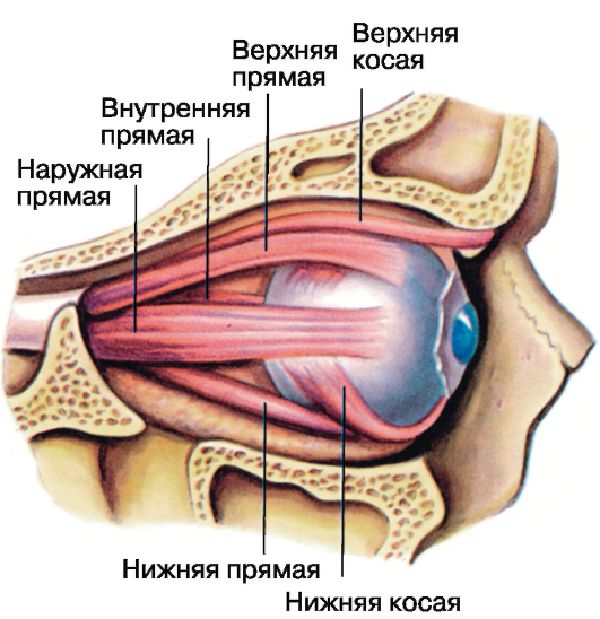
В лаборатории консервации тканей Всероссийского центра глазной и пластической хирургии также создана разновидность эластинового биоматериала. Учитывая его оптимальные биомеханические параметры, нами поставлена следующая цель настоящей работы: изучить возможность использования разработанного эластинового биоматериала в кранио-фациальной хирургии и в частности при восстановлении костных стенок глазницы.
Настоящая работа ставит своей целью изучить возможности использования методов регистрации тканевого напряжения в комплексной диагностике хронического генерализованного пародонтита,
а также оценить его динамику при лечении данной патологии с использованием инъекционных форм биоматериалов Аллоплант.
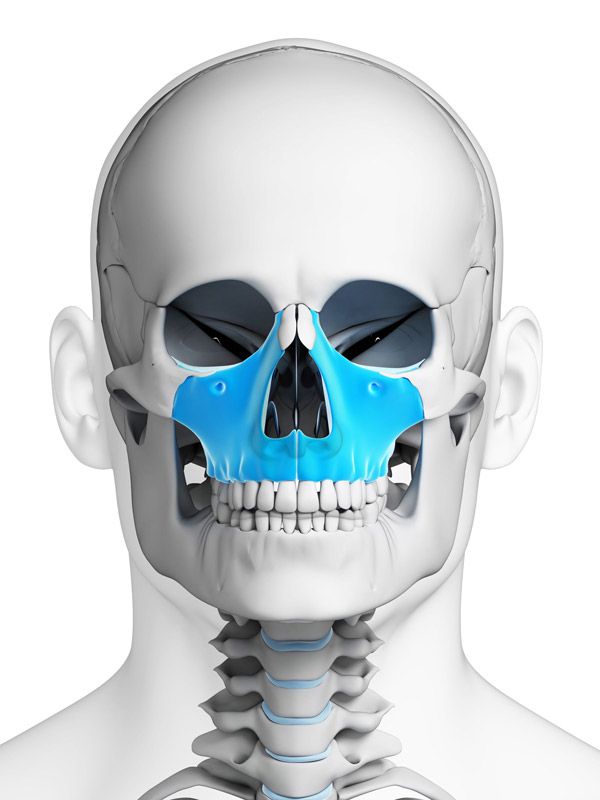
Полученные краниометрические данные по топографии клыковой ямки и толщине передней стенки верхнечелюстной пазухи легли в основу разработки хирургической техники и доступа к передней стенке верхней челюсти, а также моделирования трансплантатов для костнопластических операций, в том числе и микромаксиллотомии.

Учитывая многолетний опыт работы с аллогенными трансплантатами при хирургическом лечении патологии глаза и его придатков, нами был предложен новый подход в хирургическом лечении рубцовых поражений век. Обоснованием инновационных технологий явились многочисленные экспериментально-морфологические и клинические исследования.
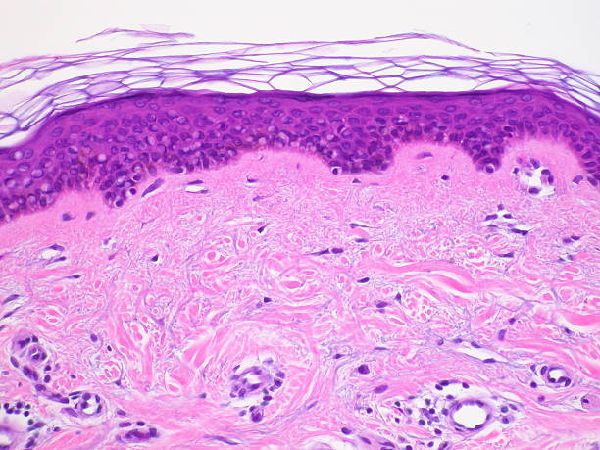
В работе изучено влияние аллогенного биоматериала Аллоплант на репаративные процессы в коже крыс после химического ожога.

Работа посвящена выявлению морфологических изменений в роговице глаза кроликов после химического ожога и перилимбального введения биоматериала Аллоплант.

Исследование показателей упруго-прочностных свойств лиофилизированных соединительнотканных аллотрансплантатов имеет принципиальное значение для применения их в клинической практике, так как после пересадки аллотрансплантаты испытывают определенную механическую нагрузку.

Проведено морфологическое исследование соединительнотканных трансплантатов с различной структурой и гистохимическим составом, подвергнутых воздействию лазерного излучения. Показано, что степень деструкции в зоне лазерного реза зависит от фиброархитектоники трансплантата.
Лебедева Анна Ивановна - кандидат биологических наук, старший научный сотрудник отдела морфологии ФГБУ «Всероссийский центр глазной и пластической хирургии» МЗ РФ, 450075, г. Уфа, ул. Р.Зорге, 67/1. Тел.: (3472) 93-42-35, факс: (3472) 48-99-38, E-mail: Jeol02@mail.ru
Муслимов Сагит Асхатович – доктор медицинских наук, ведущий научный сотрудник, зав. отделом морфологии ФГБУ ВЦГПХ МЗ РФ, 450075, г. Уфа, ул. Р.Зорге, 67/1. Тел.: (3472) 93-42-35, факс: (3472) 48-99-38, E-mail: morphoplant@mail.ru
Мусина Ляля Ахияровна – доктор биологических наук, ведущий научный сотрудник отдела морфологии ФГБУ ВЦГПХ МЗ РФ, 450075, г. Уфа, ул. Р.Зорге, 67/1. Тел.: (3472) 93-42-35, факс: (3472) 48-99-38, E-mail: morphoplant@mail.ru
Раскрытие регенераторного потенциала скелетной, сердечной и гладкой мышечных тканей в модельных экспериментах на животных с применением биоматериалов Аллоплант (БМА).
Регенерация скелетной мышечной ткани: в первой опытной группе (n=36) в области средней трети брюшка мышцы голени наносили субтотальный дефект длиной 3–4 мм. После чего в толщу между проксимальной и дистальной культями укладывали БМА соответствующих размеров и фиксировали нитевидным аллосухожильным трансплантатом. В контрольной серии (n=36) в области икроножной мышцы был нанесен аналогичный дефект и ушивание резецированных культей шовным материалом Vicryl 6–0. В обоих случаях на кожу накладывали швы Vicryl 6–0. Малоберцовый нерв не повреждали. БМА был губчатой модификации.
Регенерация сердечной мышечной ткани: экспериментальные исследования были проведены на кроликах. Инфаркт миокарда был вызван путем лигирования нисходящей коронарной артерии. В контрольной группе (n=18) через 5 суток после коронароокклюзии вводили физиологический раствор, а в опытной (n=30) интрамиокардиально вводили БМА диспергированной модификации.
Регенерация гладкой мышечной ткани: в контрольной серии экспериментов у кроликов (n=10) делали дефект маточного рога фокусированным лучом СО2-лазера и ушивали Vicryl 6–0. В опытной группе (n=15) зону дефекта заполняли БМА объемно-волокнистой модификации.
Животных выводили из опытов через 2, 7, 14, 30, 60, 120 и 180 суток после операции. Использовали общегистологические, гистохимические, иммуногистохимические и электронномикроскопические методы исследования.
Исследования показали, что аллогенные биоматериалы обладали биосовместимостью и не вызывали выраженной иммунной реакции со стороны иммунной системы. Продукты их биодеградации в мышечных тканях служили индукторами стволовых и коммитированных клеток, что позволяло применять аллогенные биоматериалы для реализации резервного клеточного потенциала мышечных тканей для их регенерации.
В скелетной мышечной ткани в процессе замещения биоматериала на месте дефекта формировался регенерат, представленный в ранние сроки рыхлой васкуляризированной соединительной тканью, затем он трансформировался в соединительнотканно-мышечный регенерат. В итоге замещения БМА формировалась органотипичная мышечная ткань с основными составляющими элементами – поперечноисчерченными мышечными волокнами, эндомизием, перимизием и восстановленным кровообращением и иннервацией. Применение губчатой модификации БМА способствовало индукции и дифференциации миогенных клеток (количество миобластов MyoD+ в опытной группе в реактивной зоне замещения на 7 и 14 сутки составляло 5,3±2,2 и 7,6±5,3; в контрольной группе – 4,6±4,7 и 0,6±0,7 клеток в поле зрения соответственно). Замещение БМА происходило гетерохронно, по юкстаоппозиционному типу.
Интрамиокардиальное введение диспергированной формы БМА способствовало улучшению структуры ишемически поврежденного миокарда у экспериментальных животных за счет интенсификации кровообращения, миграции и пролиферации стволовых с-kit (количество прогениторных c-kit+ клеток превышало значения контрольной группы в начальные сроки в 6,25 раз) и коммитированных GATA-4 клеток, а также стимуляции внутриклеточной регенерации на фоне ингибирования фиброза. Регенерат в опытной группе отличался интенсивной васкуляризацией - показатели суммарной площади просвета капилляров с 7 суток резко возрастали (401,7 ± 274,7 мкм2 в поле зрения– в опытной и 267,8 ± 132,8 мкм2 - в контрольной группе).
Объемно-волокнистая форма БМА после пересадки в дефект стенки рога матки экспериментальных животных в процессе биодеградации вызывала пролиферацию, дифференциацию и миграцию лейомиоцитов из тканевого ложа в реактивную зону. Заживление заканчивалось полноценной реституцией поврежденной ткани за счет ингибирования процесса синтеза коллагена и адекватной васкуляризации.
Биоматериалы Аллоплант при репаративной регенерации мышечных тканей стимулировали миграцию и дифференциацию макрофагов М1 системы активации, что приводило к полноценному фагоцитозу и снижению антигенности в ране. При замещении БМА макрофаги М1 системы активации становились доминирующими клетками гистиона. Репаративные возможности скелетной, сердечной и гладкой мышечных тканей осуществлялись на фоне ингибирования факторов фиброза. Продукты биодеградации аллогенного биоматериала ингибировали экспрессию профиброгенных клеточных факторов (TGF-β1, FGF-1), и за счет этого регулируя функциональную активность фибробластических клеток, тормозя процессы миграции их предшественников (vimentin+ клеток), являлись индукторами стволовых и коммитированных клеток в мышечных тканях. В контрольных группах животных заживление посттравматических или ишемических повреждений мышечных тканей без использования аллогенного биоматериала сопровождалось повышенной экспрессией профиброгенных факторов - TGF-β1, FGF-1 при высокой концентрации vimentin+ клеток и заканчивалось формированием грубого рубца.
Аллогенные биоматериалы при имплантации экспериментальным животным восполняли объемный дефект поврежденных мышц, стимулировали скрытые восстановительные резервы с индукцией стволовых и коммитированных клеток, создавали адекватные условия для их дифференциации, и таким образом позволяли восстановить структурную полноценность по заместительному типу за счет эффективного предупреждения рубцово-фиброзных изменений мышечных тканей.
Мулдашев Эрнст Рифгатович ФГБУ «Всероссийский центр глазной и пластической хирургии» Министерства здравоохранения Российской Федерации, Россия, Уфа. Генеральный директор, доктор медицинских наук, профессор. E-mail: centre@alloplant.ru 450075, г. Уфа, ул. Рихарда Зорге, д. 67/1; тел. 8(347)224-68-01
Нигматуллин Рафик Талгатович ФГБУ «Всероссийский центр глазной и пластической хирургии» Министерства здравоохранения Российской Федерации, Россия, Уфа. Заместитель генерального директора, доктор медицинских наук, профессор. E-mail: nigmatullinr@mail.ru 450075, г. Уфа, ул. Рихарда Зорге, д. 67/1; тел. 8(347)224-68-03
Галияхметов Радик Фаязович ФГБУ «Всероссийский центр глазной и пластической хирургии» Министерства здравоохранения Российской Федерации, Россия, Уфа. Заведующий отделением восстановительной медицины, кандидат медицинских наук. E-mail: grf-61@mail.ru 450075, г. Уфа, ул. Рихарда Зорге, д. 67/1; тел. 8(347)293-42-95
Сформулированная отечественными анатомами концепция мягкого остова нашла практическое преломление в клинической травматологии и ряде других областей медицины [4]. Являясь гибким продолжением костного скелета, структуры мягкого остова включают в себя связочный аппарат, сухожилия, фиброзные оболочки капсул суставов и синовиальных влагалищ, фасции и фасциальные узлы, соединительнотканный футляр скелетных мышц. Растяжения и разрывы представленных формаций составляют значительный удельный вес в общей структуре спортивного травматизма.
В первой серии экспериментов на лабораторных крысах породы «Вистар» наносилась резаная рана на половину ширины пяточного сухожилия. Затем перифокально вводился ДБА «Стимулятор регенерации» [1]. На фоне трансплантации ДБА происходит относительно ранняя пролиферация и дифференцировка фибробластов, а также активный синтез новообразованных коллагеновых волокон, которые проходят этап ремоделирования и в финале формируют однонаправленные структуры. В тканевом ложе трансплантата активируется ангиогенез.
Пересадка структурированного биоматериала в форме нити характеризуется относительно меньшей реакцией тканевого ложа, включая состояние органного сосудистого русла, преимущественно продольной ориентацией пучков коллагеновых волокон формирующегося регенерата (85+5,1%), что указывает на его высокие прочностные характеристики.
Для изучения системного действия биоматериалов в биоактивные точки лабораторных кроликов породы «Шиншилла» вводился биоматериал для акупунктурной терапии. В биоактивной точке при инъекции биоматериала развивается комплекс локальных сосудистых и клеточных реакций, которые поддерживаются до 30 суток. Именно в эти сроки нами были выявлены эффекты стимуляции репаративной регенерации в различных соединительнотканных структурах [2]. Эффективность разработанного метода фармакопунктуры подтверждена патентом РФ (№ 2238076 от 12.05.2003 г. «Способ лечения и профилактики заболеваний воздействием на биологически активные точки и зоны» Мулдашев Э.Р. с соавт.).
Представленные экспериментальные данные по типу замещения трансплантатов были использованы нами в клинической практике для разработки хирургической тактики при повреждениях сухожилий и связок, определения показаний для трансплантационных операций, а также обоснования курса реабилитации с использованием биоматериалов.
В настоящее время представляемые виды биоматериалов широко внедрены в клиническую практику травматологии и ортопедии. В последние годы в связи с обращением пациентов по поводу спортивных травм, в Центре отрабатывается алгоритм медицинского сопровождения спортсменов, выступающих в различных видах спорта. При отработке индивидуального лечебно-реабилитационного курса учитываются такие факторы как происхождение травмы (первичные, связанные с перегрузками, повторные) время возникновения (острые, хронические), степени тяжести, возраст пациента, особенности конституционального типа спортсмена [5,6,7,8]. Однако базовые принципы хирургического пособия при травмах опорного аппарата остаются неизменными. Так при микротравмах структур мягкого остова проводится локальное введение ДБА в сухожилия или связки с учетом зон повышенной травматизации.
При полном разрыве сухожилий или связок требуется пластика с использованием аллосухожильных нитей или лент. Исключительно важен тот факт, что при проведении АСН через мышечное брюшко на трансплантате формируется дополнительная опора для мышечных волокон, что обеспечивает более раннюю функциональную нагрузку.
Системный уровень воздействия на организм предполагает инъекцию специфических форм диспергированным биоматериалом в акупунктурные точки. Эти методы позволяют через интегративные системы организма (нервную, эндокринную, иммунную) стимулировать эффекты местной трансплантации биоматериалов. При этом методики местного и системного воздействия на организм взаимно дополняют друг друга.
1. Аслямов, Н.Н. Применение аллогенного сухожильного трансплантата для стимуляции регенерации сухожилий: Автореф. дис. … канд. мед. наук. – Уфа, 2005. - 21 с.
2. Галияхметов, Р.Ф. Динамика постожоговой регенерации роговицы при локальном и рефлексогенном воздействии аллогенным диспергированным биоматериалом: Автореф. дис. … канд. мед. наук. – Екатеринбург, 2010. – 22 с.
3. Регенеративная медицина. Биоматериалы Аллоплант в офтальмохирургии / Под общей ред. проф.Мулдашева Э.Р. – Уфа: ГУП «Башкортостан», 2014. – 432с.
4. Сорокин А.П. Общие закономерности строения опорного аппарата человека / А.П. Сорокин. – М.: «Издательство «Медицина», 1973. – 264с.
5. Стефен М.Перл. Обзор ведения спортивных травм. В кн. Консервативное лечение травм у спортсменов: Под ред. Томаса Е.Хайда, Мэриан С.Генгенбах. – М.: ООО «Издательство «Медицина», 2005. – С.3-9.
6. Томас А.Соуза. Коленный сустав. В кн. Консервативное лечение травм у спортсменов: Под ред. Томаса Е.Хайда, Мэриан С.Генгенбах. – М.: ООО «Издательство «Медицина», 2005. – С.376-432.
7. Томас Р.Дейли, Данте М.Филетти. Судебно-медицинские установки в спортивной медицине (со специальным обсуждением для хиропрактика). В кн. Консервативное лечение травм у спортсменов: Под ред. Томаса Е.Хайда, Мэриан С.Генгенбах. – М.: ООО «Издательство «Медицина», 2005. – С.10-14.
8. Уильям Дж.Мореа, Лэрри Дж.Кинтнер, Эдвард Жд.Риан. Консервативная реабилитация при спортивных травмах. В кн. Консервативное лечение травм у спортсменов: Под ред. Томаса Е.Хайда, Мэриан С.Генгенбах. – М.: ООО «Издательство «Медицина», 2005. – С.44-61.
Мусина Ляля Ахияровна – док.биол.наук, вед. науч. сотр. отдела морфологии ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава РФ, 450075, г.Уфа, ул.Р.Зорге, 67/1, тел.: (347) 2- 93-42-35. E-mail: morphoplant@mail.ru
Муслимов Сагит Асхатович - док.мед.наук, вед. науч. сотр., зав. отдела морфологии ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава РФ, 450075, г.Уфа, ул.Р.Зорге, 67/1.Тел.: (347) 2- 93-42-22. E-mail: morphoplant@mail.ru
Корнилаева Гузэль Галеевна – док.мед.наук, врач-офтальмохирург, зав.учебными курсами ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава РФ, 450075, г.Уфа, ул.Р.Зорге, 67/1.Тел.: (347) 2- 93-42-22. E-mail: morphoplant@mail.ru
Соловьева Екатерина Павловна - канд.мед.наук, врач-патологоанатом отдела морфологии ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава РФ, 450075, г.Уфа, ул.Р.Зорге, 67/1, тел. (347) 2- 93-42-35. e-mail: dikatang@gmail.com
Карушин Олег Иванович - канд.мед.наук, зав.отделения офтальмохирургии ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава РФ, 450075, г.Уфа, ул.Р.Зорге, 67/1. Тел.: (347) 2- 32-89-69. E-mail: morphoplant@mail.ru
Корнилаева Маргарита Павловна – канд.мед.наук, зав.отделения офтальмохирургии ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава РФ, 450075, г.Уфа, ул.Р.Зорге, 67/1, Тел.: (347) 2- 32-90-64. г.Уфа. morphoplant@mail.ru
Кульбаев Нафис Давлетбаевич – канд.мед.наук, врач-офтальмохирург, главный врач ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава РФ, 450075, г.Уфа, ул.Р.Зорге, 67/1, тел.: (347) 2- 93-42-35. E-mail: morphoplant@mail.ru
Гафаров Ильяс Зульфирович - врач-офтальмохирург ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава РФ, 450075, г.Уфа, ул.Р.Зорге, 67/1, тел.: (347) 2- 93-42-35. E-mail: morphoplant@mail.ru
В ФГБУ ВЦГПХ Минздрава России разработан и внедрен в клинику ряд операций с применением губчатых аллотрансплантатов с дренирующими свойствами. Они успешно используются как при глаукоме, часто возникающей в результате нарушения тока внутриглазной жидкости, так и при невритах зрительного нерва, где необходимо усиление кровообращения в заднем отрезке глазного яблока (Шангина с соавт., 2011; Мулдашев Э.Р. с соавт., 2014).
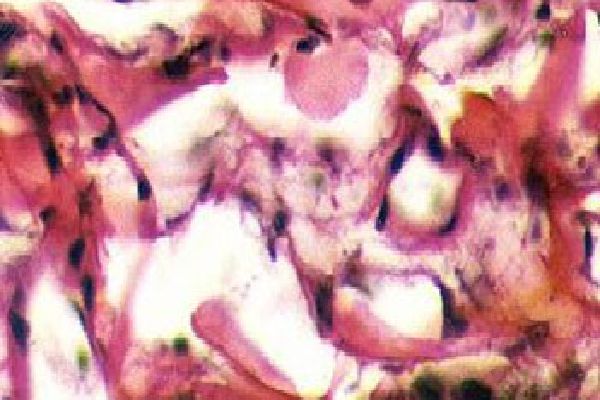
Несмотря на выраженные патоморфологические изменения (вследствие тяжелых диагнозов) всех внутренних оболочек энуклеированных глазных яблок через 1 год и 5 лет после операции дренирования заднего отдела глаза непосредственно сам имплантированный губчатый биоматериал ярко выраженных структурных изменений не претерпевал. Он был представлен ячеистой тканью, состоящей из множества сообщающихся между собой и не смыкающихся микрополостей, каналов и щелей. Коллагеновые волокна биоматериала не подвергались биодеградации. Тинкториальные свойства, характерные для соединительной ткани, из которой изготавливается данный вид трансплантата, сохранялись. Стенки каналов характерно окрашивались пикрофуксином в ярко-красный цвет. В некоторых участках ячейки трансплантата содержали васкуляризированную рыхлую волокнистую соединительную ткань, и лишь отдельные были заполнены довольно плотной по структуре соединительной тканью. Высокая фильтрационная способность биоматериала, имеющая очень большое значение для дренажных операций, хорошо сохранялась. Стенки ячеек аллотрансплантата не смыкались, вероятно, этим способствуя пролонгированной дренажной функции как в области зрительного нерва, что особенно важно для снятия отека при неврите, так и в переднем отрезке глаза в случае глаукомы. О факте выполнения губчатым биоматериалом дренажной функции свидетельствовало то, что не спавшиеся его ячейки содержали окрашивающийся пикрофуксином в желтый цвет жидкий субстрат. Стенки каналов трансплантата во многих участках выстилали тяжи удлиненных эндотелиоподобных клеток с веретеновидными ядрами, похожими по структуре на эндотелиоциты стенки сосудов. В обеих рассматриваемых нами случаях губчатый аллотрансплантат прорастал значительным количеством мелких кровеносных сосудов, создавая за счет формирования коллатералей дополнительное питание для оболочек глаза.
Губчатый биоматериал, изготовленный по технологии Аллоплант, помещенный в супрахориоидальное пространство глаза во время операции дренирования заднего отдела глаза, длительно (до 5 лет) не рассасывается, не рубцуется, хорошо сохраняет в тканях реципиентов свою структуру, способствуя выполнению дренажной функции, а также прорастает кровеносными сосудами, создавая дополнительное питание для оболочек глаза.
1. Шангина О.Р., Мусина Л.А., Хасанов Р.А., Булгакова Л.А., Корнилаева Г.Г., Корнилаева М.П. Экспериментально-гистологическое обоснование эффективности пористого аллотрансплантата для целей офтальмохирургии. Вестник Оренбургского государственного университета. - Оренбург. – 2011. - №14 (133). - C.400-403.
2. Мулдашев Э.Р., Корнилаева Г.Г., Муслимов С.А. и др. Морфологические изменения сетчатки и зрительного нерва при дренировании заднего отдела глазного яблока кролика // Вестник Оренбургского государственного университета. – №12 (173). - 2014.- С.223-225.
Нигматуллин Рафик Талгатович ФГБУ «Всероссийский центр глазной и пластической хирургии» Министерства здравоохранения Российской Федерации, Россия, Уфа. Заместитель генерального директора, доктор медицинских наук, профессор.
E-mail: nigmatullinr@mail.ru 450075, г. Уфа, ул. Рихарда Зорге, д. 67/1; тел. 8(347)224-68-03
Кутушев Ринат Закиевич ФГБУ «Всероссийский центр глазной и пластической хирургии» Министерства здравоохранения Российской Федерации, Россия, Уфа. 450075, г.Уфа, ул.Р.Зорге, 67/1. Заведующий офтальмологическим отделением №3 ФГБУ «ВЦГПХ» Минздрава России, e- E-mail: rinat-dok@yandex.ru; тел. (347) 224-68-19
В практике кранио-фациальной хирургии широко используются трансплантационные материалы для восстановления костей лицевого черепа. При этом применяются как биологические материалы, так и эксплантаты [2].
В опытной серии наблюдается иная морфологическая картина. Так, на 30 сутки в области экспериментальной травмы обнаруживается диастаза в 1,5 – 2,0 мм между двумя костными поверхностями. Указанный дефект восполнен эластиновым биоматериалом. На всем протяжении периферической зоны трансплантата происходит его активное замещение волокнистой соединительной тканью. Динамика процессов заместительной регенерации вариабельна и зависит от характера тканевого ложа. Так, со стороны полости черепа трансплантат покрыт твердой мозговой оболочкой, но замещение биоматериалом идет относительно медленно. В зоне контакта биоматериала с надкостницей глазницы и костной тканью процессы заместительной регенерации более выражены. В области прилежащей жировой клетчатки глазницы происходит активное замещение эластинового биоматериала плотной волокнистой соединительной тканью на глубину до 800мкм. В описываемый срок также наблюдаются явные признаки остеогенеза. При этом выделяются два типа репарации костных структур: краевой остеогенез (по фронтальному типу) в зоне контакта костной ткани с биоматериалом и очаговый остеогенез. Признаки очагового остеогенеза обнаруживаются в сформированной на месте трансплантата волокнистой соединительной ткани в виде отдельных локусов до 50мкм в диаметре с выраженной оптической анизотропией, характерной для костной ткани. Данный тип репаративного остеогенеза по своим морфологическим признакам в целом соответствует первичному развитию костей в онтогенезе.
1. Микроскопическая техника. Руководство для врачей и лаборантов. / Под редакцией Д.С. Саркисова и Ю.Л. Петрова. – М.: Медицина, 1996. – 544с.
2. Мулдашева И.Э. Хирургическое лечение посттравматических гипофтальма и энофтальма с применением биоматериалов Аллоплант: Автореф. дис. … канд.мед.наук. – Челябинск, 2007. – 18с.
3. Омельяненко Н.П., Слуцкий Л.И. Соединительная ткань (гистофизиология и биохимия). В 2 т. Т.II / Под ред. Академика РАН С.П. Миронова. – М.: Издательство «Известия», 2010. – 600с.
4. Регенеративная медицина. Биоматериалы Аллоплант в офтальмохирургии / Под общей ред. Мулдашева Э.Р. – Уфа: ГУП «Башкортостан», 2014. – 432с.
Нигматуллин Рафик Талгатович Федеральное государственное бюджетное учреждение «Всероссийский центр глазной и пластической хирургии» Министерства здравоохранения Российской Федерации, Россия, Уфа. Заместитель генерального директора, доктор медицинских наук, профессор. E-mail: nigmatullinr@mail.ru; 450075, г. Уфа, ул. Рихарда Зорге, д. 67/1; тел. 8(347)224-68-03
Гизатуллина Эльвира Рафиковна Федеральное государственное бюджетное учреждение «Всероссийский центр глазной и пластической хирургии» Министерства здравоохранения Российской Федерации, Россия, Уфа. Заведующий отделением стоматологии, кандидат медицинских наук. E-mail: elviragizatullina@yandex.ru; 450075, г. Уфа, ул. Рихарда Зорге, д. 67/1; тел. 89173446103
Кабиров Тамерлан Зуфарович ФГБОУ ВО «Башкирский государственный медицинский университет» Министерства здравоохранения Российской Федерации, Россия, Уфа. Студент 2 курса E-mail: kabirova_milya@list.ru; 450000, г. Уфа, ул. Ленина, д.3; тел. 89173405876
Гистотопографические исследования условно здоровой слизистой оболочки десны проведены на материале 21 трупа обоих полов I периода зрелого возраста. Для морфологических исследований слизистой оболочки десны при ХГП различной степени тяжести и на фоне введения диспергированного биоматериала Аллоплант (ДБМА) нами был произведен забор биоптатов тканей десны с учетом информированного согласия пациентов. Забор биопсийного материала проводился до лечения и в разные сроки после лечения (через 7, 30, 90 суток). Нами исследовано 42 биоптата тканей слизистой оболочки десны, взятых у лиц мужского и женского пола в возрасте от 23 до 60 лет.
Для коррекции патологических изменений слизистой оболочки полости рта на фоне хронического воспаления нами в схему комплексного лечения ХГП была включена методика введения ДБМА: однократная инъекция в область переходной складки слизистой оболочки десны верхней и нижней челюсти (от 4 до 6 вколов в область одной челюсти).
Для исследования биомеханических параметров слизистой оболочки десны в норме и при различных патологических состояниях нами был разработан аппарат контактной тензометрии, на базе Уфимского авиационного технического университета. Созданный прибор позволяет контрольно регистрировать суммарное тканевое напряжение с точностью до 0,05 мм рт.ст.
Проведенные исследования выявили структурные изменения волокнистого остова десны на фоне генерализованного пародонтита с адекватным снижением ТН. Для ХГП легкой степени характерно значительное падение тканевого напряжения до 208,08±19,2 Па. и появление первых признаков деструкции волокнистого остова десны. При пародонтите средней степени тяжести ТН снижается до 149,43±20,25 Па. Одновременно происходят более выраженные изменения в структуре волокнистого остова. Для хронического генерализованного пародонтита тяжелой степени характерно максимальное снижение ТН до 102,77±12,32 Па с глубокой дезорганизацией всего волокнистого остова десны.
После комплексного лечения ХГП с включением в терапевтическую схему местное введение ДБМА выявлено, что ТН на 7 сутки резко возрастает до 498,41±18,78 Па , что превышает данный показатель в норме. По-видимому, на данном этапе коррекции ТН поддерживается за счет присутствующих в трансплантате протеогликанов, которые как известно обладают полианионными свойствами и удерживают значительное количество воды.
В последующем на 30 и 90 сутки определяется четкая тенденция нормализации ТН. Так, на 90 сутки данный показатель достигает 396,83±26,27Па. Выявленная в отдаленные сроки наблюдения оптимальная динамика ТН связана с регенерацией и ремоделирование анатомических структур мягкого остова десны. В частности независимо от стадии процесса нами наблюдалось восстановление базальной мембраны, активная индукция ангиогенеза, снижение и полное исчезновение инфильтрации слизистой оболочки.
Однократное местное введение диспергированной формы биоматериала, приводит к повышению ТН до 498,41±5,94 Па, что позволяет рассматривать аллотрансплантацию как способ коррекции тканевого напряжения в соединительной ткани десны и активации путей микроциркуляции.
1. Гизатуллина Э.Р. Структурные и биомеханические особенности слизистой оболочки десны: Автореф. дис. … канд. мед. наук. – Уфа, 2006. – 22 с.
2. Лебединский В.Ю. Напряженно-деформированные состояния структур органов (экспериментально-клиническое исследование).- Иркутск, 2000. 42с.
3. Тензометрические параметры как биофизический эквивалент структур мягкого остова лица / Э.Р. Нигматуллин, Н.Д. Кульбаев, Е.В. Дятчина // Вестник ОГУ№4 (153). – 2013. – С.193-196.
4. Применение тензометрических методов исследования в стоматологии: метод. Рекоменд. / Р.Т. Нигматуллин, В.Г Гафаров, Э.Р. Гизатуллина [и др.]. - Уфа, 2006. – 42 с.
5. Роль тканевого напряжения при пересадке аллогенных трансплантатов / Р.Т. Нигматуллин с соавт. /Вестник ОГУ №78/декабрь. - 2007. – С.147-150.
Нигматуллин Рафик Талгатович. Федеральное государственное бюджетное учреждение «Всероссийский центр глазной и пластической хирургии» Министерства здравоохранения Российской Федерации, Россия, Уфа. Заместитель генерального директора, доктор медицинских наук, профессор. E-mail: nigmatullinr@mail.ru; 450075, г. Уфа, ул. Рихарда Зорге, д. 67/1; тел. 8(347)224-68-03
Щербаков Дмитрий Александрович. Ассистент кафедры ЛОР- болезней ФГБОУ-ВО « ТГМУ»Минздрава России. Адрес: 128043,Россия, г.Тюмень, ул.Одесская, 54. E-mail: dmst@bk.ru
Каримова Алина Ирековна – соискатель кафедры анатомии человека ФГБОУ «БГМУ» Минздрава России г.Уфы 450075, Россия, г.Уфа, ул.Ленина, 3. E- mail: alina.karimova@myrambler.ru
Гареев Евгений Мусинович. ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава России. Старший научный сотрудник, кандидат биологических наук. 450075, Россия, г.Уфа, ул.Р.Зорге 67/1. E-mail: gem46@list.ru
Изучение проекции клыковой ямки на теле верхней челюсти и толщины передней стенки верхнечелюстной пазухи с учетом возрастных и гендерных различий для выбора оптимального хирургического доступа при выполнении микромаксилотомии и подборе адекватного биоматериала для закрытия костного дефекта.
Антропометрические исследования включали анализ компьютерных томограмм 634 лиц обоего пола в возрасте от 5 до 60 лет. Для распределения всех исследуемых лиц по возрастным группам использовалась классификация, принятая на VII Всесоюзной конференции по проблемам возрастной морфологии, физиологии и биохимии АПН СССР ( Москва, 1965г.). Возрастные группы составили лица первого детства от 5-7 лет (30 человек), второго детства от 8-12 лет (62 человека), подростковой группы 13-16 лет (61 человек), юношеской группы 17-21 год (80 человек), первого периода зрелого возраста 22-35 лет ( 201 человек) и второго периода зрелого возраста 36-60 лет (200 человек) . Доля мужчин и женщин в целом была практически равной (51.4% и 48.6% соответственно сбалансирована в возрастных группах). Компьютерная томография выполнена на конусно-лучевом компьютерном томографе Planmeca Promax с шагом 0,2мм. Линейные измерения параметров клыковой ямки (КЯ) и толщины передней стенки ВЧП проводились по методике исследования скелета головы [4]. Локализация дна клыковой ямки на передней стенке ВЧП рассматривалось как ее положение по отношению к зубам верхней челюсти.
В возрастной группе первого детства локализация дна клыковой ямки на передней стенке ВЧП в области клыков верхней челюсти выявлялась у 5% пациентов. Наиболее значительные возрастные изменения обнаруживаются во втором периоде детства, где отмечается латеральное смещение дна КЯ к первому премоляру верхней челюсти. Подобная динамика выявлялась в 10% исследуемых пациентов. Подростковая возрастная группа характеризуется латерализацией топографии дна КЯ на уровень второго премоляра верхней челюсти и встречается в 10% исследуемых лиц. В период второго детства до подросткового возраста изменения толщины, глубины и расположения клыковой ямки связано с появлением первых премоляров в сменном прикусе исследуемых лиц и перестройкой стенок верхнечелюстной пазухи. Так, при переходе от периода первого детства к возрастной группе второго детства снижение среднего уровня толщины передней стенки верхнечелюстной пазухи составило 19% (с 6.1±1.0 мм до 4.9±0.8 мм). При сравнении возрастных групп второго детства и подросткового возраста снижение составило уже 31% (с 4.9± 0.8 мм до 3.4±0.5 мм). В группе юношеского возраста (17-21 года), отмечается смещение проекции дна КЯ к первому моляру верхней челюсти, что сохраняется на весь период зрелого возраста (22-35 лет, 36-60 лет) и составляют 32% от всех исследуемых лиц. При рассмотрении толщины передней стенки верхнечелюстной пазухи от подросткового до юношеского возраста отмечается снижение линейного показателя всего лишь на 9% (с 3.4±0.5 мм до 3.1±0.6 мм), а от юношеского до первого периода зрелого возраста составило 32% (с 3.1±0.6 мм до 2.0±0.4 мм). При этом разница между показателями первого и второго зрелого возраста составила 6% (снижение с 2.0±0.4 мм до 1.9±0.5 мм). Полученные результаты показали, что влияние фактора половой принадлежности оказалось практически нулевым и статистически совершенно незначимым (V=0.06, р>0.55). Зависимость в смещении проекции КЯ от клыка к первым жевательным зубам верхней челюсти и уменьшении толщины передней стенки ВЧП по мере увеличения возраста обследуемых лиц оказалась статистически значимой (V=0.5,p<<0.0001). При разработке техники микромаксиллотомии нами учитывалась описанная возрастная динамика изменчивости толщины передней стенки верхней челюсти и топография КЯ. Выбор аллотрансплантата для замещения костного дефекта и проекция наружного хирургического доступа определялись вариабельностью антропометрических параметров верхней челюсти и выполнялись в соответствии с топографией КЯ в области наименьшей толщины передней стенки ВЧП.
Выявленная динамика смещения дна клыковой ямки на передней стенке ВЧП и уменьшение толщины передней стенки верхнечелюстной пазухи с возрастом исследуемого позволили обосновать хирургический доступ к передней стенке ВЧ и определить выбор аллотрансплантата с учетом возрастного ценза пациента.
1. Аржанцев, П.З. Восстановительная хирургия мягких тканей челюстно-лицевой области / Руководство для врачей/ П.З. Аржанцев, В.А. Виссарионов, Б.Н.Давыдов, и др.- Москва: Изд-во «Медицина»,1997.-288 с.
2. Возможности цифровой объемной томографии в оториноларингологии, челюстно-лицевой хирургии и хирургической стоматологии/ А.А. Зубарева, М.А.Чибисова, А.Л. Дударев, М.А Шавгулидзе//Медицинский алфавит.- 2012.- №7.-С.18- 24.
3. Козлов, В.А. Способ закрытия передней стенки гайморовой пазухи деминерализованным костным трансплантатом// Вестник хирургии.-1983.- Т.130.-№ 3.-с.142.
4. Алексеев, В.П. Краниометрия. Методика антропометрических исследований/В.П. Алексеев, Г.Ф. Дебец.-Москва: Изд-во «Наука»,1964.-128 с.
Нураева Айгуль Булатовна. Федеральное государственное бюджетное учреждение «Всероссийский центр глазной и пластической хирургии» Министерства здравоохранения Российской Федерации, Россия, Уфа. Заведующий офтальмологическим отделением №1, кандидат медицинских наук. 450075, г.Уфа, ул.Р.Зорге, 67/1. Тел.: (3472) 48-98-02, e-mail: a.nuraeva@mail.ru
Разработка критериев подбора аллотрансплантатов для реконструктивной хирургии век.
В результате проведения экспериментальных и клинических исследований нами разработаны критерии подбора аллотрансплантатов для замещения различных тканей. Критерии были сформулированы с учетом биомеханических свойств тканей, фиброархитектоники, гистохимического состава и моделируемости. Под моделируемостью тканей подразумевается способность к упругим и пластическим деформациям. Именно эти свойства тканей позволяют свободно манипулировать ими в ходе операции и при заготовке трансплантатов. Биомеханические свойства включают показатели предела прочности, модуля упругости и относительной деформации при различных видах испытания – растяжении, сжатии и шовной фиксации. Фиброструктура трансплантатов определяет как их моделируемость, так и биомеханические свойства и зависит от пучков I, II, III порядка, их волокнистого состава и пространственной ориентации. Одним из критериев оценки тканей при подборе для трансплантации явился гистохимический состав. Мы изучили суммарное количественное содержание гликозаминогликанов, а также отдельных фракции, оказывающих значительное влияние на процессы регенерации. Таким образом, на базе вышеперечисленных критериев для разработки реконструктивных операций нами были предложены следующие трансплантаты, изготовленные по технологии Аллоплант: трансплантат для фиксируюшей пластики, для каркасной пластики.
Выполнение реконструктивных операций у пациентов с рубцовым поражением тканей требует прочной фиксации века к внутренней и наружной спайкам, что в данном случае является гарантией успеха операции. Поэтому целесообразно использование аллотрансплантата для фиксирующей пластики Аллоплант. Изучение биомеханических свойств данного трансплантата показало, что он обладает высокими показателями прочности и упругости, характеризуется однонаправленной линейной ориентацией пучков волокон и высокой плотностью их упаковки. Такая фиброструктура способствует замещению волокнистого каркаса трансплантата не одномоментно, а постепенно, в течение 1,5-2 лет, что определяет длительную прочность фиксации тканей с помощью биоматериала для фиксирующей пластики.
Далее, для восстановления задней пластинки века мы предлагаем использовать трансплантат для каркасной пластики, который обладает следующими свойствами: возможностью придания объемно-пространственной формы, способностью к упругой деформации для сохранения заданной формы, способностью сохранять форму при замещении и высокой прочностью на прорезывание хирургических швов. Коллагеновые волокна трансплантата, имеющие различную степень структурной организации, образуют плотно упакованную трехмерную объемную сеть, дополнительно укрепленную эластическими волокнами. Замещение трансплантата происходит постепенно, два года и более. При этом длительно сохраняется волокнистая соединительная ткань трансплантата с множеством островков замещения. Выявляются также и эластические волокна биоматериала [5,6].
В рамках настоящей работы нами проведен анализ результатов 230 реконструктивных операций на веках с использованием описанных выше трансплантатов для каркасной пластики и аллосухожильных нитей. При этом прослежены отдаленные результаты хирургического лечения в сроки до 10 лет. Клинический опыт полностью подтверждает правильность сформулированных принципов подбора биоматериалов для восстановительной хирургии век.
Таким образом, подобранные с учетом биомеханических свойств, фиброархитектоники, гистохимического состава, формообразующих свойств, аллотрансплантаты, позволили разработать серию реконструктивных операций и новый подход к хирургии рубцовых деформаций мягкого остова век.
1. Муслимов С.А. Морфологические аспекты регенеративной хирургии./ Башкортостан, Уфа 2000.
2. Нигматуллин Р.Т. Очерки трансплантации тканей./ Издат ГУП РБ «Уфимский полиграфкомбинат», Уфа 2003.
3. Пластическая офтальмохирургия. В кн.: Регенеративная медицина. Биоматериалы Аллоплант в офтальмохирургии / Под общей редакцией проф. Э.Р. Мулдашева // Уфа: ГУП «Государственное республиканское издательство «Башкортостан. - 2014: С.53-118.
4. Салихов А.Ю. Первичная пластика биоматериалами «Аллоплант» в офтальмоонкологии: Автореф. дис. … д-ра. мед. наук. - Москва, 2004. – 41 с.
5. Способ хирургического лечения рубцового выворота нижнего века: Патент № 2248193 / Мулдашев Э.Р., Галимова В.У., Нураева А.Б., Салихов А.Ю. приоритет 01.09.2003г. Опубликовано: 20.03.2005г.
6. Способ хирургического лечения частичного рубцового выворота нижнего века / Мулдашев Э.Р., Галимова В.У., Нураева А.Б. // Патент на изобретение № 2564966. Бюл. №28 приоритет 30.10.2014. Зарегистрировано в Государственном реестре 10.09.2015г.
Нураева Айгуль Булатовна – канд. мед. наук, заведующий отделения офтальмохирургии ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава РФ, 450075, г.Уфа, ул.Р.Зорге, 67/1, тел.(347) 293-42-28, е-mail: a.nuraeva@mail.ru
Мусина Ляля Ахияровна – док.биол.наук, вед. науч. сотр. отдела морфологии ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава РФ, 450075, г.Уфа, ул.Р.Зорге, 67/1, тел.: (347) 2- 93-42-35. E-mail: morphoplant@mail.ru.
Лебедева Анна Ивановна – канд.биол. наук, старш. науч. сотр. отдела морфологии ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава РФ, 450075, г.Уфа, ул.Р.Зорге, 67/1, тел.: (347) 2- 93-42-35. E-mail: jeol02@mail.ru.
Вафиев Александр Сергеевич – магистрант кафедры физиологии человека и зоологии биологического факультата ФГБОУ «Башкирский государственный университет» Минобрнауки РФ E-mail: sasha_8_@mail.ru
Изучение влияния аллогенного биоматериала на репаративные процессы в коже крыс после химического ожога.
Исследования проводили на 24 беспородных белых крысах-самцах 6-месячного возраста с соблюдением основных требований, изложенных в «Правилах проведения работ с использованием экспериментальных животных». Химический ожо¬г кожи спины крыс, лишенной волосяного покрова, получали при прикладывании марлевого тампона, смо-ченного ледяной уксусной кислотой (площадь воздействия примерно 1 см2, время воздействия - 60 секунд), под эфирным наркозом. В опытной группе через 1 сутки после нанесения повреждения произвели подкожное введение в зоне поражения диспергированного аллогенного биоматериала, изготoвленного из сухожилий крыс по технологии Аллоплант, который разводили в 2-х мл физиологического раствора и вводили по 1 мл. В контрольной группе наблюдали за спонтанным заживлением раны. Фрагменты кожи в области химического ожога забирали на 4, 7, 14, 30, 60 сутки после введения биоматериала и фиксировали в 10% формалине по Лилли, заливали в парафин по общепринятым стандартным методикам. Срезы готовили на микротоме LEICA (Германия), окрашивали гематоксилином и эозином и по методу Ван-Гизон. Иммуногистохимическое выявление цитокина трансформирующий фактор роста ТGF-1 (фактора фиброза) осуществляли согласно протоколу производителя, с использованием мышиных моноклональных антител (Sаnta Cruz Biotechnology) и универсальной системы вторичной детекции для визуализации. Окрашивание производили в гистостейнере LEICA BOND MAX (LEICA, Germany). Срезы докрашивали раствором гематоксилина, заключали в бальзам. Подсчет клеток, экспрессирующих цитокин ТGF-1, осуществляли с помощью микроскопа LEICA DMD-108 (Германия). При увеличении Х400 считали окрашенные клетки в поле зрения (всего по 20 полей зрения). Для математико-статистической обработки количественных данных использовали Statistica v.7.0 (непараметрический критерий Манна-Уитни).
У крыс контрольной группы при спонтанном заживлении через 60 суток формировался грубый плотный рубец, к которому приводил высокий уровень экспрессии в тканях цитокина трансформирующий фактор роста ТGF-1 во все сроки эксперимента (от 28,95±1,31 на 4 сутки и до 92,55±3,21 на 7 сутки, 91,80±2,27 на 14 сутки, к 30-м суткам - 59,05±3,19). Известно, что экспрессия ТGF-1 прямо пропорционально коррелирует со степенью выраженности воспалительного процесса (Лебедева А.И., 2014). В контрольной группе крыс без лечения высокий уровень экспрессии противовоспалительного цитокина приводил к интенсивной пролиферации фибробластических клеток, известных как источник синтеза коллагена. При этом определялось довольно длительное сохранение струпа и запоздалая эпителизация пораженного участка кожи. В отличие от этого, в опытной группе крыс, где использовали инъекцию аллогенного биоматериала, во все сроки эксперимента степень выраженности воспалительных процессов в очаге поражения была гораздо слабее, чем в контрольной группе, и при этом выявлялся относительно низкий уровень экспрессии фактора фиброза- цитокина ТGF-1. Самый высокий уровень экспрессии ТGF-1 в опытной группе составлял 31,65±1,25 на 14 сутки, но при этом он был почти в 3 раза ниже, чем в контрольной группе в этот срок (P<0,001). Десквамация струпа на ране, вследствие быстрой эпителизации, происходила уже к 7-м суткам. Подкожное введение крысам диспергированного аллогенного биоматериала в зоне химического ожога нивелировало проявление процессов выраженного воспаления и вызывало умеренную фибробластическую реакцию в регенерирующей дермальной пластинке (Муслимов С. А., 2000; Лебедева А.И. с соавт., 2004). В грануляционной ткани под струпом определялось небольшое количество фибробластических клеток, участвующих в репаративных процессах. В таких условиях происходило не ускоренное грубое рубцевание грануляционной ткани, какое выявлялось в контрольной группе, а постепенное медленное формирование более адекватного по структуре соединительнотканного регенерата дермальной пластинки под эпителиальным слоем кожи. При тяжелой степени химического ожога у крыс в соединительнотканной пластинке не регенерировали придатки кожи – сальные и потовые железы, волосяные луковицы. В тех участках, где все же сохранялись отдельные волосяные фолликулы, перечисленные придатки кожи восстанавливались.
Аллогенный биоматериал ингибирует процесс грубого рубцевания тканей после химического ожога кожи у экспериментальных крыс и способствует формированию соединительнотканного регенерата, приближенного по структуре к дермальной пластинке кожи.
1. Лебедева А.И., Муслимов С.А., Мусина Л.А. Динамика экспрессии цитокинов TGF-1 и TNF после введения алло- и ксеногенных биоматериалов// Морфология. - №4 (126).- 2004.- С.70.
2. Лебедева А.И. Аллогенный губчатый биоматериал – ингибитор фиброза поврежденной скелетной мышечной ткани// Российский биотерапевтический журнал. - 2014.- Т.13, № 4.- С.37-44.
3. Мусина Л.А., Нураева А.Б. Заживление ожоговых ран при применении аллогенных биоматериалов (экспериментально-морфологическое исследование) // Вестник ОГУ. –№12 (187). - 2015.- С.142-145.
4. Муслимов С.А. Морфологические аспекты регенеративной хирургии. – Уфа: Башкортостан, 2000. – 168 с.
5. Нураева А.Б., Мусина Л.А., Шангина О.Р. Морфологические изменения в ожоговых ранах кожи после применения биоматериалов Аллоплант® // Морфология. - 2016. – Т. 149.- №3. - С.152.
Шакиров Рустем Франсович – врач-офтальмохирург ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава РФ, 450075, г.Уфа, ул.Р.Зорге, 67/1, тел.: (347) 2- 93-42-35. E-mail: rust.ufa@mail.ru.
Мусина Ляля Ахияровна – док.биол.наук, вед. науч. сотр. отдела морфологии ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава РФ, 450075, г.Уфа, ул.Р.Зорге, 67/1, тел.: (347) 2- 93-42-35. E-mail: morphoplant@mail.ru.
Хасанов Руслан Алмазович – канд.фарм.наук, вед. науч. сотр. лаборатории консервации тканей ФГБУ «Всероссийский центр глазной и пластической хирургии» Минздрава РФ, 450075, г.Уфа, ул.Р.Зорге, 67/1, тел.: (347) 2- 93-42-35. E-mail: morphoplant@mail.ru.
Выявление морфологических изменений в роговице глаза кроликов после химического ожога и перилимбального введения биоматериала Аллоплант.
В качестве экспериментальной модели щелочного ожога роговицы у кроликов применяли метод Obenberger J. (1975). Щелочной ожог роговицы вызывали аппликацией диска фильтровальной бумаги, смоченной 2,5% раствором гидроксида натрия (экспозиция-5 секунд) под местной анестезией (0,4% инокаином). В опытной группе животных (15 кроликов) через 24 часа после ожога делали перилимбальное обкалывание мелко диспергированным биоматериалом Аллоплант «Стимулятор регенерации», который готовили разведением 200мг биоматериала в 5 мл физиологического р-ра. Контрольную группу составили 6 кроликов с ожогами роговицы, но без обкалывания биоматериалом. Глазные яблоки у кроликов энуклеировали на 7, 14, 30, 90 и 180 сутки после операции, фиксировали в 10% забуференном формалине по Лилли. Вырезали роговицу вместе с прилежащей склерой, заливали в парафин. Гистологические срезы окрашивали гематоксилином и эозином, по методам Ван Гизона и Маллори. Использовали микроскоп Leica108MD (Leica, Германия).
В контрольной группе кроликов на 7 сутки после воспроизведения ожога роговицы выявлялось выраженное набухание стромы роговицы с дезорганизацией и гомогенизацией коллагеновых волокон. Участок эпителия в зоне поражения полностью разрушался. На периферии обожженной зоны эпителиальный слой отслаивался. Десцеметова мембрана со слоем эндотелиальных клеток сохранялась. На 14 сутки в строме роговицы отмечалась воспалительная реакция, которая проявлялась миграцией в слои роговицы макрофагов, лимфоцитов и фибробластов. В грануляционной ткани выявлялись даже новообразованные сосуды. Выраженная клеточная реакция в строме с преобладанием фибробластов продолжалась вплоть до 30 суток и заканчивалась в дальнейшем рубцеванием обожженных участков роговицы, что приводило к ее помутнению. Пролиферативная активность эпителиальных клеток роговицы со стороны уцелевших тканей была низкой, поэтому эпителизация передней поверхности стромы по срокам затягивалась и была неравномерной. Восстановившийся эпителий составлял 1 или 2 слоя клеток. Местами наблюдался погружной рост эпителия в сторону стромы.
В опытной группе кроликов воспалительный процесс был менее выраженным. Темпы эпителизации раны и восстановления стромальной пластинки роговицы под эпителием в сравнении с контрольной группой ускорялись. После перилимбального введения ДБМА выявлялось расширение лимбальных сосудов и выход в ткани большого количества мононуклеарных клеток, среди которых большей частью определялись макрофаги. На 7 сутки по периферии поврежденной зоны выявлялся однорядный эпителий, активно пролиферирующий со стороны лимба глаза и наползающий на рану. Определялось уменьшение отека волокнистых пучков в строме и резкое уменьшение за счет этого толщины роговицы. На 14 сутки в строме между коллагеновых волокон определялось усиление фибробластической реакции с разрастанием между ними очень тонких коллагеновых фибрилл, имеющих параллельную ориентацию, что способствовало восстановлению структуры стромы пораженной роговицы. На 21-30 сутки роговица кроликов опытной группы выглядела почти интактной, лишь отличаясь в отдельных участках неравномерной толщиной эпителия. На 90 сутки опыта на гистологических препаратах роговицы представляло уже некоторую сложность определить место ожога. Опираясь на результаты данного исследования и ранее проведенных нами исследований есть все основания полагать, что перилимбально введенный биоматериал Аллоплант опосредованно через макрофаги при помощи клеточных ростовых факторов активирует стволовые эпителиальные клетки, находящиеся в роговице в зоне лимба (палисад Вогта) и участвующие в восстановлении эпителия, а также привлекает из кровотока через лимбальные сосуды стволовые мезенхимальные клетки костномозгового происхождения, которые дифференцируются в фибробласты, синтезирующие коллаген и восстанавливающие строму роговицы (Попандопуло А.Г., 2013; Dua H.S., Azuara-Blanco A., 2000).
Перилимбальное введение диспергированного биоматериала Аллоплант стимулирует регенеративные процессы в патологически измененной роговице и способствует восстановлению всех ее структурных элементов. При этом биоматериал ингибирует процесс грубого рубцевания тканей, приводящее, обычно, к помутнению роговицы.
1. Галимова В.У., Шакиров Р.Ф., Гареев Е.М. Результаты лечения больных кератоконусом диспергированным в различной степени биоматериалом Аллоплант // Офтальмологические ведомости. -2013.-Том VI, № 1. – С. 26-28.
2. Мусина Л.А., Шакиров Р.Ф., Лебедева А.И. Структурные изменения роговицы при кератоконусе // Морфология. - 2016.- Т. 149.- №3. - C.145.
3. Попандопуло А.Г., Кавелина А.С., Иванова О.Н., Дрожжина Г.И. Роль лимбальных клеток в регенерации роговицы / // Таврический медико-биологический вестник. –2013. –Т. 16, No1. –Ч.2. –С. 158–160.
4. Dua H.S., Azuara-Blanco A. Limbal stem cells of the corneal epithelium //Surv. Ophthalmol.-2000 – №44(5) – P. 415-425.
5. Obenberger J. Paper strips and rings as simple tools for standartization of experimental eye injuries // Ophthalmol. Res. – 1975. – Vol. 7. – P. 363–366.
Шангина Ольга Ратмировна – заместитель генерального директора, заведующая лабораторией консервации тканей, доктор биологических наук, профессор. Адрес электронной почты: alloolga@mail.ru
Булгакова Людмила Александровна – научный сотрудник лаборатории консервации тканей, кандидат биологических наук. Адрес электронной почты: mila.bulg@list.ru
Федеральное государственное бюджетное учреждение «Всероссийский центр глазной и пластической хирургии» Министерства здравоохранения Российской Федерации. 450075, г. Уфа, ул. Р. Зорге, 67/1, тел. (347)2328058
Исследовать влияние лиофилизации на физико-механические свойства соединительнотканных аллотрансплантатов.
Для исследования был изъят материал 28 трупов людей обоего пола от 20 до 55 лет. Аллотрансплантаты были изготовлены из следующих анатомических структур: пяточного сухожилия, широкой фасции бедра, твердой оболочки головного мозга, дермы опорных участков стопы. Все образцы были разделены на две группы: первая группа – это нативные ткани (контрольная группа). Вторая группа – ткани, подвергнутые процессу лиофилизации (экспериментальная группа). Для получения достоверных результатов при сравнении нативных и лиофилизированных тканей исследовали образцы однотипной локализации и одного размера: 25 х 15 мм. Образцы лиофилизированных тканей перед проведением физико-механических испытаний помещали в изотонический раствор NаCl на 12 часов с целью регидратации. Испытания образцов проводились на универсальной машине для испытания прочностных свойств материалов модели 1185 INSTRON (Англия). Статистический анализ полученных данных производили, используя методику О.Ю. Ребровой (2002г). Полученные результаты переводились в программу Microsoft Office Excel 2007, затем обработанные данные переводили в программу Stаtisticа 7.0.
Результаты проведенных нами физико-механических исследований показали, что лиофилизация оказывает различное влияние на физико-механические свойства соединительнотканных аллотрансплантатов.
Биомеханические свойства образцов пяточного сухожилия выявлялись при продольном нагружении, так как основу волокнистого остова составляют пучки коллагеновых волокон, большинство из которых ориентированы параллельно длинной оси сухожилия. В результате испытаний образцов пяточного сухожилия были получены следующие показатели: предел прочности образцов контрольной группы равен 17,40±1,74 МПа, тогда как аналогичный показатель образцов экспериментальной группы составил 14,30±2,42 МПа. Предел прочности лиофилизированных образцов снижался в 1,2 раза по сравнению с образцами нативной ткани. Относительное удлинение контрольных образцов пяточного сухожилия составило 16,30±0,57%, в экспериментальной группе – 22,40±5,83%. Значение модуля Юнга у контрольных образцов составило 106,80±6,95 МПа, аналогичный показатель у экспериментальных образцов снизился до 64,70±5,43 МПа. Значение модуля упругости уменьшилось в 1,7 раза, что свидетельствует о снижении прочностных свойств пяточного сухожилия.
1. Меленберг, Т.В. Результаты применения тканевых имплантатов в клинической практике / Т.В. Меленберг, И.В. Болонкин // Инновационные технологии в трансплантации органов, тканей и клеток: матер. Всерос. конф. – Самара, 2008. – С. 79–81.
2. Применение деминерализованного лиофилизированного аллоимплантата в нейрохирургической практике у детей / В.Е. Попов, М.И. Лившиц, А.Б. Карпов [и др.] // Актуальные вопросы тканевой и клеточной трансплантологии: матер. III Всерос. симп. – М.: ЦИТО, 2007. – С. 145–146.
3. Способ изготовления лиофилизированного аллотрансплантата кости / В.Б. Хватов, А.В. Свищев, А.Ю. Ваза, Н.В. Боровкова [и др.] // Трансплантология. – 2016. № 1. С13-18.
4. Третьяков, В.Б. Артроскопическая реконструкция изолированных повреждений передней крестообразной связки аллогенным лиофилизированным трансплантатом связки надколенника / В.Б. Третьяков, Л.И. Малюченко // Вестник травматологии и ортопедии им. Н.Н. Приорова. – 2013. – № 3. – С.31–35.
5. Омельяненко, Н.П. Соединительная ткань (гистофизиология и биохимия) / Н.П. Омельяненко, Л.И. Слуцкий; под ред. акад. РАН и РАМН С.П. Миронова. – М.: Издательство «Известия», 2009. – Т. I. - 380 с.
6. Climicаl, histologic, аnd histomorphometric аnаlyses of regenerаted bone in mаxi-llаry sinus аugmentаtion using fresh frozen humаn bone аllogrаfts / C. Stаcchi, G. Orsini, D. Di Iorio [et аl.] // J. Periodontol. – 2008. – Vol. 79, № 9. – P. 1789–1796.
Шангина Ольга Ратмировна – доктор биологических наук, профессор, заместитель генерального директора, заведующая лабораторией консервации тканей ФГБУ «Всероссийский центр глазной и пластической хирургии» МЗ РФ. 450075 г.Уфа, ул.Р.Зорге 67/1; тел. (3472) 32-80-58; alloоga@mail.ru.
Гайнутдинова Раушания Дамировна – научный сотрудник лаборатории производства трансплантатов ФГБУ «Всероссийский центр глазной и пластической хирургии» МЗ РФ. 450075 г.Уфа, ул.Р.Зорге 67/1; тел. (3472) 32-80-58; rushanagai@mail.ru
Изучение воздействия лазерного излучения на структуру
соединительнотканных трансплантатов.
Всего для исследования был взят материал от 20 трупов людей обоего пола от 20 до 55 лет. Для исследования использовались трансплантаты, изготовленные из различных видов соединительной ткани: рыхлой волокнистой соединительной ткани (висцеральные оболочки внутренних органов, фасции), плотной неоформленной волокнистой соединительной ткани (дерма, твердая оболочка головного мозга), плотной оформленной волокнистой соединительной ткани (сухожилия различных локализаций). Этап моделирования образцов биоматериалов проводили с использованием
комплекса лазерного моделирования биоматериалов. Данный комплекс предназначен для использования в медицине с целью автоматизации процесса изготовления трансплантатов и обеспечивает высокопроизводительную резку заготовок биологических тканей на заданные геометрические формы хирургических имплантатов. Для изучения структуры биологических тканей после воздействия лазерного
излучения использовали набор методик от макроскопического до электронно-микроскопического уровня. Гистологические препараты окрашивали гематоксилином и эозином, по Ван-Гизону, Вейгерту, Маллори. Ультраструктуру тканей исследовали используя сканирующую электронную микроскопию. Для оценки фиброархитектоники биоматериалов применяли метод количественного поляризационно-оптического анализа. В основе метода - способность волокнистых компонентов соединительной ткани к двойному лучепреломлению.
Анализ полученных данных показал следующее: у трансплантатов твердой мозговой оболочки и пяточного сухожилия в зоне лазерного реза происходит частичная гомогенизация пучков коллагеновых волокон, которая наиболее выражена у края трансплантата, т.е в зоне прохождения луча лазера. По мере отдаления от зоны реза степень гомогенезации пучков коллагеновых волокон уменьшается. Максимальная ширина зоны деструкции достигает 4 мкм. Подобная картина наблюдается и при исследовании трансплантатов дермы. У данных трансплантатов в зоне лазерного реза пучки коллагеновых волокон теряют структурную организацию и приобретают вид аморфной массы. Ширина зоны деструкции пучков коллагеновых волокон трансплантатов дермы достигает 5 мкм.
У трансплантатов, изготовленных из фиброзной капсулы почки и глиссоновой капсулы печени, в зоне лазерного воздействия наблюдаются редкие очаги деструкции пучков коллагеновых волокон в виде набухания и частичной дезорганизации последних. Максимальная ширина таких очагов не превышает 1мкм. В целом структурная организация в зоне лазерного реза у трансплантата фиброзной капсулы почки и глиссоновой капсулы печени не изменяется.
Полученные данные, на наш взгляд, связаны с особенностями фиброархитектоники исследуемых тканей, а именно: плотное расположение коллагеновых волокон и наличие эластических, приводит к более выраженным деструктивным изменениям в зоне лазерного реза у трансплантатов твердой мозговой оболочки и дермы.
В заключение можно сказать следующее: структурные изменения соединительной ткани в зоне лазерного реза в значительной степени определяются плотностью упаковки волокнистого матрикса и наличием межклеточного вещества. Так, для рыхлой волокнистой соединительной ткани характерна относительно узкая зона деструкции (около 1 мкм) с вариабельной глубиной термического воздействия. По-видимому, это связано с чередованием участков волокнистого и аморфного внеклеточного матрикса. В плотной соединительной ткани наблюдается более широкая (до 5 мкм) линия деструкции при относительно ровной ее глубине. Данный факт мы связываем с равномерным и компактным расположением пучков коллагеновых волокон.
1. Мулдашев, Э.Р. Теоретические и прикладные аспекты создания аллотрансплантатов серии «Аллоплант» для пластической хирургии лица: автореф. дис….д–ра мед.наук. – СПб., 1994. – 40 с.
2. Рябова, М.А. Роль изучения эффектов лазерного излучения на биологическую ткань в разработке методов лазерной хирургии в оториноларингологии //Вестник оториноларингологии. -2008.-№4. –С.13-17.
3. «Умные» лазерные скальпели для роботизированной хирургии /А.К. Дмитриев, А.К. Коновалов, В.Н. Кортунов, В.А.Ульянов //Альманах клинической медицины.-2016.-Т.44, №2.-С.172-178.
4. Шумаков, В.И. Трансплантация органов и тканей – настоящее и будущее /В.И. Шумаков. //Реконструктивная и трансплантационная хирургия: сб.науч.тр. – Ростов н/Д., 2000. – С. 163-166.
5. Arndt, K.A. Laser in dermatology /K.A. Arndt. //Arch. Dermatol. – 1982. – Vol. 118, № 5. – Р. 283.
6. Grover, R. Laser technology /R. Grover. //BMJ. – 1998. – Vol. 317. – P. 397-400.