|
Хирургическая
реабилитация больных анофтальмом на основе применения биоматериалов Аллоплант Кульбаев Н.Д. Актуальность По данным Р.А.Гундоровой (1980) в лечебных
учреждениях страны за год производится более 3500 энуклеаций и более 5000
человек нуждаются в протезировании. В связи с учащением огнестрельных ранений
боевого и криминального происхождения этот вопрос на сегодняшний день стоит
особенно остро (Р.А.Гундорова, А.В.Степанов, О.И.Кваша, 1995). Другие авторы приводят данные о необходимости
удаления глазного яблока в России более чем у 12 тысяч пациентов (Ю.А.Чеглаков,
А.Ц.Лясковик, 1995, 1997). Эти авторы указывают, что в 2/3 случаях не
формируется опорно-двигательная культя. Вышеуказанные причины приводят к недостаточности опорно-двигательной культи и
образованию огромной конъюнктивальной полости. При протезировании в таких
случаях используются тяжелые большие глазные протезы, которые не только не
устраняют косметический дефект, но приводят
к провисанию нижнего века (Kaltreider S.A.,
2000). Для профилактики и устранения этих недостатков применяется несколько
методов хирургического лечения. Формирование первичной или вторичной
опорно-двигательной культи, как правило, устраняет вышеперечисленные дефекты.
Другие виды оперативного лечения лишь дополняют косметический эффект. При первичной и вторичной имплантации
опорно-двигательной культи используется большое количество материалов. Согласно
международной классификации трансплантатов (Вена, 1967) их принято делить по
происхождению на аутологичные (ткани самого больного), аллогенные (ткани
донора), ксеногенные (ткани животных) и эксплантаты (чужеродные небиологические
материалы) (Шиф Л.В., 1973; Гундорова Р.А. с соавт., 1996; Коваленко П.П.,
2000). Среди аутологичных трансплантатов
типичным является подкожная жировая клетчатка (Покровский А.И., 1959; Плешаков
В.В., Федотов В.Г., 1981). У данного материала имеются существенные недостатки:
нанесение больному дополнительной травмы, плохая приживлямость и быстрая
резорбция (Филатов В.П., 1933; Покровский А.И., 1944; Мухамеджанова М.М.,
1966). Аналогичные недостатки имеют кожа
с подкожно-жировой клетчаткой (Соколенко О.М., 1963; Цветков В.Л., Н.В.Цветков
Н.В., 1987), широкая фасция бедра, у реберный хрящ и т.д. (Шиф Л.В., 1973). Аллогенные трансплантаты, как правило, это
трупные ткани: реберный хрящ (Свердлов Д.Г., 1941; Гундорова Р.А., Катаев М.Г.,
1987), который имеет малый объём (Беликова Л.П., 1944) и быстро рассасывается
(Зайкова М.В., 1969), склера (Медведев Н.И., 1942; Чеканов Ю.Н., 1976), твердая
мозговая оболочка (Грязнова И.И., 1968) и костная ткань (Мазурян А.В., 1985) -
вызывают выраженную послеоперационную реакцию, что приводит к рассасыванию и
потере объёма культи (Шиф Л.В., 1973). Ксенотрансплантация не получила широкого
распространения ввиду иммунологического барьера межвидовой несовместимости
тканей (Жаворонков Н.А., Перельман М.И., 1993). Эксплантаты, изготовленные из инертных
металлов, представляют в настоящее время лишь исторический интерес (Doherty,
1923; Freiberger, 1937). При применении синтетических материалов наблюдается
множество осложнений, среди которых обнажение имплантатов и их отторжение (Филатова И.А., Катаев М.Г.,
1996; Горячев Ю.Е. с соавт., 1996; С.Н.Федоров
С.Н. с соавт., 1998). Использование в качестве имплантата природных материалов,
таких как гидроксиапатит, получило большое распространение (David
R. Jordan, Stanley
Chan, Louise Mawn
et al., 1999; Philip
L. Ouster, Kathryn
M. T-rinkaus,
Jane Fornoff, 1999). Недостатками
данного материала является выраженный отек конъюнктивы, сильная
послеоперационная боль (Edelstein C,
Shields CL, De
Potter P, Shields
JA, 1997; Oestreicher JH,
Liu E, Berkowitz M, 1997). Кроме того,
высокая цена данного имплантата делает его недоступным для большей части
нуждающихся пациентов (Филатова И.А., Катаев М.Г., 1996). Осложнения в виде обнажения и выталкиваний
эксплантатов или трансплантатов не идентичны при имплантации сходных типов
материалов для формирования опорно-двигательной культи. Причиной возникновения
или не возникновения осложнения могут быть: надежность гемостаза; соответствие
объёма имплантата размерам полости теноновой капсулы; шовный материал для
фиксации мышц и ушивания теноновой капсулы; время снятия швов; поведение
больного в первые 3-5 недель после операции; растяжение и разрыв тканей у
передней поверхности жесткого имплантата (Шиф Л.В., 1973). Многие перечисленные
причины относятся к той категории, где имеют место тактика лечения и опыт
лечащего врача данной категории больных. Свойства трансплантатов и
эксплантатов, применяемых для формирования опорно-двигательной культи,
перечислены выше. Применяемый для фиксации прямых мышц глазного яблока и
герметизации теноновой капсулы в качестве шовного материала кетгут к 5-му дню
теряет половину первоначальной крепости, а к 10-му дню прочность их ничтожна.
За этот короткий период сохранения прочности кетгута мышцы и теноновая капсула
не успевают надежно срастаться. Другие небиологические шовные материалы имеют
отрицательные свойства, такие как прорезывание, инкапсуляция и лигатурные
свищи. Учитывая ненадежность кетгута и других небиологических шовных
материалов, мы обратили внимание на аллосухожильные нити, применяемые в
челюстно-лицевой хирургии в качестве
погружного шовного материала, которые испытывают значительную статическую и
динамическую нагрузку (Юсупбаев Б.С., Мулдашев Э.Р., 1977; Булатов Р.Т., 1981;
Гурьянов А.С., 1993; Гурьянов А.С., Салихов А.Ю., 1994; Булатов Р.Т. с соавт.,
1997). При других офтальмопластических оперативных
вмешательствах, в частности, при
устранении недостаточности нижнего века, используются модифицированные
трансплантаты и эксплантаты из вышеперечисленных материалов (Катаев М.Г., 1983;
1986; Морозова О.Д., 1980; Кирилличев А.И., 1981). Таким образом, многие трансплантаты и
эксплантаты, применяемые при анофтальмическом синдроме, не отвечают следующим
требованиям: низкому удельному весу, незначительной резорбционной способности,
хорошей переносимости тканями, отсутствию канцерогенных свойств, способности к
формообразованию, отсутствию аллергических реакций, хорошей стерилизуемости
(Шкромида М.И., Мосяк М.А., 1991; Филатова И.А., Катаев М.Г., 1996). В Государственном учреждении «Всероссийский
центр глазной и пластической хирургии» Министерства здравоохранения Российской
Федерации (директор д.м.н., профессор Э.Р. Мулдашев) разработан и выпускается
серийно ряд биоматериалов Аллоплант для различных пластических операций,
которые практически отвечают вышеизложенным требованиям. Целью исследования являются разработка и внедрение методов
хирургической реабилитации больных анофтальмом с применением биоматериалов Аллоплант. Материалы и методы
исследования С применением биоматериалов Аллоплант
пролечено 334 пациента. Формирование опорно-двигательной культи из
биоматериалов Аллоплант было произведено в 347 случаях. Наблюдаемые нами
пациенты были подразделены на три группы
по срокам формирования опорно-двигательной культи. В первую группу вошли 135
пациентов, которым после энуклеации первично была сформирована
опорно-двигательная культя из биоматериала Аллоплант. Техника
операции формирования опорно-двигательной культи из биоматериалов Аллоплант
после энуклеации. Под общей анестезией, после обработки
операционного поля на веки накладывали блефаростат. Микрохирургическим пинцетом
фиксировали конъюнктиву глазного яблока и делали её надрез у лимба. При помощи
изогнутых ножниц через сформированный надрез отсекали конъюнктиву вокруг лимба.
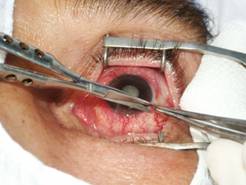
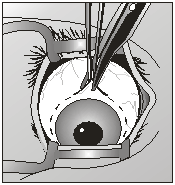
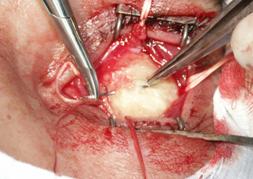
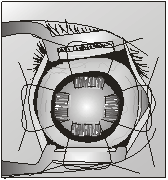
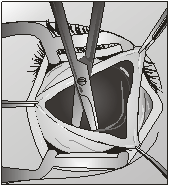
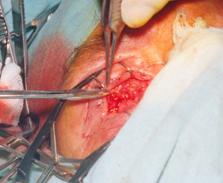
Разрез необходимо производить как можно ближе к лимбу, тем самым максимально
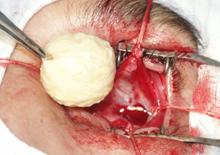
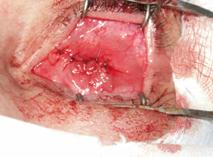
сохранив и минимально травмируя конъюнктиву (рис. 1).
Рис. 1. Разрез
конъюнктивы вокруг лимба Далее
отсепаровывали конъюнктиву и теноновую оболочку тупым путем изогнутыми
ножницами. Имеющиеся рубцы и спайки пересекали, не повреждая склеру. После
отсепаровки конъюнктивы и теноновой оболочки выделяли прямые глазные мышцы. В
первую очередь выделяли верхнюю прямую мышцу с помощью мышечного крючка. Мышцу
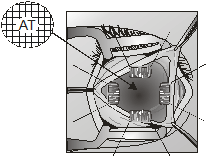
прошивали аллосухожильной нитью и пересекали у места прикрепления к склере (рис.
2).
Рис. 2. Выделение прямых
мышц глазного яблока и прошивание их аллосухожильными нитями Аналогичные действия проводили с нижней и
наружной прямыми мышцами. Внутреннюю прямую мышцу прошивали аллосухожильной
нитью, отступя от места прикрепления к склере на 5-6 мм. Пересекали мышцу таким
образом, чтобы оставалась культя на глазном яблоке длиной 3-5 мм. Культю
использовали для фиксации глазного яблока с помощью кровоостанавливающего
зажима. Мобилизованное глазное яблоко легко вывихивалось. При помощи зажима
глазное яблоко вытягивали вперед, повторяя поворот глазного яблока кнаружи
вокруг вертикальной оси. После этого зрительный нерв становится доступным для
перерезки. Изогнутые бранши ножниц
проводили в сомкнутом положении с медиальной стороны к зрительному
нерву. Концом ножниц нащупывали зрительный нерв, далее чуть вытягивали ножницы
и разводили бранши. Раздвинутыми браншами ножницы вновь продвигали в глубь
орбиты так, чтобы зрительный нерв попал между браншами. В таком положении
бранши ножниц отодвигали от склеры на 2-4 мм и одним движением пересекали
зрительный нерв. Глазное яблоко подтягивали вперед и пересекали сухожилия обеих
косых мышц у склеры. После удаления глазного яблока проводили гемостаз путем тампонады
полости орбиты марлевой салфеткой, смоченной в растворе перекиси водорода.
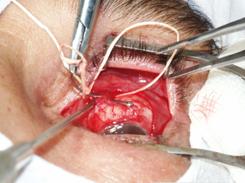
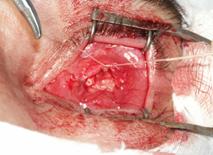
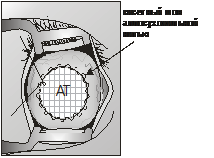
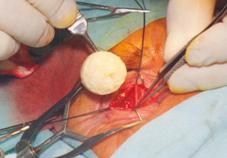
После удаления тампона в полость орбиты имплантировали Аллоплант для
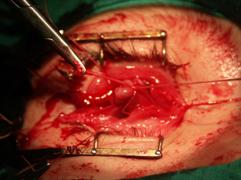
формирования опорно-двигательной культи (рис. 3).
Рис. 3. Имплантация биоматериала Аллоплант
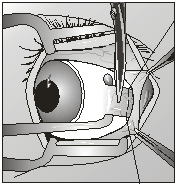
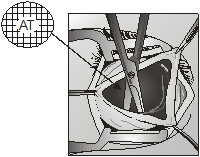
для формирования опорно-двигательной культи Прямые мышцы глазного яблока соединяли между
собой над Аллоплантом для формирования опорно-двигательной культи, используя
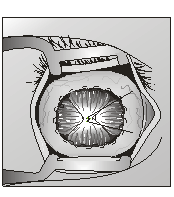
ранее наложенные аллосухожильные нити (рис. 4).
Рис. 4. Перекрестное
соединение прямых мышц глазного яблока над биоматериалом Аллоплант При соединении мышц
использовали парное соединение мышц-антогонистов. В некоторых случаях прямые
мышцы глаза были фиксированы кпереди от
экватора опорно-двигательной культи на 4-5 мм (рис. 5).
Рис. 5.
Фиксация прямых мышц глазного яблока к
биоматериалу Аллоплант для формирования опорно-двигательной культи ранее
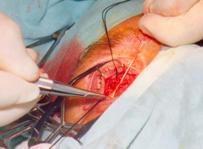
наложенными аллосухожильными нитями Следующим этапом герметично ушивали тенонову
оболочку аллосухожильными нитями. На данном этапе накладывали кисетный шов,
иногда узловые швы. Узлы погружали в рану, то есть в тенонову полость (рис. 6).
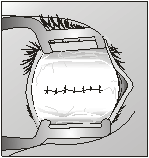
Рис. 6. Наложение на
тенонову капсулу кисетного шва аллосухожильной нитью На конъюнктиву накладывали
узловые швы викрилом 3-4/0 (рис. 7).
Рис. 7. Ушивание
конъюнктивальной раны Вторая группа состояла из 199 пациентов,
которым была произведена отсроченная имплантация опорно-двигательной культи при
анофтальме. Техника
операции отсроченной имплантации опорно-двигательной культи из биоматериалов
Аллоплант. Под наркозом устанавливали блефаростат и
хирургическим пинцетом захватывали конъюнктиву с теноновой капсулой. Делали
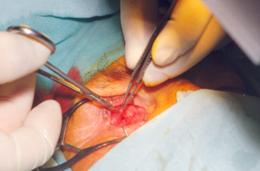
сквозную насечку в нижне-наружном или верхне-наружном секторе ближе к центру (рис.
8).
Рис. 8. Захват
конъюнктивы с подлежащими тканями и нанесение сквозной насечки В рану вставляли одну из браншей ножниц и
разрез продолжали, учитывая ход мышц. Длина разреза должна превышать диаметр
Аллопланта. Тенонову оболочку брали на четыре шва-держалки. В полость орбиты
вводили зажим Кохера в сомкнутом положении и в глубине орбиты бранши зажима
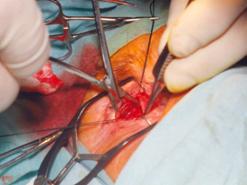
раздвигали, не применяя усилий, тем самым создавая ложе для Аллоплантата (рис. 9).
Рис. 9. Формирование
ложа в полости орбиты с помощью зажима Кохера Ревизию ложа производили пальпаторно. Ослабив
блефаростат и используя швы-держалки, в полость орбиты вводили Аллоплант для
формирования опорно-двигательной культи. Для удобства и жесткой фиксации
Аллопланта использовали зажим Кохера (рис. 3.10).
Рис. 10. Имплантация
в полость орбиты Аллопланта для формирования опорно-двигательной культи После имплантации производили пальпаторный
контроль положения имплантата. Он должен находится в мышечной воронке. Края
теноновой оболочки и конъюнктивы освобождали, если они были завернуты вместе с
Аллоплантом. Рану ушивали послойно, герметично: на тенонову оболочку
накладывали шов аллосухожильной нитью (рис. 11).
Рис. 11. Ушивание
теноновой капсулы аллосухожильной нитью На конъюнктиву
накладывали узловые швы викрилом 3-4/0 (рис. 12.).
Рис. 12. Ушивание
конъюнктивальной раны Третья группа состояла из 12 пациентов,
которым отсроченная имплантация опорно-двигательной культи производилась
неоднократно (в 11-ти случаях 2 раза и в 1-ом случае 3 раза). Хирургическая
техника повторной имплантаций опорно-двигательной культи с биоматериалом
Аллоплант Под
общей анестезией после обработки операционного поля, на веки накладывали
блефаростат. Тщательно производили ревизию конъюнктивальной полости и глазного
протеза. При этом отмечали состояние сводов, форму и размеры культи. При
осмотре глазного протеза фиксировали внимание, на какой части протеза имеются
дополнительные увеличенные части. Разрез конъюнктивы и теноновой капсулы
производили в тех секторах, где имелся наибольший дефицит тканей. Формирование
ложа для биоматериала Аллоплант производили тупым методом с помощью зажима
Кохера. Ранее имплантированный
биоматериал Аллоплант в течение 1 года представлял собой нежную соединительную
ткань с большим количеством элементов жировой клетчатки. Формирование ложа для
предстоящей имплантации биоматериала не представляло особых трудностей.
Моделирование биоматериала Аллоплант производили с учетом ревизии
конъюнктивальной полости и глазного протеза. Смоделированный и
трансплантированный биоматериал Аллоплант устранял недостатки
опорно-двигательной культи и видоизменял конъюнктивальную полость для
стандартного тонкостенного глазного протеза. Моделирование сложной по форме и
различного объёма имплантатов возможно благодаря уникальным и пластичным
свойствам данного вида биоматериала Аллоплант. Герметизацию теноновой капсулы
проводили наложением кисетного или узлового шва из аллосухожильной нити
Аллоплант. На конъюнктиву накладывали узловые швы викрилом 3-4/0. На
операционном столе подбирали соответствующий по размерам и цвету стандартный
глазной протез. Все три группы прослежены сроком свыше 10-ти
лет с естественной убылью количества наблюдаемых пациентов. В процессе
исследования возникли сложности в оценке косметического результата после
хирургической реабилитации больных с анофтальмом, так как по литературным данным
имеется объективная оценка тех или иных параметров, но нет оценки в
совокупности этих данных. Таким образом, нет общепринятого и стандартного
метода оценки косметического эффекта. На основе общепринятых методов
обследования пациентов с анофтальмом (Л.В.
Шиф, 1981) был разработан метод полуколичественной оценки косметического
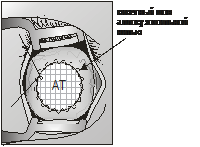
результата в баллах (табл. 1). Таблица 1 Метод
оценки косметического результата по объективным признакам в баллах
По истечении 3 – 6 месяцев после операции и
подбора индивидуального глазного протеза в лаборатории полимерных медицинских
изделий и индивидуального протезирования был проведен анализ с использованием
данного метода объективной оценки косметического результата в хирургической
реабилитации пациентов с анофтальмом. Удаление глазного яблока с формированием
опорно-двигательной культи из биоматериалов Аллоплант проведено 135 пациентам.
В отдаленные сроки наблюдения отмечалось стойкое сохранение хорошего косметического
результата в пределах 97,4 - 98,3%. Отсроченная
имплантация опорно-двигательной культи из биоматериалов Аллоплант проведена 199
пациентам. В отдаленные сроки косметический результат в целом стабилен, но с
некоторой тенденцией уменьшения показателей в группе «хороший» результат с 95,9
до 94%, увеличение в группе «неудовлетворительный» с 0 до 1,5% и в группе «удовлетворительный» с 4,1 до
4,5%. Повторные
имплантации опорно-двигательной культи были проведены 12 пациентам, из них
одному пациенту 3 раза. Раннее послеоперационное течение протекало без
особенностей. Через 4-6 месяцев производили индивидуальное глазное протезирование.
В отдаленные сроки «хороший» косметический результат с 83,3 (в сроки наблюдения
до 5 и до 10 лет) до 100 % (свыше 10 лет). Таким
образом, в группе больных, которым было проведено удаление глазного яблока с
формированием опорно-двигательной культи из биоматериалов Аллоплант, в сроки
наблюдения до 5 и до 10 лет существенными факторами, влияющими на субъективную
оценку самого больного, оказались категории «западение глазного протеза»,
«западение верхней орбито-пальпебральной борозды» и «объём движения глазного
протеза». Два других фактора - «косоглазие» глазного протеза и симметричность
глазных щелей, не играли существенной роли в этих сроках наблюдения. Это
объясняется тем, что пациенты сроком наблюдения до 10 лет после удаления
глазного яблока обращают внимание на те факторы, которые появились с
отсутствием глазного яблока (объём движения глазного протеза, степень западения
глазного протеза и верхней орбито-пальпебральной борозды). Остальные факторы,
как правило, имели место до операции (косоглазие больного глаза и асимметрия
глазной щели). В
сроки наблюдения более 10 лет в группе с первичным формированием
опорно-двигательной культи из биоматериалов Аллоплант со стабилизацией
фундаментальных признаков (западение глазного протеза, верхней
орбито-пальпебральной борозды и амплитуды движения глазного протеза) внимание
пациентов переключается на более мелкие детали косметического состояния,
которые могли присутствовать до операции (косоглазие больного глаза и
асимметрия глазной щели). Совершенно
другая картина в группе с отсроченной имплантацией опорно-двигательной культи
из биоматериала Аллоплант. Практически во всех случаях во время удаления
глазного яблока не была сформирована опорно-двигательная культя. Вследствие
этого у большинства пациентов наблюдались западение верхней
орбито-пальпебральной борозды и небольшой объём движения глазного протеза. Во
все сроки наблюдения в послеоперационном периоде наибольший вклад в оценку
субъективной удовлетворенности пациента вносили эти два фундаментальных фактора. Степень западения глазного протеза и
симметричность глазных щелей оказывали переменное влияние на субъективную
оценку, но существенно на неё не влияли. Уровень «косоглазия» глазного протеза
в данной группе пациентов на субъективную оценку самого пациента не влиял во
всех сроках наблюдения. Подтверждением
клинических результатов является анализ полученных данных
клинико-морфологического исследования биопсийного материала. Он который
показал, что через 1 год после трансплантации биоматериала Аллоплант для формирования
опорно-двигательной культи отмечалось формирование зрелой неоформленной
соединительной ткани в области локализации жировых долек трансплантата с
очаговой инфильтрацией фибробластов. Зрелая неоформленная соединительная ткань
имела зрелые сосуды (артериолы, капилляры, венулы) с упорядоченным
направлением, которые формировали замкнутое микроциркуляторное русло. Через 5
лет наблюдалась оформленная соединительная ткань, которая состояла из
упорядоченных коллагеновых волокон различной толщины. Клеточная плотность была
очень низкой за счет диффузно рассеянных единичных фибробластов и фиброцитов.
Сформированный регенерат обладает хорошо развитой сосудистой сетью с
упорядоченным направлением дифференцированных сосудов. Таким
образом, полное формирование новообразованной ткани на месте имплантированного
биоматериала Аллоплант для создания опорно-двигательной культи происходило в сроки до 5 лет после имплантации.
Новообразованный регенерат представлял собой дифференцированную соединительную
ткань из плотной оформленной соединительной ткани и жировой ткани с развитой
сосудистой сетью. Данная фиброархитектоника регенерата, по-видимому,
обусловлена выполняемой функциональной нагрузкой. Структура
аллосухожильных нитей была представлена фрагментами плотной оформленной
соединительной ткани, построенной из толстых коллагеновых волокон на 2-3-й
месяцы после проведения оперативного лечения. Через 5 месяцев после операции
картина трансформации волокон аллосухожильных нитей выглядела неоднородно. В
некоторых участках, преимущественно по краю, наблюдалась незрелая
соединительная ткань с нежным соединительно-тканным каркасом и большим
количеством фибробластов. Таким
образом, в результате макрофагально-фибробластической реакции аллосухожильные
нити полностью трансформируются в новообразованную соединительную ткань в
течение 5 месяцев после операции. При этом можно предположить, что картина
замещения зависит от типа перифокальной соединительной ткани и характера
функциональной нагрузки. Исходя
из анализа результатов исследования, можно констатировать: 1.
Стабильный
косметический результат можно ожидать по истечении 1 года, а окончательный
результат - через 5 лет по мере формирования полноценной опорно-двигательной
культи. 2.
Применение
аллосухожильных нитей снижает послеоперационные осложнение, такое как
расхождение послеоперационного шва с последующей потерей имплантата. 3.
Выявленные
недостатки биоматериала Аллоплант для формирования опорно-двигательной культи
легко устранимы. В определенных условиях недостатки данного материала играют положительную
роль в процессе лечения. Дробное введение биоматериала Аллоплант в полость
орбиты продиктовано тем, что через год морфологически отмечается образование
зрелой неоформленной соединительной ткани, а
полное замещение небольшого объема от 3 до 5,6 см3
происходить в течение 5-ти лет. С увеличением объёма биоматериала отмечается
удлинение этих сроков. Дозированная имплантация биоматериала Аллоплант при
анофтальмическом синдроме после лучевой терапии по поводу ретинобластомы
позволяет компенсировать дефицит мягкой ткани в области поражения, не вызывая
осложнения в виде некрозов кожи и т.д. Сопоставляя
полученные данные с литературными данными, можно сказать, что оголение
биоматериала Аллоплант не наблюдалось. По литературным данным это осложнение
составляет при применении хряща различного происхождения от 4,7 до 12,2 % (Катаев М.Г., 1981; Каспаров
А.А. с соавт., 1984). Применение
данного вида биоматериала Аллоплант дает наилучший результат по сравнению
широко применяемыми имплантатами (Федорищева Л.Е. с соавт., 2002). Таким образом, разработанные нами методы
хирургической реабилитации больных анофтальмом с применением биоматериалов
Аллплант позволяют сформировать оптимальную для эффективного косметического
глазного протезирования опорно-двигательную культю, а разработанные нами критерии полуколичественной оценки
результатов хирургического лечения и индивидуального косметического глазного
протезирования определить их эффективность. Заключение
и практические рекомендации Разработаны и внедрены эффективные методы
хирургической реабилитации больных анофтальмом с применением биоматериала
Аллоплант для формирования опорно-двигательной культи и аллосухожильных нитей
Аллоплант. Морфологически на биопсийном материале
установлено, что биоматериал Аллоплант для формирования опорно-двигательной
культи шаровидной формы после имплантации в тенонову полость постепенно (в
сроки до 5 лет) замещается новообразованной дифференцированной соединительной
тканью с развитой сосудистой сетью, соответствующей по фиброархитектонике
выполняемой ею функции. Аллосухожильные нити, применяемые для
наложения кисетного шва на тенонову оболочку, прочно фиксируют имплантированный
биоматериал в сроки наблюдения до 1 года постепенно замещаются новообразованной
тканью, подобной по структуре исходной нити. Метод первичной имплантации биоматериала
Аллоплант для формирования опорно-двигательной культи после энуклеации
позволяет получить хорошие косметические результаты в сроки наблюдения до 5
лет, до 10 лет и более в 97,4 - 98,3% случаев. Метод отсроченной имплантации
опорно-двигательной культи из биоматериалов Аллоплант при анофтальме позволил
добиться хорошего косметического протезирования
в сроки наблюдения до 5 лет, до 10 лет и более в 94 - 95,9% случаев. Применение биоматериала Аллоплант для формирования
опорно-двигательной культи при повторной отсроченной имплантации с целью
дополнения объёма опорно-двигательной культи позволило улучшить эффективность
хирургической реабилитации во все сроки наблюдения и получить хороший
косметический результат у 83,3% больных анофтальмом в сроки наблюдения до 5 и
до 10 лет, у 100% больных более 10 лет. Показанием к применению биоматериалов
Аллоплант в качестве трансплантата для формирования опорно-двигательной культи
являются энуклеация, анофтальм без опорно-двигательной культи и недостаточный
размер опорно-двигательной культи. Противопоказанием являются наличие
злокачественного новообразования, прорастающего за пределы глазного яблока,
явное инфицирование полости орбиты и размозжение мягких тканей орбиты. Разработанный нами метод количественной
оценки результатов хирургической реабилитации больных анофтальмом эффективен и
может быть использован в практике врачей-офтальмологов и глазных
протезистов. Практические
рекомендации С целью повышения эффективности хирургической
реабилитации пациентов анофтальмом и получения хорошего косметического глазного
протезирования рекомендуется использовать для формирования опорно-двигательной
культи из биоматериала Аллоплант. С целью прочной фиксации опорно-двигательной
культи в полости орбиты рекомендуется накладывать на тенонову оболочку шов из
аллосухожильных нитей Аллоплант. Для определения эффективности хирургической
реабилитации и косметического глазного протезирования пациентов анофтальмом
рекомендуется использовать разработанные нами критерии полуколичественной
оценки результатов. Литература
1.
Анофтальмический
синдром. Новые тенденции в тактике лечения // Новые технологии микрохирургии
глаза. – Оренбург, 1996. –С. 66. (Соавт.: Булатов Р.Т.). 2.
Формирование
опорно-двигательной культи после энуклеации глазного яблока // Актуальные
проблемы современной офтальмологии. – Саратов, 1996. -С. 9-10. (Соавт.: Булатов
Р.Т., Мулдашев Э.Р., Салихов А.Ю., Рыжов В.А., Родионов О.В.). 3.
Профилактика синдрома моторной
десинхронизации опорно-двигательной культи при энуклеации // Материалы XII научно-практической конференции «Новые технологии
микрохирургии глаза». - Оренбург, 2001. -С. 182-183. (Соавт.: Булатов Р.Т., Родионов О.В.,
Рыжов В.А.). 4.
Альтернативный
метод обезболивания при пластических операциях на нижней стенке орбиты и нижнем
веке // Медико-социальная реабилитация офтальмологических больных. – Тюмень,
1998. -С. 18. (Соавт.: Князев А.Д., Салихов А.Ю., Галимова Л.Ф., Малоярославцев
В.Д.). 5.
Хирургическое
лечение анофтальмических синдромов после энуклеации с лучевой терапией по
поводу ретинобластомы // Новые технологии микрохирургии глаза. – Оренбург,
1996. -С. 98-99. 6.
К
вопросу стабилизации результатов формирования опорно-двигательной культи после
энуклеации // Медико-социальная реабилитация офтальмологических больных. –
Тюмень, 1998. -С. 38. (Соавт.: Булатов Р.Т., Мулдашев Э.Р., Родионов О.В.,
Салихов А.Ю.). 7.
Формирование
опорно-двигательной культи после энуклеации глазного яблока //
Медико-социальная реабилитация офтальмологических больных. – Тюмень, 1998. -С.
37-38. (Соавт.: Булатов Р.Т., Мулдашев Э.Р., Салихов А.Ю, Рыжов В.А., Родионов
О.В.). 8.
Отсроченная
имплантация опорно-двигательной культи после энуклеации глазного яблока //
Актуальные проблемы современной офтальмологии. – Саратов, 1996. -С. 56.
(Соавт.: Булатов Р.Т., Мулдашев Э.Р., Салихов А.Ю., Рыжов В.А., Родионов О.В.). 9.
Отсроченная
имплантация опорно-двигательной культи материалом серии «Аллоплант» при
анофтальме // Медико-социальная реабилитация офтальмологических больных. –
Тюмень, 1998. -С. 38-39. (Соавт.: Мулдашев Э.Р., Салихов А.Ю., Булатов Р.Т.,
Рыжов В.А. ). 10.
Отсроченная
имплантация опорно-двигательной культи материалом серии «Аллоплант» при
анофтальме // Актуальные вопросы офтальмологии, посвященные 170-летнему юбилею
Московской офтальмологической клинической больницы. – М., 1996. -С. 215-216. 11.
Опыт
использования чечевицеобразных лечебных протезов для формирования
конъюнктивальной полости // Материалы I Евро-Азиатской
конференции по офтальмохирургии. - Екатеринбург, 1998. -С. 121-122. (Соавт.:
Рыжов В.А., Салихов А.Ю.). 12.
Аллопластическое
расширение конъюнктивальной полости при анофтальмическом синдроме // Новые
технологии микрохирургии глаза. - Оренбург, 1994. –С. 113-115. (Соавт.:
Мулдашев Э.Р., Булатов Р.Т., Салихов А.Ю., Рыжов В.А.). 13.
Реконструкция
конъюнктивальной полости при анофтальме // Новые технологии микрохирургии
глаза. – Оренбург, 1994. –С. 112-113. (Соавт.: Мулдашев Э.Р., Булатов Р.Т.,
Салихов А.Ю., Рыжов В.А.). 14.
Морфологические
аспекты пересадки аллотрансплантатов для фиксирующей пластики // Актуальные
проблемы клинической офтальмологии. – Челябинск, 1999. -С. 201-203. (Соавт.:
Мулдашев Э.Р., Салихов А.Ю., Искандеров Г.Ф., Кузнецов М.В.). 15.
Результаты
клинико-морфологических исследований биоматериала Аллоплант для создания
опорно-двигательной культи при анофтальме // 7-я научно-практическая
конференция Екатеринбургского Центра МНТК «Микрохирургия глаза», -
Екатеринбург, 1999. -С. 86-87. (Соавт.: Нигматуллин Р.Т., Искандеров Г.Ф.,
Рыжов В.А.). 16.
Структурные
и биомеханические особенности фасциальных узлов области глазницы // Шестая
научно-практическая конференция по вопросам хирургического лечения заболеваний
органа зрения. – Екатеринбург, 1998. –С. 97-98. (Соавт.: Нигматуллин Р.Т.,
Мулдашев Э.Р., Салихов А.Ю., Искандеров Г.Ф.). 17.
Возможные
пути оптимизации полимерных глазных протезов // 7-я научно-практическая
конференция Екатеринбургского Центра МНТК «Микрохирургия глаза». -
Екатеринбург, 1999. -С. 113-115. (Соавт.: Рыжов В.А., Салихов А.Ю.). 18.
Особенности
социальной реабилитации больных с анофтальмом престарелого возраста //
Ерошевские чтения.: Труды Всероссийской конференции «Геронтологические аспекты
офтальмологии» и VI Международного семенара по вопросам
пожилых «Самарские лекции», посвященные 100-летию со дня рождения Героя Социалистического
Труда, лауреата Государственной премии СССР, заслуженного деятеля науки РСФСР,
члена-корреспондента АМН СССР, профессора Т.И. Ерошевского / Под редакцией Г.П.
Котельникова. – Самара: «Офорт»; СамГМУ, 2002. -С. 346-348. (Соавт.: Рыжов
В.А., Салихов А.Ю., Нураева А.Б.). 19.
Опыт
применения специальных косметических глазных протезов при заборе донорских глаз
// Шестая научно-практическая конференция по вопросам хирургического лечения
заболеваний органа зрения. – Екатеринбург, 1998. -С. 106-107. (Соавт.: Рыжов
В.А., Чернов Н.В.). 20.
Способ
формирования конъюнктивальной полости при врожденном анофтальме и микрофтальме
// Пластическая хирургия придаточного аппарата глаза и орбиты. – М., 1996. –С.
65-66. (Соавт.: Салихов А.Ю., Булатов Р.Т., Мулдашев Э.Р., Рыжов В.А.,
Деревянных С.А.). |