СОДЕРЖАНИЕ НОМЕРА
ХИРУРГИЯ СЕНИЛЬНОЙ МАКУЛЯРНОЙ ДЕГЕНЕРАЦИИ БИОМАТЕРИАЛАМИ АЛЛОПЛАНТ. Кийко Ю.И.
AGE-RELATED MACULAR DEGENERATION SURGERY WITH ALLOPLANT BIOMATERIALS.
Yu.I. Kiiko
A pathogenetic approach in the combined treatment of the age-related macular degeneration with the use of different Alloplant biomaterials was suggested in the article. The method is based on angiogenesis induction and stimulation of intracellular regeneration processes in the retina. There were developed different methods of the age-related macular degeneration treatment with the use of biomaterials depending on the stage and form of the disease.
ХИРУРГИЧЕСКАЯ РЕАБИЛИТАЦИЯ БОЛЬНЫХ АНОФТАЛЬМОМ НА ОСНОВЕ ПРИМЕНЕНИЯ БИОМАТЕРИАЛОВ АЛЛОПЛАНТ
Кульбаев Н.Д.
читать статью
SURGICAL REHABILITATION OF ANOPHTHALMUS PATIENTS BASED ON THE USE OF ALLOPLANT BIOMATERIALS
N.D. Kulbaev
The author used Alloplant biomaterial for the volumetric defect replacement to form the functional stumps following the enucleation. This biomaterial was used for the delayed implantation of the functioning stump and elimination of the insufficient functional and cosmetic effects after the previous surgeries. There was developed the criteria for quantitative efficacy evaluation of the anophthalmus patient surgical rehabilitation with the use of Alloplant biomaterials.
МОРФОЛОГИЧЕСКОЕ ОБОСНОВАНИЕ ПРИМЕНЕНИЯ СОЕДИНИТЕЛЬНО-ТКАННЫХ ТРАНСПЛАНТАТОВ, МОДЕЛИРОВАННЫХ ЛАЗЕРНЫМ ИЗЛУЧЕНИЕМ Гайнутдинова Р. Д.
читать статью
THE MORPHOLOGICAL SUBSTANTIATION OF THE USE OF THE CONNECTIVE TISSUE TRANSPLANTS MODELED BY LASER RADIATION
R.D. Gainutdinova
It was for the first time that the effect of laser radiation upon the structure of connective tissue transplants had been studied. It was established that the selection of the optimum mode of the connective tissue transplant modeling is possible taking the structure of the fibrous matrix into account. There was developed an optimum mode of laser cutting for transplants of cranial dura matter, derma, serious tunics and capsules of organs, subcutaneous fatty tissue taking the peculiarities of their fibroarchitectonics into consideration.
СТИМУЛЯЦИЯ РЕГЕНЕРАТОРНЫХ ПРОЦЕССОВ В ПОСЛЕОПЕРАЦИОННОЙ РАНЕ С ИСПОЛЬЗОВАНИЕМ АЛЛОГЕННОГО БИОМАТЕРИАЛА И ЭНЕРГИИ ЛАЗЕРНОГО ЛУЧА
Пантелеев В.С.
читать статью
THE STIMULATION OF REGENERATIVE PROCESSES IN THE POSTOPERATION WOUND WITH THE USE OF ALLOGENEIC BIOMATERIAL AND LASER BEAM ENERGY
V.S. Panteleev
The allogeneic biomaterial was first used with the purpose to correct morphogenesis in the process of healing the wounds. There were studied the morphology of the wound process as well as the microcirculation condition and saturation of tissues by oxygen in the zone of the wound changes in case of the combined use of the allogeneic biomaterial and laser radiation energy. The method of the allogeneic biomaterial insertion into the tissues of the wound has been developed. There was also developed the laser polishing method of keloid and hypertrophic scars with further correction of wound healing using the allogeneic biomaterial.
КОМПЛЕКСНОЕ ЛЕЧЕНИЕ ТРОФИЧЕСКИХ ЯЗВ НИЖНИХ КОНЕЧНОСТЕЙ С ИСПОЛЬЗОВАНИЕМ СТИМУЛЯТОРА РЕГЕНЕРАЦИИ АЛЛОПЛАНТ И ЭНЕРГИИ ЛАЗЕРНОГО ИЗЛУЧЕНИЯ
Соколов В. П.
читать статью
THE COMPLEX TREATMENT OF LOWER EXTREMITY TROPHIC ULCERS WITH THE USE OF ALLOPLANT REGENERATION STIMULATOR AND LASER RADIATION ENERGY
V.P. Sokolov
Based on the carried out investigations there was proved the efficacy of Alloplant regeneration stimulator use in the treatment of lower extremity trophic ulcers. It is revealed that Alloplant regeneration stimulator has a stimulating effect on the reparative processes in the trophic ulcers. There was developed a method of Alloplant regeneration stimulator insertion into the tissues of the trophic ulcer region. It was for the first time proved based on the histological and cytological methods of the investigation that the use of Alloplant regeneration stimulator and laser radiation energy is most effective when treating lower extremity trophic ulcers.
ПРИМЕНЕНИЕ БИОСТИМУЛЯТОРА РЕГЕНЕРАЦИИ АЛЛОПЛАНТ ПРИ ЭКСПЛАНТАЦИОННОЙ ГЕРНИОПЛАСТИКЕ
Шавалеев Р. Р.
читать статью
THE USE OF ALLOPLANT REGENERATION STIMULATOR IN EXPLANTATIONAL HERNIOPLASTY
R.R. Shavaleev
The author put forward the solution of the problem relating to the surgical treatment of patients suffering from the defects of the abdominal wall by means of modulation of the local regenerative processes directly in the hernioplasty region aimed at the formation of the functionally adequate connective tissue structures. There was developed a method of the explantational hernioplasty with the use of Alloplant biomaterial (Patent №2365344 dated 29.05.2008, The Russian Federation). Experimentally there was studied the dynamics of the morphological changes in the hernioplasty region with the use of the dispersed Alloplant biomaterial. In clinical practice we perfected the method of the noninjection use of the regeneration process regulator (Alloplant dispersed biomaterial) as well as its fixation by the medical glue “Sulphacrilat” in the zone of the explant use in hernioplasty.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ НЕДОСТАТОЧНОСТИ ЗАМЫКАТЕЛЬНОГО АППАРАТА ПРЯМОЙ КИШКИ С ПРИМЕНЕНИЕМ БИОМАТЕРИАЛОВ АЛЛОПЛАНТ
Булгаков А. В., Мулдашев Э.Р.
читать статью
SURGICAL TREATMENT OF THE RECTUM CLOSURE APPARATUS (RCA) WITH THE USE OF ALLOPLANT BIOMATERIALS
A.V. Bulgakov, E.R. Muldashev
There was developed a new method of the anterior levatoroplasty accompanied by the formation of the perineum tendinous centre. The procedure is called “The surgical treatment method of the perineum postnatal traumata consequences”. Alloplant biomaterials were first used in procto-plasty to restore anatomical structures of RCA. There was proved the necessity of Alloplant biomaterial individual selection to restore RCA depending on the volume, location and character of the injury. A reliable engraftment was proved.
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ЭХИНОКОККОЗА ЛЕГКИХ У ДЕТЕЙ
Гумеров М. И.
читать статью
SURGICAL TREATMENT OF LUNG ECHINOCOCCOSIS IN CHILDREN
M.I. Gumerov
The author developed the method of carrying out thorax echography in children suffering from lung echinococcosis. The Echographic semiotics as well as echographic picture peculiarities of echinococcosis cysts in lungs depending on the parasite development stage and character of complications were described. The necessity and duration of the preoperative preparation and postoperative management in case of lung echinococcosis was scientifically proved. The method of videotorascopic echinococcectomy with noncomplicated lung echinococcosis was developed in children and implemented into practice.
ПУТИ ПРЕДУПРЕЖДЕНИЯ ФОРМИРОВАНИЯ РУБЦОВЫХ СТРИКТУР ВНЕПЕЧЕНОЧНЫХ ЖЕЛЧНЫХ ПРОТОКОВ И МЕТОДЫ ИХ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ
(Экспериментально - морфологическое и клиническое исследование)
Палтусов А. И.
читать статью
WAYS TO PREVENT CICATRICAL EXTRAHEPATIC BILIARY STRICTURE FORMATION AND METHODS OF THEIR SURGICAL CORRECTION (Experimental-morphological and clinical investigation)
A.I. Paltusov
The article presents the development and anatomical justification of the membranous biomaterial for hermiticity and restoration of the biliary-enteric anastomosis anatomical integrity. Based on the carried out clinical studies there was substantiated a possibility for the prevention and treatment of cicatrical biliary strictures with the use of allogenic membranous biomaterial.
ОПЕРАЦИЯ ЛЕЧЕБНОГО РЕТРОСКЛЕРО-ПЛОМБИРОВАНИЯ ДИСПЕРГИРОВАННЫМ БИОМАТЕРИАЛОМ АЛЛОПЛАНТ В ЛЕЧЕНИИ ДИАБЕТИЧЕСКОЙ РЕТИНОПАТИИ
Султанов Р.З.
читать статью
THERAPEUTIC RETROSCLEROFILLING SURGERY BY DISPERSED ALLOPLANT BIOMATERIAL IN DIABETIC RETINOPATHY TREATMENT
R.Z. Sultanov
Experimental and morphological methods proved that therapeutic retrosclerofilling surgery with the use of the dispersed alloplant biomaterial promote the resorption of intraocular hemorrhages and normalization of histologic state of retina. This surgery was used in the treatment of diabetic retinopathy and there were determined indications for its usage in patients suffering from diabetic retinopathy with edematous-hemorrhagic syndrome
СЛУЧАЙ
ИЗ КЛИНИЧЕСКОЙ ПРАКТИКИ
СЛУЧАЙ УСПЕШНОГО ПРИМЕНЕНИЯ МЕТОДА ФАРМАКОПУНКТУРЫ БИОМАТЕРИАЛА АЛЛОПЛАНТ В КОМПЛЕКСНОМ ЛЕЧЕНИИ АХОНДРОПЛАЗИИ
Валиева Н. И
читать статью
The clinical example shows the principal possibility of pharmacopuncture with the Alloplant biomaterials in the complex treatment of patients with achondroplasia.
-реклама-
Публикации 2012г.
Хирургия сенильной макулярной дегенерации биоматериалами Аллоплант
Кийко Ю.И.
Московский филиал ФГБУ "Всероссийский Центр глазной и пластической хирургии"
(по материалам монографии Ю.И. Кийко Сенильная макулярная дегенерация. Регенеративная хирургия биоматериалами Аллоплант Уфа-Москва 2002)
В статье предложен и обоснован патогенетический подход в комплексоном лечении сенильной макулодегенерации с использованием различных биоматериалов Аллоплант, основанный на индукции ангиогенеза и стимуляции процессов внутриклеточной регенерации в сетчатке. Разработаны различные способы хирургического лечения сенильной макулодегенерации с помощью биоматериалов Аллоплант в зависимости от стадии и формы заболевания. Определена этапность повторных оперативных вмешательств с учетом стадии и формы заболевания.
Актуальность
Сенильная макулодегенерация считается самым распространенным заболеванием у лиц старше 65 лет и является причиной потери центрального зрения. Число больных с сенильной макулодегенерацией достигают 76,5% обратившихся к окулисту (Назратенко Г.Б., 2000), причем 70% из них имеют слепоту или зрение ниже 0,1 (Мухина М.А. с соавт., 2000). По данным Macular Photocoagulation study group (1993) ежегодное увеличение больных с сенильной макулодегенерацией достигло 6% В анализе заболеваемости России сенильная макулодегенерация составляет 11,35 ± 2,2 человека на 1000 взрослого населения (Смолякова Г.Н., 1987, 1988). В связи с тем, что происходит быстрый количественный рост больных, а так же двусторонний характер заболевания и необратимая потеря зрения при сенильной макулодегенерации, Всемирная организация здравоохранения (1994) ставит одной из приоритетных задач разработку более совершенных методов лечения этого заболевания среди медико-социальных проблем мирового здравоохранения.
Большинство исследователей считают, что основной причиной развития сенильной макулодегенерации является нарушение гемодинамики в капиллярах хориоидеи. В связи с тем, что 80-90% циркулирующей крови в глазу сосредоточено в хориоидее (Бунин А.Я., 1971; Day J. С соавт., 1971; Alm A., Bill A.1973), основные методы лечения (консервативные, лазерные, альтернативные, хирургические) направлены на улучшение кровообращения в ней. Восстановление кровообращения в хориоидее может предотвратить развитие сенильной макулодегенерации и даже обеспечить обратимость патологического процесса.
Поэтому понятен интерес многих авторов, разрабатывающих операции реваскуляризации хориоидеи, в том числе с применением различных биоматериалов (Волошинов Д.Б., 1968,1971; Базарный В.Ф., 1969, 1973; Шпак Н.Н., 1976; Смеловский А.С., 1982; Водовозов А.М. с соавт., 1992; Корепанов А.В. с соавт. 1996, 1997, 1999 и др.). В то же время, несмотря на положительные клинические результаты, получаемые авторами при этих операциях, они не получили полного клинического признания и не оказали значительного влияния на снижение количества слепых от сенильной макулодегенерации (Chong N.H.V., Bird A.C., 1998).
Дискуссионным моментом остаются вопросы стабильности получаемых результатов и биологические процессы, происходящие на месте проведения реваскуляризующей операции и имплантируемого материала. Подробно и аргументированно представлены результаты исследований о влиянии используемых материалов на функциональный эффект реваскуляризирующих операций и на стабильность получаемых результатов в монографии Муслимова С.А. (2000). Автор отметил, что стабильность вновь образованного сосудистого русла в хориоидее при реваскуляризирующих операциях зависит от возможности предупреждения имплантируемых материалов рубцовой трансформации. И только при ее отсутствии новая сосудистая сеть становится тем трофическим компонентом, который улучшает метаболизм сетчатки и приостанавливает процесс ее дегенерации. А использованием возможностей влияния трансплантатов на стимуляцию фибробластических факторов роста можно вызвать регенеративный процесс ультраструктуры сетчатки.
Во Всероссийском центре глазной и пластической хирургии Минздрава РФ разработана и внедрена в практику здравоохранения серия биоматериалов Аллоплант (Приказ № 901 Министерства здравоохранения СССР от 1987 года). Аллотрансплантаты Аллоплант имеют низкую антигенность, не вызывают рубцевания на месте трансплантации и способствуют селективному росту тканей реципиента. Процесс замещения имплантированного биоматериала сопровождается выделением различных факторов роста и других медиаторов регенерации.
Избирательно регулируя содержание различных гликозаминогликанов в аллотрансплантате, стало возможным управление процессом формирования регенерата (“Биоматериал Аллоплант для регенеративной хирургии” Решение о выдаче Патента от 26 марта 2002 г. по заявке № 200 11272 96 ). В Центре уже более 25 лет разрабатывается хирургическое направление, основанное на стимуляции селективной регенерации различных тканей биоматериалом Аллоплант (Мулдашев Э.Р. с соавт., 1988, 1994; Muldashev E.R. et al., 1999; Муслимов С.А., 2000). В частности, Аллоплант для реваскуляризации хориоидеи, Аллопланты - стимуляторы васкулогенеза и фагоцитоза, приводят к выраженной активации внутриклеточной регенерации в нейронах и пигментном эпителии с достоверным расширением диапазона их функциональных возможностей. Разработка указанного регенеративно-биологического аспекта в хирургии является весьма перспективным ввиду того, что появляется возможность воздействовать на биохимические процессы и репаративные способности тканей глаза, а также для лечения заболеваний, связанных с нарушением обмена веществ и микроциркуляции тканей. Одним из таких заболеваний является сенильная макулодегенерация, патогенез которой большинство исследователей связывает с возрастными изменениями обмена веществ и микроциркуляции глаза.
Цель исследования
Разработать патогенетически ориентированное хирургическое лечение сенильной макулярной дегенерации с использованием биоматериала Аллоплант и изучить его клиническую эффективность. На первом этапе были проведены экспериментально-морфологические исследования с целью изучить закономерности репаративных процессов при трансплантации биоматериалов Аллоплант и их возможности для восстановления ультраструктуры клеток пигментного эпителия и нейронов сетчатки. Экспериментальные исследования проведены на 24 пигментированных кроликах весом 3-3,5 кг. Субретинальное кровоизлияние (СРК) моделировалось инъекцией 0,1 мл собственной крови (Johnson M. с соавт., 1991). Эта модель является наиболее близкой к патогенезу сенильной макулодегенерации. У 18 кроликов на 7-й день после создания субретинального кровоизлияния в опытной группе производили операцию с внедрением в супрахориоидальное пространство эписклерального лоскута на ножке и аллогенного биоматериала Аллоплант.Контрольную группу составили 6 кроликов. Животных выводили из опыта внутривенным введением фенобарбитала через 7, 14, 30, 60, 120 и 180 дней после операции.
Методы экспериментальных исследований
- микроскопическое исследование с окраской гематоксилином и эозином, импрегнацией нитритом серебра;
-электроннор-микроскопические исследования с окраской uranil acetate, lead citrate.
Результаты исследований
Экспериментально-морфологические исследования на модели субретинального кровоизлияния показали, что в контрольной группе кроликов они были наиболее выражены в наружных слоях сетчатки (особенно в пигментном эпителии сетчатки и фоторецепторных клетках) и мембране Бруха. Эти изменения наблюдались уже на 7-й день после кровоизлияния, а затем нарастали, достигая на 90-е сутки полной деструкции наружной сетчатки и замены нейронов пролиферирующими глиальными клетками.
Обобщая результаты электронно-микроскопического изученияможно заключить, что восстановление ультраструктуры клеток сетчатки после операции происходило в следующей последовательности: клетки пигментного эпителия сетчатки - фоторецепторы - Мюллеровы глиоциты - ассоциативные нейроны. Также восстанавливаются взаимоотношения между фоторецепторами и клетками пигментного эпителия, что означает восстановление процесса фоторецепции и утилизации сброшенных дисков наружных сегментов фоторецепторов. А также обнаруживалась активная и быстрая васкуляризация трансплантата для мембранной пластики с формированием дифференцированного органного сосудистого русла.
Эписклеральный лоскут и аллотрансплантат, введенные в супрахориоидальное пространство, образуют в итоге единую структуру с сохранением сосудов лоскута и неоваскуляризацией аллотрансплантата.
Таким образом, учитывая биологический потенциал биоматериалов Аллоплант по индукции ангиогенеза и стимуляции репаративной регенерации, использование его при разработке патогенетически ориентированного хирургического лечения сенильной макулодегенерации представляется обоснованным.
Материалы и методы клинических исследований
Разработка техники операций с применением биоматериалов Аллоплант Для разработки патогенетического подхода в лечении сенильной макулодегенераци – улучшения хориоретинального кровообращения и нормализации метаболизма хориоидеи и сетчатки, были использованы возможности различных биоматериалов Аллоплант вызывать регенерацию как кровеносных сосудов, так и лимфатических капилляров, образующих единую сеть регенерата и хориоидеи, а также усиливать секрецию различных факторов роста и других медиаторов регенерации в результате активизации мононуклеарных фагоцитов при их резорбции: Аллоплант для реваскуляризации хориоидеи, аутолимфосорбции (мембранный и “спонч”), стимулятор васкулогенеза, и стимулятор фагоцитоза.
В основу разрабатываемой хирургической техники лечения сенильной макулодегенерации биоматериалами Аллоплант была взята операция реваскуляризации хориоидеи с помощью эписклерального сосудистого лоскута, предложенная Галимовой В.У. и Мулдашевым Э.Р. (1980, 1999).
Основные этапы разработанной операции - аутолимфореваскуляризации хориоидеи - заключались в следующем: в нижне-наружном секторе глазного яблока выкраивали эписклеральный лоскут прямоугольной формы и вводили в супрахориоидальное пространство (рис. 1.);
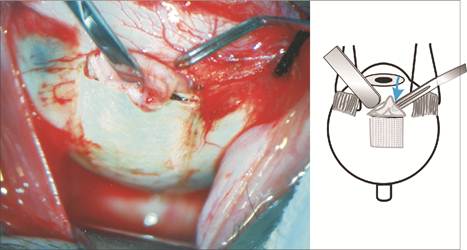
Рис. 1 Введение эписклерального лоскута в супрахороидальное пространство
поверх него вводили и расправляли в супрахориоидальном пространстве Аллоплант для реваскуляризации хориоидеи (рис.2);
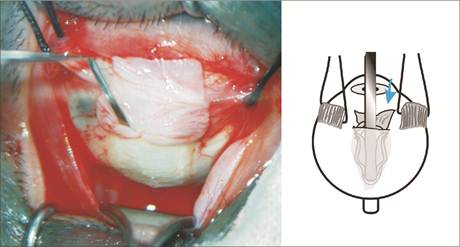
Рис. 2 Аллоплант для реваскуляризации хориоидеи и его введение в супрахориоидальное пространство
над ним дополнительно вводили Аллоплант для аутолимфосорбции (рис. 3);
Рис. 3 Аллоплант для аутолимфосорбции
на склеральный разрез накладывали П-образный шов с фиксацией введенных Аллоплантов. В супрахориоидальное пространство засыпали порошкообразный Аллоплант, после чего ушивали конъюнктиву.
Объем клинических исследований составили 704 больных (1338 глаз), прошедших лечение с 1980 по 2001 год с диагнозом сенильная макулярная дегенерация. В анализ вошли больные без выраженной сопутствующей офтальмологической патологии (высокая осложненная близорукость, развитая и далекозашедшая стадия глаукомы, абиатрофия сетчатки, посттромботические изменения сетчатки, атрофия зрительного нерва) со сроками наблюдения более 8 лет. Офтальмологическое обследование было стандартным и включало: определение остроты зрения без коррекции и с коррекцией по таблице Сивцева, аппланационную тонометрию (при необходимости - электротонографию), исследование глазного дна прямым офтальмоскопом Neitz Instruments (Япония) и трехзеркальной линзой Гольдмана.
В связи с изменениями в диагностической аппаратуре в течение 20 лет для исследования полей зрения использовались полусферический периметр Карл Цейс Йена, автоматический периметр Takagi-85, а также компьютерная периметрия (Humphrey Instr.,model 640, USA) в разные сроки до и после операции с использованием программы 30-2, стимул 4. У части пациентов с различными стадиями сенильной макулодегенерацией были проведены электрофизиологические исследования до операции и в различные сроки после нее.
Исследовались: порог возникновения электрического фосфена, критическая частота слияния электрофосфена и характеристики общей электроретинограммы в условиях световой и темновой адаптации. Для регистрации ЭРГ использовалась электрофизиологическая система «PRIMUS» (Lace Elettronica, Италия). Выборочно проведены флюоресцентая ангиография (Фундус-камера, FK-50, Karl Zeiss), оптическая когерентная томография – ОCТ-2000 фирмы Humphrey (Optical coherent tomography, США). Из 704 больных женщин было 422 (60%), мужчин 282 (40%). Возраст пациентов варьировал от 47 (первичное обследование) до 95 лет (на момент последнего обследования и лечения).
Сочетание сенильной макулодегенерации с другими офтальмологическими заболеваниями имелось в 64% глаз. Результаты клинических исследований. Основываясь на работах Л.А. Кацнельсона, нами была составлена рабочая классификация стадий сенильной макулярной дегенерации.
Первая стадия – зрение 0,5 и выше. На глазном дне просматривается крапчатость, небольшие точечные не сливающиеся друзы, могут быть мелкие кровоизлияния.
Вторая стадия – зрение 0,2-0,4. На глазном дне появляются кровоизлияния, друзы увеличиваются в размере и начинают сливаться.
Третья стадия – зрение 0,1 и ниже. На глазном дне просматриваются неоваскуляризация, экссудативная или геморрагическая отслойка пигментного эпителия или нейроэпителия.
Четвертая стадия – зрение 0,05 и ниже. Выраженные рубцовые изменения на глазном дне. Эффективность различных видов лечения в основном оценивали по результатам остроты центрального зрения, так как поле зрения при сенильной макулярной дегенерации значимо начинает изменяться уже при выраженном падении центрального зрения.
В зависимости от примененного метода лечения все исследуемые глаза были распределены на три группы. Длительность наблюдения одних и тех же глаз больных была не менее 8 лет, что позволяло делать вывод об эффективности методов лечения в зависимости от стадии заболевания.
В I группу были объединены больные, получающие консервативное лечение иногда в сочетании с лазеркоагуляцией, лечение и динамическим наблюдением в течение 8 лет. Всего 658 глаз.
Во II группу были объединены больные, которым проводилось хирургическое лечение по разработанной хирургической технологии Аллоплант и динамическим наблюдением в течение 8 лет. Всего 629 глаз.
В III группу были объединены больные, у которых была диагностирована I стадия сенильной макулодегенерации. Эти больные не согласились на хирургическое лечение при высокой остроте зрения. Чаще всего у них на другом глазу не ещё было проявлений заболевания.
В течение 8 лет им проводилось консервативное лечение. Затем, когда стало снижаться центральное зрение, они были оперированы по технологии Аллоплант и далее наблюдались и лечились по этой технологии в течение 8 лет. Всего 51 глаз. Распределение глаз в зависимости от метода лечения и стадии заболевания представлено на таблице 1.
| Группа | Метод лечения |
Стадия заболевания |
Всего глаз | |||
I |
II |
III |
IV |
|||
1 |
Консервативный |
216 |
185 |
172 |
85 |
658 |
2 |
По технологии Аллоплант |
127 |
241 |
184 |
77 |
629 |
3 |
Комбинированный |
51 |
- |
- |
- |
51 |
Всего |
394 |
425 |
356 |
162 |
1338 |
|
I группа состоит из 658 глаз с различными стадиями сенильной макулярной дегенерацией, которые получали консервативное лечение. Лечение проводилось, как правило, курсами в стационаре один раз в году. Большинству больным проводился дополнительно курс медикаментозного лечения в течение года амбулаторно. Непосредственный эффект повышения остроты зрения соответственно после консервативного лечения, в I и II стадиях наблюдается в 86% и в 70% глаз (с эффективностью до 3 - 8 месяцев.
При последующих госпитализациях и обследованиях уже через 3-4 года эффективность повышения зрения при консервативном лечении была только в 47% и 38% глаз. Соответственно при многолетнем наблюдении выявляется явная тенденция прогрессирования заболевания и снижения зрительных функций. Это четко просматривается на графиках динамики остроты зрения этой группы больных. Динамика остроты зрения 1 группы больных с 1 стадией заболевания в течение 8 лет представлена на рис. 4. 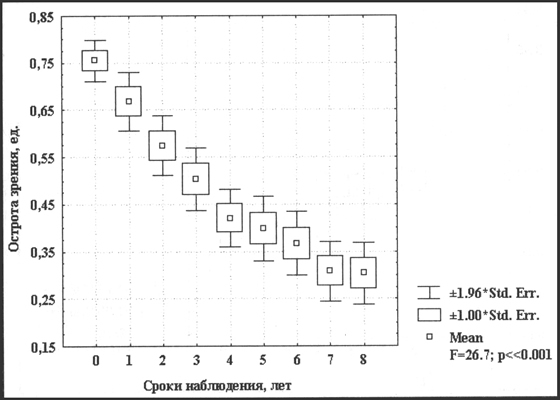
Рис.4 Динамика остроты зрения при консервативном лечении 1 стадии СМД:
по оси абцисс показаны временные срезы наблюдений (0 – первичное наблюдение; 1 – обращение и лечение через один год; 2 – обращение и лечение через два года; 3 – обращение и лечение через три года; 4 – обращение и лечение через четыре года; 5– обращение и лечение через пять лет; 6 – обращение и лечение через 6 лет; 7 – обращение и лечение через 7 лет; 8 – обращение и лечение через 8 лет). По оси ординат обозначена острота зрения
Как видно из представленного рисунка, несмотря на проводимое ежегодное консервативное лечение в течение 8 лет, зрение больных с начальной стадией снижается более чем в 2 раза. При статистической обработке отмечается наиболее значимо влияние фактора времени ( F = 26.7, P << 0.001 ). По клинической картине и визуальным данным большинство глаз этих больных переходят во II стадию заболевания. Средняя острота зрения больных 1 стадии сенильной макулодегенерации при консервативном лечении в течение 8 лет снизилась с 0,76 до 0,32.
Динамика остроты зрения 1 группы больных со II стадией заболевания в течение 8 лет представлена на рис. 5.
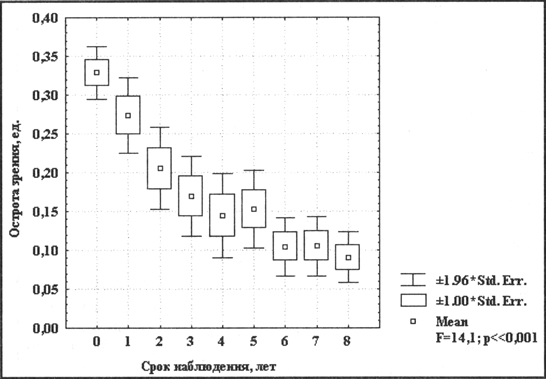
Рис 5 Динамика остроты зрения при консерватив ном лечении II стадии СМД
В этой группе больных также отмечается влияние фактора времени ( F = 14.1, P << 0.001 ) на значительное снижение зрения. И несмотря на проводимое лечение средняя величина остроты зрения постоянно снижается. И за 8 лет наблюдений она снизилась с 0,33 до 0,09. Как и при начальной стадии сенильной макулодегенерации наиболее быстрое падение зрения происходит в первые 4 года. Это косвенно подтверждает результаты других исследователей, что 5- летний цикл наблюдений позволяет судить об эффективности предложенного метода лечения.
Больные со II стадией заболевания за 8 лет теряют зрение в 3,5 раза и в 95% случаев переходят в III стадию и относятся уже к группе слабовидящих.
Динамика остроты зрения 1 группы больных с III стадией заболевания в течение 8 лет представлена на рис. 6. При этой стадии заболевания также значимо влияние фактора времени (F = 5.9, P << 0.001) на снижение остроты зрения.
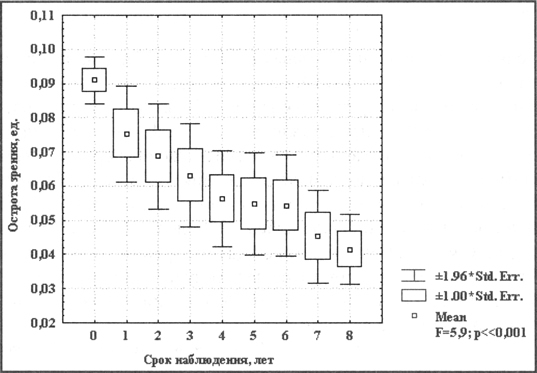
Рис 6 Динамика остроты зрения при консервативном лечении III стадии СМД
Хотя уровень снижения его несколько ниже, но всё же основная часть больных переходит в IV, рубцовую стадию заболевания в течение 8 лет. Средняя острота центрального зрения снижается с 0.09 до 0.04. Динамика остроты зрения при консервативном лечении IV стадии заболевания показана на рис. 7. Изменения остроты зрения в целом незначимо (F = 1.7, P > 0.1). Оно колеблется в пределах 0.025 – 0.035 , т.е. счета пальцев на расстоянии 1 – 1,5 м. При комплексном обследовании у этих больных в основном изменяется центральное поле зрения.
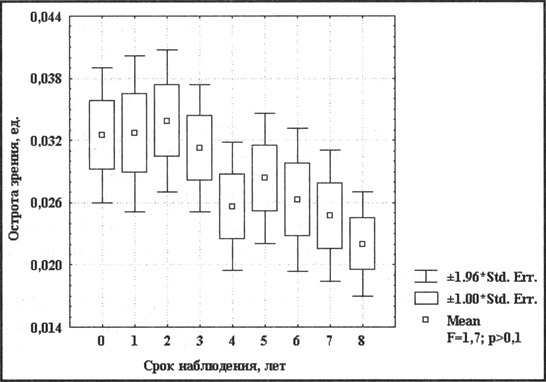
Рис 7 Динамика остроты зрения при консервативном лечении IV стадии СМД
Анализируя наблюдения за одними и теми же больными 1 группы с сенильной макулодегенерацией в течение 8 лет, регулярно проводящих консервативное лечение, приходится констатировать, что большинство из них становятся практически слепыми.
Клинические наблюдения за результатами лечения разработанной и предлагаемой нами хирургии сенильной макулодегенерации биоматериалом Аллоплант объединены и представлены во II группе из 629 глаз. Наблюдения за этими больными проводились в течение 8 лет. Изучение предлагаемой технологии регенеративной хирургии биоматериалами Аллоплант проводилось при различных стадиях сенильной макулодегенерации и представлено во II группе больных. Всего им было проведено 1894 операции за эти годы.
Динамика остроты зрения II группы больных с 1 стадией заболевания представлена на рис. 8.
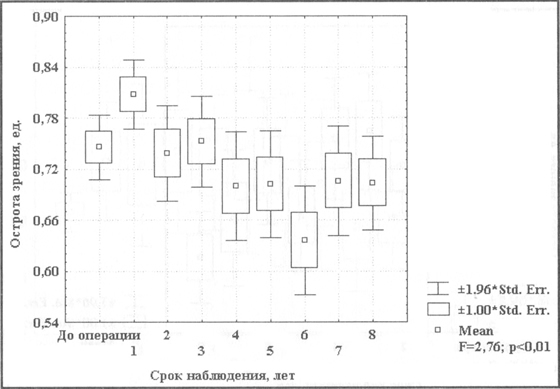
Рис 8 Динамика остроты зрения при лечении по технологии «Аллоплант» 1 стадии СМД
Как видно из рисунка, оперативное вмешательство при 1 стадии сенильной макулодегенерации повышает остроту зрения в среднем с 0,75 до 0,81 и позволяет стабилизировать заболевание и зрительные функции у 95% больных в течение 8 лет. Повышение центрального зрения после операции в течение года имеет статистически значимое различие.
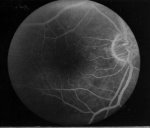
Повышение остроты зрения в послеоперационном периоде наблюдается у 68% оперированных и у 32% - зрительные функции не изменяются. Ухудшение остроты зрения не было отмечено ни в одном случае. Ангиографические исследования, проводимые при начальной стадии заболевания, подтверждают стабилизацию процесса изменений сосудов хориоидеи и сетчатки (рис. 9, 10).
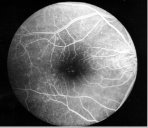 |
 |
 |
| а | б | в |
Рис 9 ФАГД до лечения, 1 стадия СМД. «Сухая» форма. Ранняя венозная фаза. Крапчатость в макулярной области и по периферии сетчатки обусловлена светлыми очагами друз (а). Через два года после начала лечения. Начало венозной фазы. Гиперфлюоресценция друз наблюдается в основном парамакулярной области, со стороны диска зрительного нерва. Макула флюоресцирует слабо (б). Через 6 лет – начало венозной фазы; количество друз сохраняется на минимальном уровне (стабилизация процесса). Макулярная зона не флюоресцирует (в)
 |
 |
 |
| а | б | в |
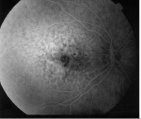
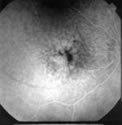
Рис 10 ФАГД до лечения, 1 стадия СМД. Начало веноз ной фазы. Гипо-гиперфлюоресценция центральной зоны сетчатки с окончатыми дефектами пигментного эпи телия в парамакулярной зоне (а). Через год после начала лечения. Начало венозной фазы, картина флюоресценции и площадь очага без видимых изменений, процесс стаби лизировался (б). Через пять лет. Начало венозной фазы. О стабилизации процесса говорит сохранность площади флюоресценции
При анализе результатов лечения по технологии Аллоплант больных со II стадией сенильной макулодегенерации обращает на себя внимание то, что оперативное вмешательство дает более значительный подъем остроты зрения (с 0,28 до 0,38), чем при оперативном лечении больных с I стадией заболевания. (рис.11.).
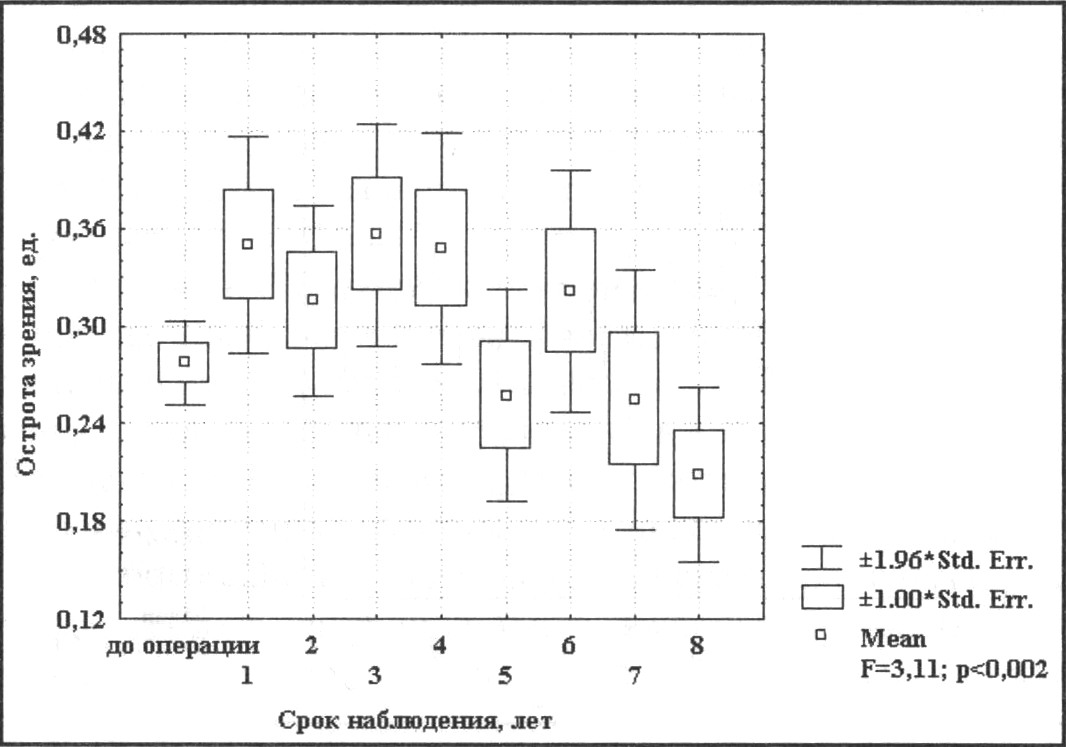
Рис 11 Динамика остроты зрения II стадии СМД при лечении по технологии Аллоплант
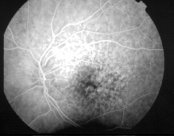
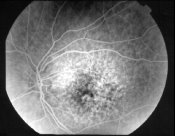
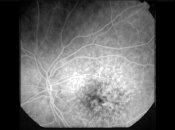
В течение года острота зрения несколько снижается, и остается на уровне 0,35, что выше исходного на 25%. Подъем остроты зрения сразу в послеоперационном периоде объясняется уменьшением отека сетчатки, рассасыванием кровоизлияний или частичного гемофтальма. Это хорошо подтверждается ангиографическими исследованиями (рис. 12) и результатами оптической когерентной томографии макулярной области (рис. 13, 14).
 |
 |
 |
| а | б | в |
Рис 12 ФАГД до лечения, СМД II стадия. Венозная фаза. Крапчатость макулярной зоны обусловлена светлыми точками друз и темными глыбками пигмента (а). Через три года после начала лечения по технологии «Аллоплант». Венозная фаза. Площадь поражения не зменилась, что характеризует стабильность процесса (б). Через пять лет. Площадь гипо- и гиперфлюоресценции не изменилась. Процесс стабильный (в)
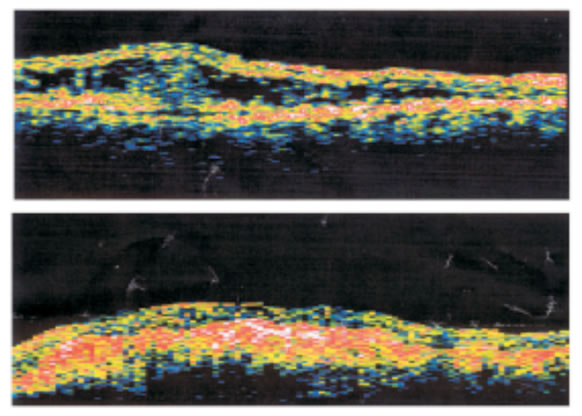
Рис 13 Оптическая когерентная томография макулярной области при СМД II стадии до лечения/ Видно
отслоение нейроэпителия сетчатки и его значительное
отстояние за сет субретинальной серозной жидкости.
Частичное разрушение пигментного эпителия сетчатки.
Visus 0.3 (вверху). Через два года лечения. Остается незначительное отслоение нейроэпителия сетчатки. Субрети
нальная жидкость рассосалась. Пигментный эпителий в
значительной степени восстановился. Visus 0.6 (внизу)
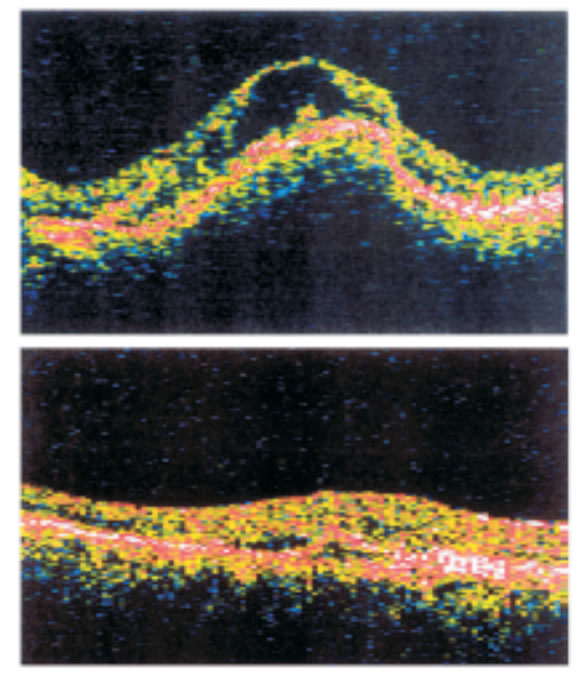
Рис 14 Вертикальная оптическая когерентная томография макулярной области при СМД II стадии до лечения. Высокое отстояние ретинального пигментного эпителия в виде высокого купола и значительное о слоение нейросенсорной сетчатки в виде одной кисты с распространением серозной жидкости вдоль нейроэпителия. Visus 0.2 (вверху). Через полтора года лечения. Серозная жидкость рассосалась, осталась незначительная киста, отслаивающая ретинальный пигментный эпителий. Отслоение нейросенсорной сетчатки в виде двух маленьких кист. Visus 0.4 (внизу)
Повышение остроты зрения в послеоперационном периоде отмечается у 63% больных и в 37% - не изменяется. Ухудшения зрительных функций после оперативного вмешательства в этой стадии сенильной макулодегенерации также не было отмечено.
Исследования в течение 8 лет показали, что влияние фактора времени статистически не значимо (F=3.11; p<0.002). Наблюдения за больными в течение 8 лет показали, что разработанная технология Аллоплант стабилизирует заболевание во II стадии сенильной макулодегенерации у 85% больных, не давая развития неоваскулярному синдрому. У 15% зрение продолжает снижаться. Но темпы падения зрения остаются более медленными при сравнении с больными, получавшими только консервативное лечение.
Динамика остроты зрения во II группе больных с III стадией заболевания в течение 8 лет представлена на рис. 15.
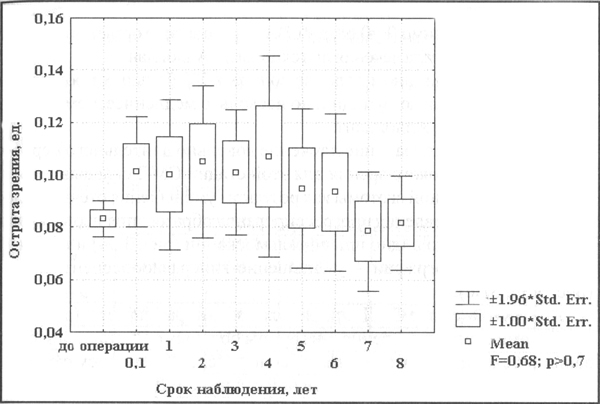
Рис 15 Динамика остроты зрения III стадии СМД при лечении по технологии «Аллоплант»
Выраженные экссудативно-геморрагические проявления на глазном дне и особенно наличие неоваскулярной мембраны говорят всем офтальмологам, что заболевание переходит в терминальную стадию. Используемые методы лечения в этот период (лазеркоагуляция, ретинотомия, удаление неоваскулярных мембран, телетерапия и другие) по данным большинства исследователей считаются малоэффективными. Даже при успешном хирургическом или другом виде лечения в течение 6-18 месяцев более чем у половины больных возникают рецидивы, и заболевание прогрессирует (Amato R.J, Adamis A.P., 1995).
Лечение этой стадии сенильной макулодегенерации по технологии Аллоплант повышает зрительные функции у 57% больных и позволяет у 77% больных сохранить начальное более высокое остаточное зрение в пределах 0,08-0,09 в течение 8 лет.
Учитывая, что при лечении этой стадии заболевания по технологии Аллоплант каждый глаз был оперирован в среднем 3,5раза, мы имеем разнообразие ответов зрительной системы. Это заметно по резкому увеличению индивидуальных дисперсий остроты зрения. В то же время общее влияние незначимо (F=0.68; p>0.7). Острота зрения остается на том же уровне, что и до начала лечения по технологии Аллоплант.
В послеоперационном периоде только у 7% больных продолжали снижаться зрительные функции, но несколько медленнее, чем до лечения по технологии Аллоплант. Повышение и сохранение в течение довольно длительного периода относительно высокого зрения для этой стадии сенильной макулодегенерации складывается из регресса центральной скотомы как результат уменьшения отечного синдрома и приостановления прогрессирования образования неоваскулярной мембраны.
Это видно при флюоресцентной ангиографии - рис. 16, 17, (уменьшение гиперфлюоресцентных зон).
 |
 |
| а | б |
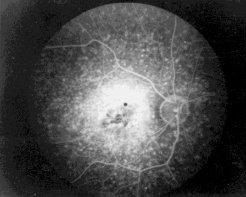
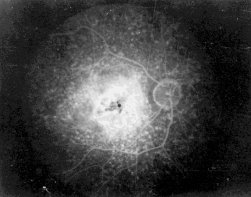
Рис 16 ФАГД до лечения, СМД III стадия. Венозная фаза. Очаг гипо- гиперфлюоресценции в центральной зоне сетчатки. Гиперфлюоресценция фиброваскулярной мембраны с четкими контурами (а). Через 4 года после начала лечения. Венозная фаза. Размер очага прежний. Гиперфлюоресценция на том же уровне. Стабилизация процесса (б)
 |
 |
| а | б |
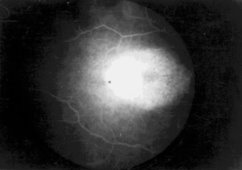
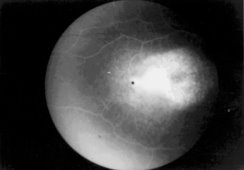
Рис 17 ФАГД до лечения, СМД III стадия. Поздняя
фаза. Гиперфлюоресценция субретинальной мембраны в
макулярной области (а). Через 3 года после начала лечения. Поздняя фаза. Зона гиперфлюоресценции сосудов
субретинальной мембраны уменьшилась (б)
Динамика остроты зрения II группы больных с IV стадией заболевания в течение 8 лет представлена на рис. 18.
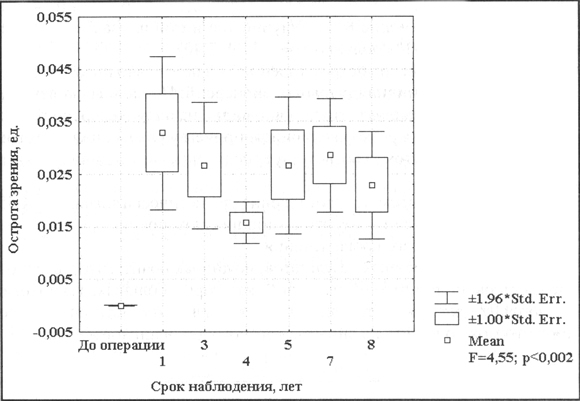
Рис 18 Динамика остроты зрения IV стадии СМД при лечении по технологии Аллоплант
На рисунке также видно, что при лечении терминальной стадии сенильной макулодегенерации по технологии Аллоплант значительно повысить остроту зрения невозможно. Больные остаются в категории практически слепых. В то же время у 43% острота зрения повышалась в 2 раза. Это имеет особенно большое значение в том случае, когда у больных это единственный видящий глаз. У больных этой группы было проведено в среднем по 4 операции на глазу в течение 8 лет. Ухудшения зрительных функций не было. Улучшение и стабилизация процесса отмечены у 91% больных. До операции уровень остроты зрения был предельно низок, что видно по отсутствию индивидуальных дисперсий. После начала лечения по технологии Аллоплант, что хорошо видно на рисунке , средний уровень остроты зрения резко увеличился, причем, у разных пациентов на разную величину (этому соответствует появление межиндивидуальных дисперсий). Отмеченный подъем остроты зрения статистически значим.
Результаты электрофизиологических исследований
В исследовании принимали участие 25 пациентов в возрасте от 55 до 82 лет, пролеченных по технологии Аллоплант. Для контроля исследовались пациенты, получающие консервативное лечение.
Результаты измерения порога электрической чувствительности и критической частоты слияния фосфена показывают относительную стабильность этих психофизиологических характеристик зрительной системы в процессе всех измерений. Несколько иная картина возникает при анализе ретинографических данных. Несмотря на статистически недостоверные различия между результатами в различные сроки, можно отметить некоторые интересные тенденции. Учитывая, что макулярная область содержит всего около 1,5-2% всей популяции колбочек, при регистрации общей ЭРГ мы получаем ответ, определяемый состоянием нейрональных и глиальных элементов сетчатки в целом. Таким образом, задачей исследования являлось рассмотрение электрической активности сетчатки в целом, а также ее общая реакция на различные виды воздействий. По исходным данным выделяется группа сенильной макулодегенерацией III стадии. Вероятнее всего, это объясняется вовлечением в патологический процесс не только центральной части сетчатки, но и периферических ее отделов. Данные ЭФИ в остальных группах лежат на границе нормативных значений.
Динамика изменения показателей электрофизиологического исследования в различных группах больных была следующая. Можно было отметить определенное сходство в динамике больных 1 и 2 стадий заболевания. Максимальное значение амплитуды различных видов ЭРГ у них фиксируется через 6-12 месяцев после операции. Учитывая, что в эти сроки имеется положительная динамика и остроты зрения, можно говорить об общем стимулирующем воздействии Аллопланта на сетчатку и соответственно вызывающем улучшение метаболитических функций сетчатки в целом, включая и макулярную область. Из литературных источников, известно, что амплитуда b-волны уменьшается с возрастом (Weleber R.G; Peterson H.; Zeidler I.).
Наши результаты согласуются с этими данными, хотя можно отметить, что сроки и градиент подобного падения в значительной степени зависят не только от абсолютного возраста пациента, но и от состояния его организма в целом и сетчатки в частности. Результаты клинических исследований при наблюдении за больными в течение 16 лет.
Клинические результаты
Оценить результаты лечения сенильной макулодегенерации всегда сложно. Для анализа отдаленных результатов регенеративного хирургического лечения сенильной макулодегенерации с применением биоматериала Аллоплант мы также представляем репрезентативную группу пациентов, которые наблюдались и проходили ежегодное лечение у нас в клинике в течение 16 лет. Этих больных мы объединили в III комбинированную группу, включающую 89 глаз, они начали лечение при начальной стадии сенильной макулодегенерации. Среднее значение остроты зрения составило 0,67. Из них 51 глаз после 8-летнего ежегодного консервативного лечения был прооперирован по технологии Аллоплант и далее в течение 8 лет больные лечились по этой технологии (хирургическая группа Аллоплант). Другая часть репрезентативной группы (38 глаз – консервативная группа) продолжала наблюдаться в течение следующих 8 лет, получая ежегодное консервативное лечение. Острота зрения со статистическим анализом one-way ANOVA и post-hoc сравнительной характеристикой с использованием теста LSD представлена на рис. 19.
.jpg) |
| a |
.jpg) |
| b |
Рис 19 Динамика остроты зрения в 3-й группе
Анализируя показатели остроты зрения репрезентативной группы пациентов (89 глаз), проходивших наблюдение в течение 16 лет, мы пришли к выводу, что консервативное лечение не останавливает процесс дегенерации сетчатки и острота зрения продолжает снижаться. Среднее значение остроты зрения снизилось с 0,67 до 0,31 в течение первых 8 лет из-за прогрессирования заболевания. Динамика снижения остроты зрения пациентов группы при консервативном лечении оставалась аналогичной как в первые 8 лет, так и в последующие 8 лет. Таким образом, хирургическое лечение сенильной макулодегенерации с применением биоматериала Аллоплант позволяет стабилизировать зрительные функции и значительно замедляет прогрессирование заболевания.
Показания и противопоказания
За более чем 25-летнее использование различных видов биоматериалов Аллоплант мы ни разу не наблюдали реакции отторжения или аллергической реакции на материал, поэтому индивидуальных противопоказаний к применению этих биоматериалов нет.
Противопоказания для использования хирургической технологии Аллоплант могут быть только со стороны соматического состояния больного. Эти противопоказания существуют при всех интраокулярных операциях.
Для введения Аллопланта в супрахориоидальное пространство необходимо снижение внутриглазного давления. Это предупреждает выбухание хориоидеи при вскрытии супрахориоидального пространства и возможность ее перфорации.
Для экстраокулярного использования технологии Аллоплант противопоказаний нет, за исключением инфекции в конъюнктивальной полости. В связи с вышесказанным можно заключить, что при установлении диагноза «Сенильная макулодегенерация» больному показано хирургическое лечение по технологии Аллоплант вне зависимости от стадии заболевания.
Схема хирургического лечения
Наблюдения, проведенные за пролеченными больными в течение 20 лет, позволили нам разработать схему хирургического лечения сенильной макулодегенерации биоматериалом Аллоплант. Тип операции и периодичность оперативных вмешательств зависят от стадии заболевания, динамики падения зрительных функций, картины глазного дна.
Если заболевание укладывается в I стадию, то оперативное вмешательство зависит от размеров друз. При мелкодисперсных друзах предлагается экстраокулярная операция с порошкообразным биоматериалом Аллоплант. Дальнейшее лечение зависит от появления отечности сетчатки, увеличения размера друз, их приближения к фовеолярной области. Если эти явления нарастают, больному предлагается интраокулярная операция, чаще – аутолимфореваскуляризация хориоидеи.
При «географической атрофии» пигментного эпителия проводится операция реваскуляризации хориоидеи. Повторные операции проводятся при снижении зрительных функций. Больные предупреждаются о их необходимости.
При I стадии заболевания наибольшее число повторных операций приходится на 3 и 6 год после первичного оперативного вмешательства (т.е. на этот срок процесс стабилизируется).
При II - III стадиях заболевания повторные операции чаще приходится проводить в первые 2 - 3 года, т.е. стабилизация длится более короткий период, после чего период стабилизации зрительных функций увеличивается до 3 - 5лет.
При наличии II стадии сенильной макулодегенерации целесообразно первоначальное проведение интраокулярного вмешательства и в течение первых двух лет показана экстраокулярная операция.
При терминальных стадиях в первые 2 - 3 года нужно провести интраокулярную операцию в другом секторе глазного яблока (нижне-наружном и нижне-внутреннем). Через 6 - 8 месяцев после интраокулярной операции необходимо провести экстраокулярное введение биоматериала Аллоплант. Такой комплекс оперативных вмешательств останавливает прогрессирование заболевания и сохраняет остаточное зрение. Частота операций на один глаз за 8-летний период при I стадии СМД составила 2,1; при II стадии - 2,8 ; при III - 3,5; при IV стадии - 4 (табл. 5). Процент интраокулярных заболеваний при сенильной макулодегенерации возрастает пропорционально тяжести процесса.
Таким образом, лечение сенильной макулодегенерации по технологии Аллоплант позволяет стабилизировать зрительные функции, вне зависимости от стадии болезни.
ЗАКЛЮЧЕНИЕ
Проблема лечения сенильной макулярной дегенерации до сих пор остается нерешенной: серьезных успехов, сопоставимых с клиническими результатами в других разделах офтальмологии (миопия, кератопластика и т.п.), не достигнуто, несмотря на то, что различные вариации клинического течения и патогенез заболевания изучены весьма досконально.
Исследования, проведенные нами на материале, включающем 704 пациента (1338 глаз), которые наблюдались от 8 до 16 лет, показали, что регенеративно-хирургический подход с использованием биоматериалов Аллоплант создают определенную перспективу успешного лечения больных с сенильной макулярной дегенерацией.
Наиболее показательны результаты исследования рандомизированной группы больных (89 глаз), которые начали наблюдаться в начальной I стадии заболевания и далее ежегодно обследовались нами в течение 16 лет. Эти больные в течение первых 8 лет получали консервативное лечение, далее, 51 из них был прооперирован с применением биоматериалов Аллоплант и лечился уже по этой технологии еще 8 лет.
Выяснилось, что в течение первых 8 лет, когда больные получали ежегодное консервативное лечение, средняя острота зрения снизилась с 0,8 до 0,3, т.е. почти в 3 раза. В периоде наблюдения, длившемся 8 лет, когда больные стали лечиться по технологии Аллоплант, средняя острота зрения не снизилась, а наоборот, повысилась с 0,3 до 0,36. При этом в первые 5 лет она держалась на уровне 0,35 - 0,3, но потом имела тенденцию к постепенному снижению, хотя и через 8лет сохранялась в пределах II стадии заболевания и осталась на уровне 0,2. Анализ этой рандомизированной группы показал, что лечение больных с сенильной макулярной дегенерацией по технологии Аллоплант позволяет не только стабилизировать, но и повысить остроту зрения в отдаленные сроки наблюдения.
В сравнении с этим консервативное лечение оказывая позитивное действие, тем не менее, привело к снижению средней остроты зрения за первые 8 лет с 0,8 до 0,3. Представляет интерес судьба больных 38 глаз из 89, которые не были оперированы по технологии Аллоплант и продолжали ежегодно лечиться консервативно в течение последних 8 лет; средняя острота зрения у этих больных неуклонно снижалась и дошла до уровня 0,05.
Итак, судьба 89 глаз, прослеженных в течение 16 лет, показала, что тем больным, которые начали лечение по технологии Аллоплант, удалось сохранить остроту зрения почти на исходном уровне и даже повысить ее в первые пять лет. Консервативная группа больных показала явную тенденцию к прогрессивному падению зрения. Анализ наблюдений больных, поступивших в клинику с начальной стадией сенильной макулярной дегенерации, показал, что при оперативном лечении по технологии Аллоплант (127 глаз) в течение 8 лет средняя острота зрения несколько снизилась с 0,75 до 0,68 (падение статистически недостоверно), и больные остались в I стадии заболевания, в то время как при консервативном лечение (I группа) средняя острота зрения (216 глаз) снизилась за те же 8 лет от 0,76 до 0,32, то есть более чам в два раза, и больные перешли в следующую, II стадию заболевания.
При II стадии сенильной макулярной дегенерации после лечения по технологии Аллоплант (241 глаз) за 8 лет острота зрения изменилась с 0,28 до 0,19, а в группе с консервативным лечением (185 глаз) средняя острота зрения снизилась с 0,33 до 0,09.
У больных III стадии сенильной макулярной дегенерации (184 глаза) после лечения по технологии Аллоплант в течение 8 лет средняя острота зрения сохранялась почти на прежнем уровне (0,08 и 0,09), а в группе с консервативным лечением (172 глаза) она снизилась с 0,09 до 0,04.
В терминальной IV стадии заболевания (77 глаз) после лечения по технологии Аллоплант в течение 8 лет наблюдалось повышение остроты зрения с 0,022 до 0,046, что очень важно для больных с остаточным зрением. В группе с консервативным лечением (85 глаз) отмечался уровень остроты зрения, близкий к исходному (0,03 и 0,02), т.е. почти в два раза ниже, чем у пролеченных по технологии Аллоплант.
Достоверность вышеприведенных результатов подтверждена данными статистической обработки (кластерный анализ по программе ANOVA). Что касается анализа полей зрения, то строгих статистически достоверных данных получить не удалось ввиду неоднородности данных, полученных при использовании разных в силу их постоянного усовершенствования измерительных приборов в течение 16 лет.
Положительное влияние операции по технологии Аллоплант на функционирование сетчатки было также зафиксировано такими методами, как флюоресцентная ангиография, фотосъемка глазного дна, оптическая когерентная томография, и данными электрофизиологических исследований.
Таким образом, сравнительный анализ отдаленных результатов операций, произведенных по технологии Аллоплант при сенильной макулярной дегенерации, позволил нам прийти к заключению, что хирургическое вмешательство с использованием биоматериалов Аллоплант позволяет стабилизировать зрительные функции, а в ряде случаев даже несколько повысить их.
Надо отметить, что одной операции с комбинированным использованием аллоплантов для реваскуляризации хориоидеи, аутолимфосорбции и стимулятора фагоцитоза недостаточно для полного удержания зрительных функций от прогрессивного снижения: необходимо через те или иные промежутки времени проводить дополнительные операции,– чаще экстраокулярное введение суспензии порошкообразного Аллопланта, стимулятора фагоцитоза. Так, при регенеративно-хирургическом лечении больных с I стадией сенильной макулярной дегенерацией за 8 лет было произведено в среднем на одном глазу - 2,1 операции, при II стадии –2,8, III – 3,5 и IY стадии – 4,0. Естественен вопрос: «Через какие промежутки времени производить дополнительные оперативные вмешательства по технологии Аллоплант.
Основываясь на результатах многолетних наблюдений, мы считаем, что нужно ориентироваться по признаку снижения остроты зрения: как только больной начинает ощущать снижение остроты зрения (обусловленное именно прогрессированием сенильной макулодегенерации), то целесообразно выполнить операцию. Чаще всего достаточно экстраокулярного введения биоматериала Аллоплант. Особенно это характерно для начальных стадий сенильной макулодегенерации. Более гарантированную стабилизацию зрения можно обеспечить, проводя вышеуказанное малотравматичное вмешательство каждые 1-2 года. При более выраженных изменениях проводится интраокулярная операция в другом секторе глазного яблока.Повторное интраокулярное вмешательство (реваскуляризация или аутолимфосорбция) в том же секторе может повторяться через 2 – 2.5 года.
Таким образом, клинические результаты проведенного нами комплекса исследований по лечению сенильной макулярной дегенерации позволяют заключить, что регенеративно-хирургический подход является эффективным и перспективным в лечении этого тяжелого заболевания.
Чем же обусловлена эффективность предлагаемого нами регенеративно-хирургического подхода? Во-первых, необходимо принять во внимание патогенез сенильной макулярной дегенерации, в котором можно выделить несколько основных взаимосвязанных звеньев: снижение плотности хориокапилляров (Ramrattan RS, с соавт., 1994), биохимические нарушения (Tate D.J. с соавт., 1993), деструкция мембраны Бруха и пигментного эпителия сетчатки с врастанием хориокапилляров через мембрану и субретинальной неоваскуляризации (Van der Schaft T.L. с соавт., 1993; Bressler N.M. с соавт., 1994; Dastheib K., Green W.R., 1994), образование друз (Holz F.G. с соавт.,1994) и дегенерация фоторецепторов (Curcio C.A., 1996). Большинство авторов, занимающихся лечением сенильной макулярной дегенерации (Бранчевская С.Я., 1972; Гольцева С.В., 1984; Шульпина Н.Б. с соавт., 1985; Wetzig P.C., 1988; Cha Kravarthy V.G., 1993; Bynoe L.A. с соавт., 1994; Algvere P.V. с соавт., 1997; Husain D., Miller J.W., 1997; del Cerro M. с соавт., 1997), признают, что эффективность тех или иных методов лечения весьма относительна, даже если воздействию подвергаются несколько патогенетических звеньев сенильной макулярной дегенерации.
По-видимому, влияние только на какой-то вид обмена не может обеспечить лечебный эффект, так как дегенерация фоторецепторных нейронов – это конечная фаза сложного патологического процесса, имеющая стереотипный характер (Рапис Е. Г., Грацианская Е. А., 1978; Зуева М. В., Иванина Т.А, 1980; Иванина Т. А. И с соавт., 1983), ключевые факторы которого, однако, до конца не выяснены.
Клинически и экспериментально установлено, что многие виды патологии сетчатки сопровождаются гемоциркуляторными и морфологическими изменениями в сосудистой оболочке (Еременко А. И., 1974; Шершевская О.И. с соавт., 1974). Не является исключением и возрастная макулярная дегенерация, при которой зафиксированы снижение скорости хориоидального кровотока и увеличение периферического сопротивления сосудов хориоидеи (Friedman E. A. et al., 1995, Ravaliko G. et al., 1996).
Показано, что возрастные дегенеративные изменения затрагивают как хориокапилляры (Ramrattan R. S. et al., 1994; Ravalico G. et al., 1996), так и более крупные сосуды хориоидеи (Spraul C. W. et al., 1999). E. A. Friedman (1997) была даже предложена гемодинамическая модель патогенеза возрастной дегенерации сетчатки.
Сравнительный анализ систем кровоснабжения сетчатки, хориоидеи и зрительного нерва, проведенный С. А. Муслимовым (2000) на основе морфометрического исследования сосудов, позволил обосновать ведущую роль сосудистой оболочки в трофике наружных слоев сетчатки.
Были также выявлены пути компенсации кровоснабжения хориоидеи и оттока крови – транссклеральные анастомозы (Муслимов С.А., Мусина Л.А., 2000). Исходя из этого положения, становится понятным, почему так называемые реваскуляризирующие операции (Agarval L. P., 1963; Базарный В. Ф., 1972; Шлопак Т. В. с соавт.,1976; Шпак Н. И., 1978; Водовозов А. М. и соавт, 1995; Басинский С. Н. с соавт, 1997 и др.), которые по сути создают искусственный транссклеральный анастомоз, действительно улучшают кровоснабжение хориоидеи и, следовательно, - трофику сетчатки.
Однако экспериментальные исследования показали, что эти операции имеют весьма существенный недостаток: ткани, погруженные через склеральный разрез в супрахориоидальное пространство, подвергаются рубцовой трансформации с обратным развитием кровеносных сосудов (Муслимов С. А., 2000). Видимо, этим и объясняется временный эффект реваскуляризирующих операций. Следовательно, для того, чтобы обеспечить более длительный трофический эффект, нужен фактор, стабилизирующий сосудистое русло мобилизованного лоскута. Таким фактором может быть биоматериал Аллоплант, введенный вместе с эписклеральным лоскутом, так как проведенные нами базовые исследования (Muldashev E. R. еt al., 1999) показали, что одним из свойств биоматериалов Аллоплант является эффективное предупреждение развития рубцовой ткани. Кроме того, установлено, что различные виды биоматериалов Аллоплант в зависимости от гистохимического состава могут селективно стимулировать регенерацию различных тканей, включая кровеносные и лимфатические сосуды. Основываясь на результатах этих базовых исследований, для регенеративного лечения сенильной макулярной дегенерации нами предложенычетыре вида биоматериалов Аллоплант. Первый из них, условно названный в лабораторном регламенте Аллоплант для реваскуляризации хориоидеи», предназначен для улучшения кровообращения хориоидеи за счет стимуляции регенерации кровеносных сосудов и стабилизации сосудистого русла эписклерального лоскута. Проведенное нами электронно-микроскопическое исследование показало, что после операции с биоматериалом происходит восстановление нарушенных при экспериментальном моделировании патологического процесса внутриклеточных органелл как в клетках пигментного эпителия, так и в нейронах сетчатки. Второй вид биоматериала, названный в лабораторном регламенте Аллоплант для аутолимфосорбции», предназначен для дренирования супрахориоидального пространства глаза за счет лимфатических и кровеносных сосудов, стимулятором роста которых он и является. Учитывая сорбирующую и очищающую функции лимфатической системы (Куприянов В.В. и соавт., 1983), можно думать, что использованиие этого вида биоматериала способствует улучшению состояния супрахориоидальной жидкости и, как следствие, приводит к активации лизосомальных ферментов и фагоцитарной активности резидентных макрофагов хориоидеи и клеток пигментного эпителия сетчатки, очищающих ретину от друз, геморрагий, экссудата и отека, имеющих место при сенильной макулярной дегенерации (Holz F.C. с соавт., 1984). Третий тип биоматериала Аллоплант, имеющий диспергированную (порошкообразную) форму и названный «Стимулятор фагоцитоза», мы используем путем его введения в виде суспензии в теноново пространство. Как показали экспериментальные исследования, проведенные во Всероссийскомм центре глазной и пластической хирургии МЗ РФ (Надольская С. Н., Муслимов С. А., 1998; Муслимов С.А., Шумкин А. М., Султанов Р. З., 1999), главной особенностью этого Аллопланта является выраженная стимуляция миграционной, фагоцитарной и лизосомальной активности макрофагов, которые концентрируются в зоне введения Аллопланта, а также восстановление нормального фенотипа резидентных макрофагов хориоидеи и клеток пигментного эпителия сетчатки. Можно предположить, что механизм регенераторного влияния этого вида биоматериала раскрывается в двух аспектах. Первый аспект – это активация мононуклеарных фагоцитов, которые принимают участие в лизисе недоокисленных продуктов обмена, накопившихся в хорио-ретинальном комплексе, а также являются регуляторами активности других клеточных популяций за счет цитокинов, например, фактора роста фибробластов, который замедляет дегенерацию нейронов сетчатки (Faktorovich E.G. с соавт., 1990; La Vail M.M., с соавт., 1992). Вторым немаловажным фактором положительного влияния биоматериала являются, на наш взгляд, продукты его биологической деградации – гликозаминогликаны и гликопротеины. Известно, что при нарушении хорио-ретинального барьера, приводящего к дистрофическим изменениям наружных слоев сетчатки, происходит значительное снижение количества гликозаминогликанов, а именно гепаран-сульфата, в межфоторецепторном матриксе (Prunte C., Kain H. L., 1995). Исследование, проведенное сотрудником Центра Р. А. Хасановым (1999), выявило преобладание гепаран-сульфата среди гликозаминогликанов диспергированного биоматериала Аллоплант. А то, что продукты деградации биоматериала после ретросклерального введения накапливаются во всех оболочках глаза, в том числе и сетчатке, убедительно доказано С. А. Муслимовым (2000) с помощью радиоизотопного исследования. Четвертый тип биоматериала Аллоплант, также имеющий диспергированную (порошкообразную) форму и чаще всего применяемый при «сухих» формах сенильной макулодегенерации экстраокулярно, был условно назван “Стимулятором васкулогенеза”. Этот вид Аллопланта, как показали исследования Муслимова С.А. (2000) и Хасанова Р.А. (1999), способствует более интенсивному ангиогенезу. Для более наглядной демонстрации вышеизложенного, мы свели последовательность морфофункциональных взаимодействий, лежащих в основе регенеративной хирургии сенильной макулодегенерации, с применением биоматериалов Аллоплант в единую схему (рис. 21). На практике, в зависимости от стадии заболевания и степени поражения можно применять все четыре вида Аллоплантов в комбинации для усиления эффекта действия, но возможно и изолированное применение каждого вида биоматериала. Из изолированных видов хирургических вмешательств мы чаще всего пользуемся введением порошкообразного «стимулятора фагоцитоза» или «стимулятора васкулогенеза» для поддержания эффекта проведенной интраокулярной операции в последующие годы диспансерного наблюдения больного. Это вмешательство, носящее экстраокулярный характер, названо лечебным ретросклеропломбированием. Техника операции чрезвычайно проста – Аллоплант вводится в виде суспензии через микроразрез конъюнктивы с помощью изогнутой иглы в субтеноново пространство.
Резюмируя вышеизложенное, можно заключить, что регенеративно-хирургический подход в отличие от других методов лечения сенильной макулодегенерации обеспечивает комплексный биологический эффект, позволяющий в достаточной степени нивелировать патологические изменения в хорио-ретинальном коплексе и стабилизировать зрительные функции.
Таким образом, разработана хирургическая технология с использованием биоматериалов Аллоплант, оказывающая влияние на патогенетические механизмы сенильной макулодегенерации путем стимуляции процессов репаративной регенерации в хориоидее и сетчатке. Биоматериалы Аллоплант для реваскуляризирующих операций при помещении в супрахориоидальное пространство индуцируют ангиогенез и создают дополнительный источник кровообращения оболочек глазного яблока, способствуя улучшению микроциркуляции при сенильной макулодегенерации.
Разработанные на основе биоматериалов Аллоплант хирургические технологии стимулируют процессы внутриклеточной регенерации в пигментном эпителии и нейронах сетчатки и тем самым замедляют дегенеративные процессы при сенильной макулодегенерации.
Хирургическая технология Аллоплант при лечении сенильной макулодегенерации включает следующие экстра- и интраокулярные операции:
- при I стадии сенильной макулодегенерации, независимо от формы заболевания, выполняется операция лечебного ретросклеропломбирования с использованием диспергированных биоматериалов - «стимулятора фагоцитоза» или «стимулятора васкулогенеза»;
- при «сухой» форме сенильной макулодегенерации II, III, IV стадий выполняется интраокулярная операция реваскуляризации хориоидеи с одновременным введением диспергированного биоматериала «стимулятор васкулогенеза» в субтеноново пространство;
- при «влажной» форме сенильной макулодегенерации показана интраокулярная операция реваскуляризации хориоидеи с аутолимфосорбцией и введением диспергированного биоматериала «стимулятор фагоцитоза» в субтеноново пространство.
Показанием для хирургических вмешательств с применением биоматериалов Аллоплант являются все стадии и формы сенильной макулодегенерации. При этом операция лечебного ретросклеропломбирования (экстраокулярное введение «стимулятора фагоцитоза» и «стимулятора васкулогенеза») не имеет противопоказаний. Противопоказанием для интраокулярной операции реваскуляризации или аутолимфореваскуляризации хориоидеи являются лишь соматические заболевания.
Технология хирургического лечения сенильной макулодегенерации биоматериалами Аллоплант включает в себя проведение повторных оперативных вмешательств при снижении зрительных функций после первичной операции и чеще в виде лечебного ретросклерального пломбирования.
Клиническое применение комплекса хирургических технологий Аллоплант у больных с сенильной макулодегенерации позволяет получить стабильный эффект в сроки до 8 лет в виде стабилизации и улучшения зрительных функций при различных стадиях заболевания: - при I стадии улучшение наступило у 68% и стабилизация - у 27%; - при II стадии улучшение наступило у 63% и стабилизация - у 22%; - при III улучшение наступило у 59% и стабилизация - у 18%; - при IV улучшение наступило у 43% и стабилизация - у 48%.
Практические рекомендации
- Для хирургического лечения всех стадий и форм сенильной макулодегенерации предлагается комплекс интра- и экстраокулярных вмешательств с использованием биоматериалов Аллоплант: - Аллоплант для реваскуляризации хориоидеи; - Аллоплант для аутолимфосорбции; - стимулятор васкулогенеза; - стимулятор фагоцитоза.
- Лечебное ретросклеропломбирование может проводиться в амбулаторных условиях.
- Повторное интраокулярное вмешательство в том же секторе глазного яболка возможно через 2 - 2,5года. 4. Повторное экстраокулярное вмешательство (лечебное ретросклеропломбирование) возможно не ранее чем через 6 месяцев.
Литература
- Изучение гемодинамики и реактивности внутриглазных сосудов с помощью реоофтальмологии // Элеткрофизиология органа зрения в практике офтальмологии. — Москва, 1974. — С. 23-27 (соавт. Беленький К.Р.).
- Методы определения нейроваскулярной реакции глаза // Нейроваскулярная патология органа зрения. - Табилиси, 1976. - С. 222-224 (Соавт. Беленький К.Р.).
- К организации магнитотерапии в лечении глазных заболеваний // Актуальные вопросы повреждений и вирусных заболеваний органа зрения. - Уфа, 1977. - С. 69-70.
- Магнитотерапия при дистрофических заболеваниях сетчатки // Актуальные вопросы повреждений и вирусных заболеваний органа зрения. - Уфа, 1977. - С. 71-72.
- К патогенезу терапевтического эффекта магнитного поля магнитофоров // Профилактика, медицинская реабилитация слепоты и слабовидения. -Уфа, 1979.-С. 113-114.
- Опыт работы Московского центра реабилитации инвалидов по зрению // Материалы 4 Всероссийского съезда офтальмологов 1982 (Соавт. Глазко И.В.).
- Реабилитация инвалидов по зрению путем прямой реваскуляризации глазного яблока. Тез. докл. 7 Украинского съезда офтальмологов. - Одесса, 1984. - С. 204-205 (соавт. Т.Ю.Амарян).
- Новые возможности медицинской реабилитации слабовидящих с нейроциркуляторными заболеваниями сетчатки и зрительного нерва. // Актуальные вопросы социальной офтальмологии сб. научн. тр. - М., 1985. — С. 68-70 (соавт. Е. С. Либман, Т. К., Амарян, О. Я. Сергеевой).
- Воздействие на синокаротидную зону в восстановительном лечении больных и инвалидов с заболеваниями сетчатки и зрительного нерва, // 6 Всесоюзный съезд офтальмологов. - М., 1985. - С. 116-117 (соавт. Т.Ю.Амарян, А.М.Харитоновой).
- Изолированные и сочетанные применения лазеров вагосимпатическими блокадами при центральных склеротических дистрофиях сетчатки // Т Эффективные методы диагностики и лечения при тяжелой патологи органа зрения.- Тез. докл. международной конференции Одесса, 1985. - С. 286-288 (Соавт. Е.С. Либман).
- Ревакуляризация хориоидеи зрительного нерва с применением Аллопланта // VI съезд офтальмологов России. - М., 1994. - С. 99 (соавт. Мулдашев Э.Р., Галимова В.У., Кийко Ю.И., Булатов Р.Т., Захваткина К.А.).
- Применение аллотрансплантатов серии Аллоплант в лечении геморрагических форм диабетической ретинопатии // VI съезд офтальмологов России. - М., 1994. - С. 177 (соавт. Мулдашев Э.Р., Родионов О.В., Галимова В.У., Булатов Р.Т., Мустафин М.М., Муслимов С.А., Кийко Ю.И.).
- Basic research conducted on Alloplant biomaterials // European Journal of Ophthalmology. - Milano, 1999. - P. 8-13 (Соавт. Мулдашев Э.Р., Муслимов С.А, Нигматуллин Р.Т., Кийко Ю.И., Галимова В.У., Салихов А.Ю., Сельский Н.Е., Булатов Р.Т., Мусина Л.А.).
- Регенеративно-биологическая хирургия сенильной дегенерации сетчатки // Актуальные вопросы клинической медицины. Сборник научных работ, посвященных 80-летию поликлиники №3 ЛДО МЗ РФ - М., 1999. - С. 200-202.
- Регенеративно-биологические подходы к лечению сенильной макулодегенерации // VII съезд офтальмологов России. Тез. докл. Часть 1. - М., 2000. - С. 446.
- Регенеративно-хирургическое лечение сенильной макулодегенерации биоматериалом Аллоплант // VII съезд офтальмологов России. Тез. докла.. Часть 1. - М., 2000. - С. 446-447.
- Трансплантационный ангиогенез - ведущий фактор реваскуляризирующих операций в офтальмологии // VII съезд офтальмологов России. Тез. докл.. Ч- 2. - М., 2000. -С.324 соавт. Нигматуллин Р.Т., Галимова В.У.).
- Морфофункциональные зоны тканевого ложа трансплантата // Морфология 2000, №3. - С. 88. (Соавт. Нигматуллин Р.Т., Галимова В.У., Минигазимов Р.С., Кийко Ю.И., Поляков В. А.).
- Регенеративная хирургия сенильной макулярной дегенерации биоматериалом Аллоплант // Материалы XII научно-практической конференции «Новые технологии микрохирургии глаза». - Оренбург, 2001.-С. 199-202. 20. Структура заболеваемости сенильной макулодегенерацией // Материалы XII научно-практической конференции «Новые технологии микрохирургии глаза». - Оренбург, 2001. - С. 274-278.
к содержанию | опубликовать статью
Хирургическая реабилитация больных анофтальмом на основе применения биоматериалов Аллоплант
Кульбаев Н.Д.
ФГБУ «Всероссийский центр глазной и пластической хирургии Минздравсоцразвития России», г. Уфа
Автором для формирования опорно-двигательной культи после энуклеации был использован биоматериал Аллоплант для замещения объёмных дефектов. Биоматериал Аллоплант был использован при отсроченной имплантации опорно-двигательной культи и устранения недостаточного функционального и косметического эффектов после предыдущих операций. Разработаны критерии количественной оценки эффективности хирургической реабилитации больных анофтальмом с применением биоматериалов Аллоплант.
Актуальность По данным Р.А.Гундоровой (1980) в лечебных учреждениях страны за год производится более 3500 энуклеаций и более 5000 человек нуждаются в протезировании. В связи с учащением огнестрельных ранений боевого и криминального происхождения этот вопрос на сегодняшний день стоит особенно остро (Р.А.Гундорова, А.В.Степанов, О.И.Кваша, 1995). Другие авторы приводят данные о необходимости удаления глазного яблока в России более чем у 12 тысяч пациентов (Ю.А.Чеглаков, А.Ц.Лясковик, 1995, 1997). Эти авторы указывают, что в 2/3 случаях не формируется опорно-двигательная культя. Вышеуказанные причины приводят к недостаточности опорно-двигательной культи и образованию огромной конъюнктивальной полости. При протезировании в таких случаях используются тяжелые большие глазные протезы, которые не только не устраняют косметический дефект, но приводят к провисанию нижнего века (Kaltreider S.A., 2000). Для профилактики и устранения этих недостатков применяется несколько методов хирургического лечения. Формирование первичной или вторичной опорно-двигательной культи, как правило, устраняет вышеперечисленные дефекты. Другие виды оперативного лечения лишь дополняют косметический эффект.
При первичной и вторичной имплантации опорно-двигательной культи используется большое количество материалов. Согласно международной классификации трансплантатов (Вена, 1967) их принято делить по происхождению на аутологичные (ткани самого больного), аллогенные (ткани донора), ксеногенные (ткани животных) и эксплантаты (чужеродные небиологические материалы) (Шиф Л.В., 1973; Гундорова Р.А. с соавт., 1996; Коваленко П.П., 2000). Среди аутологичных трансплантатов типичным является подкожная жировая клетчатка (Покровский А.И., 1959; Плешаков В.В., Федотов В.Г., 1981). У данного материала имеются существенные недостатки: нанесение больному дополнительной травмы, плохая приживлямость и быстрая резорбция (Филатов В.П., 1933; Покровский А.И., 1944; Мухамеджанова М.М., 1966). Аналогичные недостатки имеют кожа с подкожно-жировой клетчаткой (Соколенко О.М., 1963; Цветков В.Л., Н.В.Цветков Н.В., 1987), широкая фасция бедра, у реберный хрящ и т.д. (Шиф Л.В., 1973).
Ксенотрансплантация не получила широкого распространения ввиду иммунологического барьера межвидовой несовместимости тканей (Жаворонков Н.А., Перельман М.И., 1993).
Эксплантаты, изготовленные из инертных металлов, представляют в настоящее время лишь исторический интерес (Doherty, 1923; Freiberger, 1937). При применении синтетических материалов наблюдается множество осложнений, среди которых обнажение имплантатов и их отторжение (Филатова И.А., Катаев М.Г., 1996; Горячев Ю.Е. с соавт., 1996; С.Н.Федоров С.Н. с соавт., 1998). Использование в качестве имплантата природных материалов, таких как гидроксиапатит, получило большое распространение (David R. Jordan, Stanley Chan, Louise Mawn et al., 1999; Philip L. Ouster, Kathryn M. T-rinkaus, Jane Fornoff, 1999). Недостатками данного материала является выраженный отек конъюнктивы, сильная послеоперационная боль (Edelstein C, Shields CL, De Potter P, Shields JA, 1997; Oestreicher JH, Liu E, Berkowitz M, 1997). Кроме того, высокая цена данного имплантата делает его недоступным для большей части нуждающихся пациентов (Филатова И.А., Катаев М.Г., 1996).
Осложнения в виде обнажения и выталкиваний эксплантатов или трансплантатов не идентичны при имплантации сходных типов материалов для формирования опорно-двигательной культи. Причиной возникновения или не возникновения осложнения могут быть: надежность гемостаза; соответствие объёма имплантата размерам полости теноновой капсулы; шовный материал для фиксации мышц и ушивания теноновой капсулы; время снятия швов; поведение больного в первые 3-5 недель после операции; растяжение и разрыв тканей у передней поверхности жесткого имплантата (Шиф Л.В., 1973). Многие перечисленные причины относятся к той категории, где имеют место тактика лечения и опыт лечащего врача данной категории больных. Свойства трансплантатов и эксплантатов, применяемых для формирования опорно-двигательной культи, перечислены выше. Применяемый для фиксации прямых мышц глазного яблока и герметизации теноновой капсулы в качестве шовного материала кетгут к 5-му дню теряет половину первоначальной крепости, а к 10-му дню прочность их ничтожна. За этот короткий период сохранения прочности кетгута мышцы и теноновая капсула не успевают надежно срастаться. Другие небиологические шовные материалы имеют отрицательные свойства, такие как прорезывание, инкапсуляция и лигатурные свищи. Учитывая ненадежность кетгута и других небиологических шовных материалов, мы обратили внимание на аллосухожильные нити, применяемые в челюстно-лицевой хирургии в качестве погружного шовного материала, которые испытывают значительную статическую и динамическую нагрузку (Юсупбаев Б.С., Мулдашев Э.Р., 1977; Булатов Р.Т., 1981; Гурьянов А.С., 1993; Гурьянов А.С., Салихов А.Ю., 1994; Булатов Р.Т. с соавт., 1997).
При других офтальмопластических оперативных вмешательствах, в частности, при устранении недостаточности нижнего века, используются модифицированные трансплантаты и эксплантаты из вышеперечисленных материалов (Катаев М.Г., 1983; 1986; Морозова О.Д., 1980; Кирилличев А.И., 1981).
Таким образом, многие трансплантаты и эксплантаты, применяемые при анофтальмическом синдроме, не отвечают следующим требованиям: низкому удельному весу, незначительной резорбционной способности, хорошей переносимости тканями, отсутствию канцерогенных свойств, способности к формообразованию, отсутствию аллергических реакций, хорошей стерилизуемости (Шкромида М.И., Мосяк М.А., 1991; Филатова И.А., Катаев М.Г., 1996).
В Федеральном государственном учреждении «Всероссийский центр глазной и пластической хирургии» Министерства здравоохранения Российской Федерации (директор д.м.н., профессор Э.Р. Мулдашев) разработан и выпускается серийно ряд биоматериалов Аллоплант для различных пластических операций, которые практически отвечают вышеизложенным требованиям.
Целью исследования являются разработка и внедрение методов хирургической реабилитации больных анофтальмом с применением биоматериалов Аллоплант.
Материалы и методы исследования
С применением биоматериалов Аллоплант пролечено 334 пациента. Формирование опорно-двигательной культи из биоматериалов Аллоплант было произведено в 347 случаях. Наблюдаемые нами пациенты были подразделены на три группы по срокам формирования опорно-двигательной культи. В первую группу вошли 135 пациентов, которым после энуклеации первично была сформирована опорно-двигательная культя из биоматериала Аллоплант.
Техника операции формирования опорно-двигательной культи из биоматериалов Аллоплант после энуклеации
Под общей анестезией, после обработки операционного поля на веки накладывали блефаростат. Микрохирургическим пинцетом фиксировали конъюнктиву глазного яблока и делали её надрез у лимба. При помощи изогнутых ножниц через сформированный надрез отсекали конъюнктиву вокруг лимба. Разрез необходимо производить как можно ближе к лимбу, тем самым максимально сохранив и минимально травмируя конъюнктиву (рис. 1).
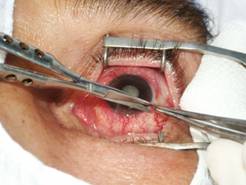 |
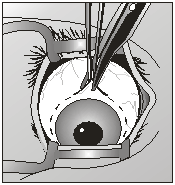 |
| Рис. 1 Разрез конъюнктивы вокруг лимба | |
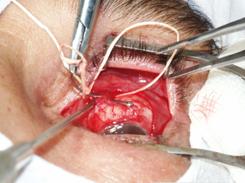
Далее отсепаровывали конъюнктиву и теноновую оболочку тупым путем изогнутыми ножницами. Имеющиеся рубцы и спайки пересекали, не повреждая склеру. После отсепаровки конъюнктивы и теноновой оболочки выделяли прямые глазные мышцы. В первую очередь выделяли верхнюю прямую мышцу с помощью мышечного крючка. Мышцу прошивали аллосухожильной нитью и пересекали у места прикрепления к склере (рис. 2).
 |
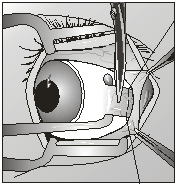 |
| Рис. 2 Выделение прямых мышц глазного яблока и прошивание их аллосухожильными нитями | |
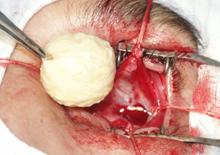
Аналогичные действия проводили с нижней и наружной прямыми мышцами. Внутреннюю прямую мышцу прошивали аллосухожильной нитью, отступя от места прикрепления к склере на 5-6 мм. Пересекали мышцу таким образом, чтобы оставалась культя на глазном яблоке длиной 3-5 мм. Культю использовали для фиксации глазного яблока с помощью кровоостанавливающего зажима. Мобилизованное глазное яблоко легко вывихивалось. При помощи зажима глазное яблоко вытягивали вперед, повторяя поворот глазного яблока кнаружи вокруг вертикальной оси. После этого зрительный нерв становится доступным для перерезки. Изогнутые бранши ножниц проводили в сомкнутом положении с медиальной стороны к зрительному нерву. Концом ножниц нащупывали зрительный нерв, далее чуть вытягивали ножницы и разводили бранши. Раздвинутыми браншами ножницы вновь продвигали в глубь орбиты так, чтобы зрительный нерв попал между браншами. В таком положении бранши ножниц отодвигали от склеры на 2-4 мм и одним движением пересекали зрительный нерв. Глазное яблоко подтягивали вперед и пересекали сухожилия обеих косых мышц у склеры. После удаления глазного яблока проводили гемостаз путем тампонады полости орбиты марлевой салфеткой, смоченной в растворе перекиси водорода. После удаления тампона в полость орбиты имплантировали Аллоплант для формирования опорно-двигательной культи (рис. 3).
 |
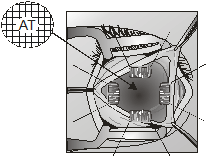 |
| Рис. 3 Имплантация биоматериала Аллоплант для формирования опорно-двигательной культи | |
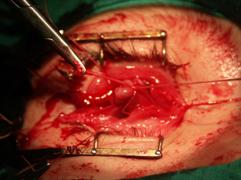
Прямые мышцы глазного яблока соединяли между собой над Аллоплантом для формирования опорно-двигательной культи, используя ранее наложенные аллосухожильные нити (рис. 4).
 |
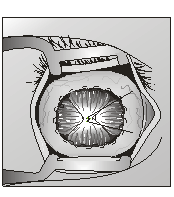 |
| Рис. 4 Перекрестное соединение прямых мышц глазного яблока над биоматериалом Аллоплант | |
При соединении мышц использовали парное соединение мышц-антогонистов. В некоторых случаях прямые мышцы глаза были фиксированы кпереди от экватора опорно-двигательной культи на 4-5 мм (рис. 5).
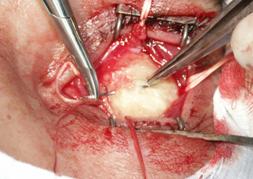 |
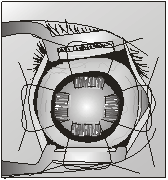 |
| Рис. 5 Фиксация прямых мышц глазного яблока к биоматериалу Аллоплант для формирования опорно-двигательной культи ранее наложенными аллосухожильными нитями | |
Следующим этапом герметично ушивали тенонову оболочку аллосухожильными нитями. На данном этапе накладывали кисетный шов, иногда узловые швы. Узлы погружали в рану, то есть в тенонову полость (рис. 6).
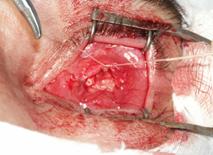 |
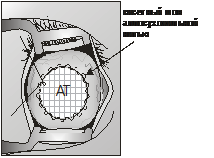 |
| Рис. 6 Наложение на тенонову капсулу кисетного шва аллосухожильной нитью | |
На конъюнктиву накладывали узловые швы викрилом 3-4/0 (рис. 7).
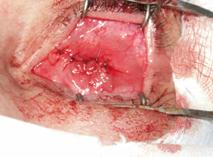 |
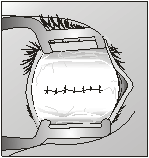 |
| Рис. 7 Ушивание конъюнктивальной раны | |
Вторая группа состояла из 199 пациентов, которым была произведена отсроченная имплантация опорно-двигательной культи при анофтальме.
Техника операции отсроченной имплантации опорно-двигательной культи из биоматериалов Аллоплант
Под наркозом устанавливали блефаростат и хирургическим пинцетом захватывали конъюнктиву с теноновой капсулой. Делали сквозную насечку в нижне-наружном или верхне-наружном секторе ближе к центру (рис. 8).
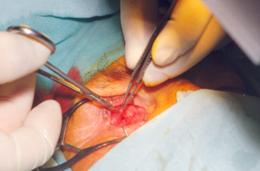 |
 |
| Рис. 8 Захват конъюнктивы с подлежащими тканями и нанесение сквозной насечки | |
В рану вставляли одну из браншей ножниц и разрез продолжали, учитывая ход мышц. Длина разреза должна превышать диаметр Аллопланта. Тенонову оболочку брали на четыре шва-держалки. В полость орбиты вводили зажим Кохера в сомкнутом положении и в глубине орбиты бранши зажима раздвигали, не применяя усилий, тем самым создавая ложе для Аллоплантата (рис. 9).
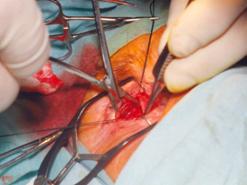 |
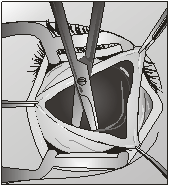 |
| Рис. 9 Формирование ложа в полости орбиты с помощью зажима Кохера | |
Ревизию ложа производили пальпаторно. Ослабив блефаростат и используя швы-держалки, в полость орбиты вводили Аллоплант для формирования опорно-двигательной культи. Для удобства и жесткой фиксации Аллопланта использовали зажим Кохера (рис. 10).
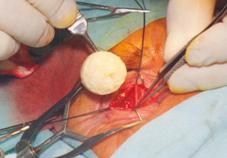 |
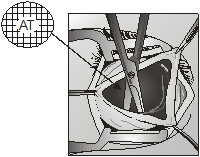 |
| Рис. 10 Имплантация в полость орбиты Аллопланта для формирования опорно-двигательной культи | |
После имплантации производили пальпаторный контроль положения имплантата. Он должен находится в мышечной воронке. Края теноновой оболочки и конъюнктивы освобождали, если они были завернуты вместе с Аллоплантом. Рану ушивали послойно, герметично: на тенонову оболочку накладывали шов аллосухожильной нитью (рис. 11).
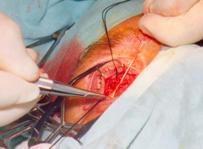 |
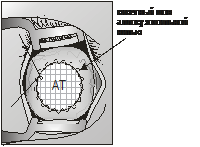 |
| Рис. 11 Ушивание теноновой капсулы аллосухожильной нитью | |
На конъюнктиву накладывали узловые швы викрилом 3-4/0 (рис. 12.).
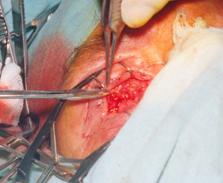 |
 |
| Рис. 12 Ушивание конъюнктивальной раны | |
Третья группа состояла из 12 пациентов, которым отсроченная имплантация опорно-двигательной культи производилась неоднократно (в 11-ти случаях 2 раза и в 1-ом случае 3 раза).
Хирургическая техника повторной имплантаций опорно-двигательной культи с биоматериалом Аллоплант
Под общей анестезией после обработки операционного поля, на веки накладывали блефаростат. Тщательно производили ревизию конъюнктивальной полости и глазного протеза. При этом отмечали состояние сводов, форму и размеры культи. При осмотре глазного протеза фиксировали внимание, на какой части протеза имеются дополнительные увеличенные части. Разрез конъюнктивы и теноновой капсулы производили в тех секторах, где имелся наибольший дефицит тканей. Формирование ложа для биоматериала Аллоплант производили тупым методом с помощью зажима Кохера. Ранее имплантированный биоматериал Аллоплант в течение 1 года представлял собой нежную соединительную ткань с большим количеством элементов жировой клетчатки. Формирование ложа для предстоящей имплантации биоматериала не представляло особых трудностей. Моделирование биоматериала Аллоплант производили с учетом ревизии конъюнктивальной полости и глазного протеза. Смоделированный и трансплантированный биоматериал Аллоплант устранял недостатки опорно-двигательной культи и видоизменял конъюнктивальную полость для стандартного тонкостенного глазного протеза. Моделирование сложной по форме и различного объёма имплантатов возможно благодаря уникальным и пластичным свойствам данного вида биоматериала Аллоплант. Герметизацию теноновой капсулы проводили наложением кисетного или узлового шва из аллосухожильной нити Аллоплант. На конъюнктиву накладывали узловые швы викрилом 3-4/0. На операционном столе подбирали соответствующий по размерам и цвету стандартный глазной протез.
Все три группы прослежены сроком свыше 10-ти лет с естественной убылью количества наблюдаемых пациентов. В процессе исследования возникли сложности в оценке косметического результата после хирургической реабилитации больных с анофтальмом, так как по литературным данным имеется объективная оценка тех или иных параметров, но нет оценки в совокупности этих данных. Таким образом, нет общепринятого и стандартного метода оценки косметического эффекта. На основе общепринятых методов обследования пациентов с анофтальмом (Л.В. Шиф, 1981) был разработан метод полуколичественной оценки косметического результата в баллах (табл. 1).
| Признаки объективного исследования | «Неудовлетвори-тельный» результат | «Удовлетвори-тельный» результат | «Хороший» результат |
| I. Глубина положения протеза | Обезображивающее – 1 балл | Умеренное явное – 2 балла | Малозаметное – 3 балла |
| II. Объём движений глазного протеза | До 45º – 1 балл | От 45º до 90º – 2 балла | 90º и больше – 3 балла |
| III. Состояние рельефа верхнего века | Резко выраженное – 1 балл | Умеренное – 2 балла | Небольшое – 3 балла |
| IV.Симметричность положения глазного протеза и второго глаза «косоглазие» | Свыше 20º – 1 балл | От 15º до 20º – 2 балла | До 15º – 3 балла |
| V.Симметричность раскрытия глазных щелей | Свыше 4 мм – 1 балл | От 2 мм до 4 мм – 2 балла | До 2 мм – 3 балла |
| VI. Оценка косметического результата самим пациентом | «Неудовлетвори-тельный» – 1 балл | «Удовлетвори-тельный» – 2 балла | «Хороший» – 3 балла |
| Средняя сумма баллов | 6 | 12 | 18 |
| Количество баллов для определенного результата (в сумме) | До 10 баллов | От 11 до 15 баллов | От 16 до 18 баллов |
По истечении 3 – 6 месяцев после операции и подбора индивидуального глазного протеза в лаборатории полимерных медицинских изделий и индивидуального протезирования был проведен анализ с использованием данного метода объективной оценки косметического результата в хирургической реабилитации пациентов с анофтальмом.
Удаление глазного яблока с формированием опорно-двигательной культи из биоматериалов Аллоплант проведено 135 пациентам. В отдаленные сроки наблюдения отмечалось стойкое сохранение хорошего косметического результата в пределах 97,4 - 98,3%.
Отсроченная имплантация опорно-двигательной культи из биоматериалов Аллоплант проведена 199 пациентам. В отдаленные сроки косметический результат в целом стабилен, но с некоторой тенденцией уменьшения показателей в группе «хороший» результат с 95,9 до 94%, увеличение в группе «неудовлетворительный» с 0 до 1,5% и в группе «удовлетворительный» с 4,1 до 4,5%.
Повторные имплантации опорно-двигательной культи были проведены 12 пациентам, из них одному пациенту 3 раза. Раннее послеоперационное течение протекало без особенностей. Через 4-6 месяцев производили индивидуальное глазное протезирование. В отдаленные сроки «хороший» косметический результат с 83,3 (в сроки наблюдения до 5 и до 10 лет) до 100 % (свыше 10 лет).
Таким образом, в группе больных, которым было проведено удаление глазного яблока с формированием опорно-двигательной культи из биоматериалов Аллоплант, в сроки наблюдения до 5 и до 10 лет существенными факторами, влияющими на субъективную оценку самого больного, оказались категории «западение глазного протеза», «западение верхней орбито-пальпебральной борозды» и «объём движения глазного протеза». Два других фактора - «косоглазие» глазного протеза и симметричность глазных щелей, не играли существенной роли в этих сроках наблюдения. Это объясняется тем, что пациенты сроком наблюдения до 10 лет после удаления глазного яблока обращают внимание на те факторы, которые появились с отсутствием глазного яблока (объём движения глазного протеза, степень западения глазного протеза и верхней орбито-пальпебральной борозды). Остальные факторы, как правило, имели место до операции (косоглазие больного глаза и асимметрия глазной щели).
В сроки наблюдения более 10 лет в группе с первичным формированием опорно-двигательной культи из биоматериалов Аллоплант со стабилизацией фундаментальных признаков (западение глазного протеза, верхней орбито-пальпебральной борозды и амплитуды движения глазного протеза) внимание пациентов переключается на более мелкие детали косметического состояния, которые могли присутствовать до операции (косоглазие больного глаза и асимметрия глазной щели).
Совершенно другая картина в группе с отсроченной имплантацией опорно-двигательной культи из биоматериала Аллоплант. Практически во всех случаях во время удаления глазного яблока не была сформирована опорно-двигательная культя. Вследствие этого у большинства пациентов наблюдались западение верхней орбито-пальпебральной борозды и небольшой объём движения глазного протеза. Во все сроки наблюдения в послеоперационном периоде наибольший вклад в оценку субъективной удовлетворенности пациента вносили эти два фундаментальных фактора. Степень западения глазного протеза и симметричность глазных щелей оказывали переменное влияние на субъективную оценку, но существенно на неё не влияли. Уровень «косоглазия» глазного протеза в данной группе пациентов на субъективную оценку самого пациента не влиял во всех сроках наблюдения.
Подтверждением клинических результатов является анализ полученных данных клинико-морфологического исследования биопсийного материала. Он который показал, что через 1 год после трансплантации биоматериала Аллоплант для формирования опорно-двигательной культи отмечалось формирование зрелой неоформленной соединительной ткани в области локализации жировых долек трансплантата с очаговой инфильтрацией фибробластов. Зрелая неоформленная соединительная ткань имела зрелые сосуды (артериолы, капилляры, венулы) с упорядоченным направлением, которые формировали замкнутое микроциркуляторное русло. Через 5 лет наблюдалась оформленная соединительная ткань, которая состояла из упорядоченных коллагеновых волокон различной толщины. Клеточная плотность была очень низкой за счет диффузно рассеянных единичных фибробластов и фиброцитов. Сформированный регенерат обладает хорошо развитой сосудистой сетью с упорядоченным направлением дифференцированных сосудов.
Полное формирование новообразованной ткани на месте имплантированного биоматериала Аллоплант для создания опорно-двигательной культи происходило в сроки до 5 лет после имплантации. Новообразованный регенерат представлял собой дифференцированную соединительную ткань из плотной оформленной соединительной ткани и жировой ткани с развитой сосудистой сетью. Данная фиброархитектоника регенерата, по-видимому, обусловлена выполняемой функциональной нагрузкой.
Структура аллосухожильных нитей была представлена фрагментами плотной оформленной соединительной ткани, построенной из толстых коллагеновых волокон на 2-3-й месяцы после проведения оперативного лечения. Через 5 месяцев после операции картина трансформации волокон аллосухожильных нитей выглядела неоднородно. В некоторых участках, преимущественно по краю, наблюдалась незрелая соединительная ткань с нежным соединительно-тканным каркасом и большим количеством фибробластов.
Таким образом, в результате макрофагально-фибробластической реакции аллосухожильные нити полностью трансформируются в новообразованную соединительную ткань в течение 5 месяцев после операции. При этом можно предположить, что картина замещения зависит от типа перифокальной соединительной ткани и характера функциональной нагрузки.
Исходя из анализа результатов исследования, можно констатировать:
- Стабильный косметический результат можно ожидать по истечении 1 года, а окончательный результат - через 5 лет по мере формирования полноценной опорно-двигательной культи.
- Применение аллосухожильных нитей снижает послеоперационные осложнение, такое как расхождение послеоперационного шва с последующей потерей имплантата.
- Выявленные недостатки биоматериала Аллоплант для формирования опорно-двигательной культи легко устранимы. В определенных условиях недостатки данного материала играют положительную роль в процессе лечения. Дробное введение биоматериала Аллоплант в полость орбиты продиктовано тем, что через год морфологически отмечается образование зрелой неоформленной соединительной ткани, а полное замещение небольшого объема от 3 до 5,6 см3 происходить в течение 5-ти лет. С увеличением объёма биоматериала отмечается удлинение этих сроков. Дозированная имплантация биоматериала Аллоплант при анофтальмическом синдроме после лучевой терапии по поводу ретинобластомы позволяет компенсировать дефицит мягкой ткани в области поражения, не вызывая осложнения в виде некрозов кожи и т.д.
Сопоставляя полученные данные с литературными данными, можно сказать, что оголение биоматериала Аллоплант не наблюдалось. По литературным данным это осложнение составляет при применении хряща различного происхождения от 4,7 до 12,2 % (Катаев М.Г., 1981; Каспаров А.А. с соавт., 1984).
Применение данного вида биоматериала Аллоплант дает наилучший результат по сравнению широко применяемыми имплантатами (Федорищева Л.Е. с соавт., 2002).
Таким образом, разработанные нами методы хирургической реабилитации больных анофтальмом с применением биоматериалов Аллплант позволяют сформировать оптимальную для эффективного косметического глазного протезирования опорно-двигательную культю, а разработанные нами критерии полуколичественной оценки результатов хирургического лечения и индивидуального косметического глазного протезирования определить их эффективность.
Заключение и практические рекомендации
Разработаны и внедрены эффективные методы хирургической реабилитации больных анофтальмом с применением биоматериала Аллоплант для формирования опорно-двигательной культи и аллосухожильных нитей Аллоплант.
Морфологически на биопсийном материале установлено, что биоматериал Аллоплант для формирования опорно-двигательной культи шаровидной формы после имплантации в тенонову полость постепенно (в сроки до 5 лет) замещается новообразованной дифференцированной соединительной тканью с развитой сосудистой сетью, соответствующей по фиброархитектонике выполняемой ею функции.
Аллосухожильные нити, применяемые для наложения кисетного шва на тенонову оболочку, прочно фиксируют имплантированный биоматериал в сроки наблюдения до 1 года постепенно замещаются новообразованной тканью, подобной по структуре исходной нити.
Метод первичной имплантации биоматериала Аллоплант для формирования опорно-двигательной культи после энуклеации позволяет получить хорошие косметические результаты в сроки наблюдения до 5 лет, до 10 лет и более в 97,4 - 98,3% случаев.
Метод отсроченной имплантации опорно-двигательной культи из биоматериалов Аллоплант при анофтальме позволил добиться хорошего косметического протезирования в сроки наблюдения до 5 лет, до 10 лет и более в 94 - 95,9% случаев.
Применение биоматериала Аллоплант для формирования опорно-двигательной культи при повторной отсроченной имплантации с целью дополнения объёма опорно-двигательной культи позволило улучшить эффективность хирургической реабилитации во все сроки наблюдения и получить хороший косметический результат у 83,3% больных анофтальмом в сроки наблюдения до 5 и до 10 лет, у 100% больных более 10 лет.
Показанием к применению биоматериалов Аллоплант в качестве трансплантата для формирования опорно-двигательной культи являются энуклеация, анофтальм без опорно-двигательной культи и недостаточный размер опорно-двигательной культи. Противопоказанием являются наличие злокачественного новообразования, прорастающего за пределы глазного яблока, явное инфицирование полости орбиты и размозжение мягких тканей орбиты.
Разработанный нами метод количественной оценки результатов хирургической реабилитации больных анофтальмом эффективен и может быть использован в практике врачей-офтальмологов и глазных протезистов.
Практические рекомендации
С целью повышения эффективности хирургической реабилитации пациентов анофтальмом и получения хорошего косметического глазного протезирования рекомендуется использовать для формирования опорно-двигательной культи из биоматериала Аллоплант.
С целью прочной фиксации опорно-двигательной культи в полости орбиты рекомендуется накладывать на тенонову оболочку шов из аллосухожильных нитей Аллоплант.
Для определения эффективности хирургической реабилитации и косметического глазного протезирования пациентов анофтальмом рекомендуется использовать разработанные нами критерии полуколичественной оценки результатов.
Литература
- Анофтальмический синдром. Новые тенденции в тактике лечения // Новые технологии микрохирургии глаза. – Оренбург, 1996. –С. 66. (Соавт.: Булатов Р.Т.).
- Формирование опорно-двигательной культи после энуклеации глазного яблока // Актуальные проблемы современной офтальмологии. – Саратов, 1996. -С. 9-10. (Соавт.: Булатов Р.Т., Мулдашев Э.Р., Салихов А.Ю., Рыжов В.А., Родионов О.В.).
- Профилактика синдрома моторной десинхронизации опорно-двигательной культи при энуклеации // Материалы XII научно-практической конференции «Новые технологии микрохирургии глаза». - Оренбург, 2001. -С. 182-183. (Соавт.: Булатов Р.Т., Родионов О.В., Рыжов В.А.).
- Альтернативный метод обезболивания при пластических операциях на нижней стенке орбиты и нижнем веке // Медико-социальная реабилитация офтальмологических больных. – Тюмень, 1998. -С. 18. (Соавт.: Князев А.Д., Салихов А.Ю., Галимова Л.Ф., Малоярославцев В.Д.).
- Хирургическое лечение анофтальмических синдромов после энуклеации с лучевой терапией по поводу ретинобластомы // Новые технологии микрохирургии глаза. – Оренбург, 1996. -С. 98-99.
- К вопросу стабилизации результатов формирования опорно-двигательной культи после энуклеации // Медико-социальная реабилитация офтальмологических больных. – Тюмень, 1998. -С. 38. (Соавт.: Булатов Р.Т., Мулдашев Э.Р., Родионов О.В., Салихов А.Ю.).
- Формирование опорно-двигательной культи после энуклеации глазного яблока // Медико-социальная реабилитация офтальмологических больных. – Тюмень, 1998. -С. 37-38. (Соавт.: Булатов Р.Т., Мулдашев Э.Р., Салихов А.Ю, Рыжов В.А., Родионов О.В.).
- Отсроченная имплантация опорно-двигательной культи после энуклеации глазного яблока // Актуальные проблемы современной офтальмологии. – Саратов, 1996. -С. 56. (Соавт.: Булатов Р.Т., Мулдашев Э.Р., Салихов А.Ю., Рыжов В.А., Родионов О.В.).
- Отсроченная имплантация опорно-двигательной культи материалом серии «Аллоплант» при анофтальме // Медико-социальная реабилитация офтальмологических больных. – Тюмень, 1998. -С. 38-39. (Соавт.: Мулдашев Э.Р., Салихов А.Ю., Булатов Р.Т., Рыжов В.А. ).
- Отсроченная имплантация опорно-двигательной культи материалом серии «Аллоплант» при анофтальме // Актуальные вопросы офтальмологии, посвященные 170-летнему юбилею Московской офтальмологической клинической больницы. – М., 1996. -С. 215-216.
- Опыт использования чечевицеобразных лечебных протезов для формирования конъюнктивальной полости // Материалы I Евро-Азиатской конференции по офтальмохирургии. - Екатеринбург, 1998. -С. 121-122. (Соавт.: Рыжов В.А., Салихов А.Ю.).
- Аллопластическое расширение конъюнктивальной полости при анофтальмическом синдроме // Новые технологии микрохирургии глаза. - Оренбург, 1994. –С. 113-115. (Соавт.: Мулдашев Э.Р., Булатов Р.Т., Салихов А.Ю., Рыжов В.А.).
- Реконструкция конъюнктивальной полости при анофтальме // Новые технологии микрохирургии глаза. – Оренбург, 1994. –С. 112-113. (Соавт.: Мулдашев Э.Р., Булатов Р.Т., Салихов А.Ю., Рыжов В.А.).
- Морфологические аспекты пересадки аллотрансплантатов для фиксирующей пластики // Актуальные проблемы клинической офтальмологии. – Челябинск, 1999. -С. 201-203. (Соавт.: Мулдашев Э.Р., Салихов А.Ю., Искандеров Г.Ф., Кузнецов М.В.).
- Результаты клинико-морфологических исследований биоматериала Аллоплант для создания опорно-двигательной культи при анофтальме // 7-я научно-практическая конференция Екатеринбургского Центра МНТК «Микрохирургия глаза», - Екатеринбург, 1999. -С. 86-87. (Соавт.: Нигматуллин Р.Т., Искандеров Г.Ф., Рыжов В.А.).
- Структурные и биомеханические особенности фасциальных узлов области глазницы // Шестая научно-практическая конференция по вопросам хирургического лечения заболеваний органа зрения. – Екатеринбург, 1998. –С. 97-98. (Соавт.: Нигматуллин Р.Т., Мулдашев Э.Р., Салихов А.Ю., Искандеров Г.Ф.).
- Возможные пути оптимизации полимерных глазных протезов // 7-я научно-практическая конференция Екатеринбургского Центра МНТК «Микрохирургия глаза». - Екатеринбург, 1999. -С. 113-115. (Соавт.: Рыжов В.А., Салихов А.Ю.).
- Особенности социальной реабилитации больных с анофтальмом престарелого возраста // Ерошевские чтения.: Труды Всероссийской конференции «Геронтологические аспекты офтальмологии» и VI Международного семенара по вопросам пожилых «Самарские лекции», посвященные 100-летию со дня рождения Героя Социалистического Труда, лауреата Государственной премии СССР, заслуженного деятеля науки РСФСР, члена-корреспондента АМН СССР, профессора Т.И. Ерошевского / Под редакцией Г.П. Котельникова. – Самара: «Офорт»; СамГМУ, 2002. -С. 346-348. (Соавт.: Рыжов В.А., Салихов А.Ю., Нураева А.Б.).
- Опыт применения специальных косметических глазных протезов при заборе донорских глаз // Шестая научно-практическая конференция по вопросам хирургического лечения заболеваний органа зрения. – Екатеринбург, 1998. -С. 106-107. (Соавт.: Рыжов В.А., Чернов Н.В.).
- Способ формирования конъюнктивальной полости при врожденном анофтальме и микрофтальме // Пластическая хирургия придаточного аппарата глаза и орбиты. – М., 1996. –С. 65-66. (Соавт.: Салихов А.Ю., Булатов Р.Т., Мулдашев Э.Р., Рыжов В.А., Деревянных С.А.).
к содержанию | опубликовать статью
МОРФОЛОГИЧЕСКОЕ ОБОСНОВАНИЕ ПРИМЕНЕНИЯ СОЕДИНИТЕЛЬНОТКАННЫХ ТРАНСПЛАНТАТОВ МОДЕЛИРОВАННЫХ ЛАЗЕРНЫМ ИЗЛУЧЕНИЕМ
Гайнутдинова Р. Д.
ФГБУ «Всероссийский центр глазной и пластической хирургии Минздравсоцразвития России», г. Уфа
Впервые изучено влияние лазерного излучения на структуру соединительнотканных трансплантатов и их регенераторные свойства при пересадке животным. Установлено, что моделирование формы соединительнотканных трансплантатов с учетом их строения и подбором оптимального режима лазерной резки позволяет максимально сохранять структуру волокнистого остова трансплантатов и их регенераторные свойства. Разработан оптимальный режим лазерной резки для трансплантатов твердой оболочки головного мозга, дермы опорных участков стопы, мембранного трансплантата и подкожной жировой клетчатки, с учетом особенностей их архитектоники.
Актуальность Современный уровень развития восстановительной хирургии невозможно представить без реконструктивных хирургических вмешательств в сочетании с использованием соединительнотканных трансплантатов. В различных областях медицины (офтальмологии, челюстно-лицевой хирургии, стоматологии, отоларингологии, нейрохирургии, травматологии, ортопедии и т.д.) ведущая роль отводится трансплантатам аллогенного происхождения (Клен Р., 1962; Имамалиев А.С., 1970; Кристинов Г., 1975; Коваленко П.П., 1975; Говалло В.И., 1979; Зайкова М.В., 1982; Arndt K.A., 1982; Мирский М.Б., 1985; Брус И.Г. и др. 1989; Мулдашев Э.Р., 1994; Grover R., 1998; Емельянов В.А., 2000; Канюков В.Н. и др. 2001; Савельев В.И. и др. 2001; Канюков В.Н., Стадников А.А., 2009). Успех любой пластической операции с использованием аллотрансплантатов в значительной степени определяется качеством последних, которое, в свою очередь, зависит от совокупности стадий технологического процесса их изготовления. Поэтому совершенствование технологий изготовления и увеличение производства соединительнотканных трансплантатов является достаточно актуальной задачей.
В процессе изготовления трансплантатов особо важным является сохранение фиброархитектоники донорских тканей. При оптимальном методе изготовления соединительнотканных трансплантатов происходит разрушение клеточных элементов, но при этом сохраняется коллагеново–волокнистый остов (Seiffert K.K., 1970), который служит каркасом для формирования регенерата. Для достижения эффективного результата хирургической коррекции соединительнотканные трансплантаты должны обладать не только необходимыми биологическими свойствами, но и иметь определенную геометрическую форму. В технологическом процессе изготовления трансплантатов существует этап моделирования формы. Этап «выкраивания» трансплантатов традиционно осуществляется при помощи скальпеля, ножниц, трепана или штампа, так как для выполнения микрохирургических операций трансплантаты должны строго соответствовать заданным размерам. В лаборатории консервации тканей Всероссийского центра глазной и пластической хирургии предложен новый метод моделирования соединительнотканных трансплантатов при помощи углекислотного лазера. Для «выкраивания» трансплантатов используется комплекс лазерного моделирования, разработанный по проекту специалистов Всероссийского центра глазной и пластической хирургии в Российском ядерном центре (г. Саров). Данный комплекс предназначен для использования в медицине с целью автоматизации процесса изготовления различных трансплантатов, где лазер выполняет роль скальпеля и способен моделировать трансплантаты любой формы. Кроме того, лазерный луч благодаря монохроматичности, строгой направленности, когерентности и свойствам концентрировать большое количество энергии на малых площадях дает возможность реза различных биологических тканей без существенных повреждений (Стадников А.А. и соавт. 2001, 2005; Сетейкин А.Ю. и соавт. 2002., Москвин С.В., 2007). Степень и результат биологического действия лазерного излучения на различные ткани зависят не только от особенностей излучения (тип лазера, длительность и плотность мощности излучения, частоты импульсов и др.), но и от физико-химических и биологических особенностей облучаемых тканей (гетерогенность, теплопроводность, коэффициент поглощения и отражения различных промежуточных поверхностей внутри среды и др.) (Гамалея Н.Ф. и соавт. 1987).
Однако воздействие лазерного излучения на структуру соединительнотканных трансплантатов на сегодняшний день не изучено. В этой связи представляется актуальным исследование воздействия лазерного излучения на структуру трансплантатов с различной фиброархитектоникой, а также подбор режимов лазерного сечения для моделирования соединительнотканных трансплантатов, применяемых в различных областях хирургии.
Цель исследования
Морфологически обосновать возможность применения лазерной технологии при моделировании соединительнотканных трансплантатов.
Материалы и методы
Объектами исследования являлись соединительнотканные трансплантаты, изготовленные из следующих анатомических структур: твердой оболочки головного мозга, мембранного трансплантата, дермы опорных участков стопы, подкожной жировой клетчатки.
Донорские ткани обрабатывали и консервировали по технологии Аллоплант, разработанной во Всероссийском центре глазной и пластической хирургии г. Уфа (патент РФ №2189257). Данная технология заключается в следующем – донорский материал подвергали многоступенчатой физико-химической обработке, которая позволяет достигнуть мембранолиза и способствует экстракции наиболее иммуногенных компонентов тканей, с сохранением коллагенового каркаса.
Моделирование полученных соединительнотканных трансплантатов проводили с помощью комплекса лазерного моделирования, разработанного по проекту специалистов лаборатории консервации тканей ВЦГПХ в Российском Федеральном ядерном центре (г. Саров). Данный комплекс является программно-аппаратным устройством, предназначенным для автоматизированного изготовления материалов хирургического назначения из органов и биологических материалов. Комплекс лазерного моделирования (КЛМ) включает в себя лазерную установку, которая состоит из СО2–лазера с предельной мощностью лазерного излучения 100 Вт на длине волны 10,6 мкм и координатно-управляемую систему (КУС) прецизионного перемещения лазерного луча по плоской поверхности. СО2–лазер и КУС обеспечивают высокопроизводительную резку заготовок биологических тканей на заданные геометрические формы хирургических имплантатов. Установка снабжена автономной системой водяного охлаждения, телеметрической системой на основе цветной телекамеры высокого пространственного разрешения VEC–535, которая осуществляет визуализацию формы заготовок биологических тканей и определяет их геометрические размеры. Управление работой КЛМ производится с помощью компьютерной программы, установленной на ПЭВМ, которая управляет работой всех входящих в КЛМ систем, а также производит оптимальный раскрой заготовок биологических материалов на заданные формы трансплантатов.
Испытуемые образцы по способу изготовления (моделирования) разделили на две группы: контрольная – вырезаны трепаном, экспериментальная – вырезаны лазером. Форма всех образцов круглая -диаметр 10 мм. Для моделирования экспериментальных образцов использовали непрерывный и импульсный режимы работы лазера. Образцы были смоделированы при длине волны лазерного излучения 10,6 мкм. Мощность, скорость излучения и количество проходов лазерного луча подбирали опытным путем в зависимости от фиброструктуры и толщины ткани. Первоначально эффективность лазерного реза соединительнотканных трансплантатов оценивали макроскопически (отсутствием карбонизации по краю трансплантата), затем для подтверждения сохранности структуры проводили морфологические исследования трансплантатов. Подбор режима лазерной резки соединительнотканных материалов фиксировали в журнале.
Для изучения структуры соединительнотканных трансплантатов после воздействия лазерного излучения был использован комплекс морфологических методов.
Гистологические срезы окрашивали гематоксилином, эозином, фукселином по Вейгерту, орсеином по Унны-Тенцера и по Ван Гизону. Микроскопические исследования проводили с использованием световых микроскопов JENAVAL и AXIO IMAGER–Z1 (C.Zeiss, Германия). Микрофотосъемку осуществляли с помощью цифровой камеры Nicon D 100.
Для электронно-микроскопического исследования кусочки тканей фиксировали в 2,5% р-ре глютаральдегида, приготовленном на какодилатном буфере (рН 7,2-7,4) с последующей дофиксацией в 1% растворе OsO4. Материал обезвоживали в спиртах возрастающей концентрации и заливали в эпон-812 по общепринятой методике Б. Уикли (1975). Предварительно изготавливали полутонкие срезы толщиной 1 мкм и окрашивали их толуидиновым синим на 2.5%-ном растворе безводной соды. На данных срезах выбирали участки для электронно-микроскопического исследования. Срезы готовили на ультратоме LKB-III 8800 (Швеция). Ультратонкие срезы контрастировали 2% водным раствором уранилацетата, цитратом свинца по Рейнольдсу (Уикли Б., 1975) и изучали в трансмиссионных микроскопах JEM-7A и JEM-СХ II (Япония) при увеличениях от 4000 до 35000.
Структуру волокнистого остова и рельеф поверхности трансплантатов исследовали используя сканирующую электронную микроскопию. Для этого образцы проводили в спиртах возрастающей концентрации, в двух порциях 100% этанола, в двух порциях ацетона и высушивали с последующим напылением в ионно-распылительной установке слоем платины (Волкова О.В. и соавт., 1987г.) Микрофотографирование проводили на сканирующем микроскопе JSM–840 (Jeol, Япония) при увеличениях 500, 1000, 3000.
Рельеф поверхности трансплантатов изучали также с использованием метода импрегнации нитратом серебра по Минигазимову Р.С. (Патент РФ № 2270446 «Способ исследования рельефа поверхностей гистологических препаратов»). Суть метода заключается в импрегнации препаратов серебром с его полным восстановлением, что придает светоотражательную способность всем импрегнированным структурам. Препараты, исследовали с помощью микроскопа AMPLIVAL (C. Zeiss, Германия) с темнопольным эпиобъективом, позволяющим визуализировать объемную картину рельефа поверхности препарата. Микрофотосъемку препаратов проводили цифровой камерой Nicon Coolpix 4500.
Для оценки фиброархитектоники биоматериалов использовали способ количественного поляризационно-оптического анализа. В основе метода – способность волокнистых компонентов соединительной ткани к двойному лучепреломлению (Scheuner G., 1981; Wolman M., Kaster F.H., 1986). Проводили поляризационную микроскопию неокрашенных гистологических срезов толщиной 10 мкм с использованием микроскопа МИН–8 и цифровой фотонасадки Nicon Coolpix 4500 при скрещенных фильтрах.
Морфометрию структурного состояния краевой зоны трансплантата после моделирования трепаном или лазером исследовали с использованием метода количественной оценки относительной плотности волокнистых структур. Учитывая тот факт, что процесс моделирования предполагает рассечение ткани, то есть нарушение ее целостности, нами выявлены две зоны трансплантата: зона реза и интактная зона. При этом выполнялась световая микроскопия гистологических срезов, окрашенных по Ван Гизону с использованием микроскопа МС-50 (Micros, Австрия) с цифровой фотонасадкой Nicon Coolpix 4500. Полученные фотоснимки передавались с Flash-карты фотоаппарата в персональный компьютер для дальнейшей обработки. С помощью предварительно откалиброванной на объектив ×40 лицензионной программы Biovision Professional («Westmedica», Австрия) производилось измерение площади зоны препарата, находящейся в поле зрения. Волокнистые структуры и основное вещество регистрировались с помощью специальной функции программы – «сегментация», при заданном диапазоне яркости: 100÷200, при этом определялась их площадь и процентное соотношение. Площадь исследуемого участка составляла 40 тыс мкм2. Полученные результаты переводились в программу Microsoft Office Excel 2007, для устранения случайных значений. Затем обработанные данные переводились в программу Statistica 7.0.
Биомеханическим испытаниям подвергались следующие анатомические структуры: твердая оболочка головного мозга, мембранный трансплантат и дерма опорных участков стопы. В работе использовали методику определения «прочности шовной фиксации» (Нигматуллин Р.Т., 1996), а так же метод деформации препарата с постоянной скоростью (Егоров В.И. и др., 2004). Изучение биомеханических свойств трансплантатов проводили на универсальной машине для испытания прочностных свойств материалов модели 1185 INSTRON (Англия). Диапазон нагрузок от 0 до 100 Н (ньютонов), скорость перемещения траверсы от 0,005 до 250 мм/мин. Для механических испытаний из исследуемых биологических тканей изготавливали образцы, имеющие прямоугольную форму (20мм х 25мм). С помощью микрометра определяли толщину образцов. Образцы, изготовленные из твердой мозговой оболочки имели толщину – 1000 мкм , из дермы – 2500 мкм, из мембранного трансплантата –100 мкм. Один конец образца фиксировали в зажим разрывной машины, через свободный край ткани проводили 4 лигатуры, концы которых укрепляли в противоположном зажиме. В качестве лигатур использовали аллосухожильные нити толщиной 100-200 мкм. Толщина нитей зависела от типа трансплантата. В последующем образцы подвергали одноосному линейному растяжению. Прочностные свойства трансплантатов испытывали при постоянной скорости деформации – 2 мм/сек.
Статистический анализ полученных данных проводили используя методику, предложенную О.Ю. Ребровой (2002г.). Полученные результаты переводились в программу Microsoft Office Excel 2007. Затем обработанные данные переводили в программу Statistica 7.0.
Экспериментальные исследования по имплантации соединительнотканных трансплантатов, смоделированных разными способами, проводили на 36 кроликах породы «Шиншилла» обоего пола массой от 1,5-2 кг. Животных содержали в виварии, оборудованном согласно требованиям «Санитарных правил по устройству, оборудованию и содержанию экспериментально-биологических клиник (вивариев)» за № 1045-73. Исследования осуществляли в соответствии с правилами проведения работ и использования экспериментальных животных (Приложение к Приказу МЗ СССР № 775 от 12.08.77), «Европейской конвенцией о защите позвоночных животных, используемых для экспериментов или в иных научных целях» от 18 марта 1986г. и Федерального закона РФ «О защите животных от жестокого обращения» от 01.01.1997г. Животные оперировались под кетаминовым наркозом (в отдельный шприц: кетамин 2 мл (внутримышечно) + дроперидол 1 мл (внутримышечно). Техника операции заключалась в следующем. В верхнем секторе глазного яблока трепаном иссекался участок коньюнктивы диаметром 10 мм. Мембранный трансплантат для экспериментальной группы моделировался при помощи лазера (диаметром 10 мм) и вручную трепаном (диаметр 10 мм), затем укладывался на оголенную поверхность склеры. Фиксация трансплантата производилась узловатыми швами, которые проводились через коньюнктиву, эписклеру и трансплантат. В послеоперационном периоде ежедневно 3 раза в день в конъюнктивальную полость инстиллировали 0,25% раствор левомицетина.
Трансплантаты с окружающими тканями коньюнктивы глазного яблока были изучены гистологическими и электронно-микроскопическими методами в различные сроки после операции. Через 7, 14, 21, 30, 60, 180 суток после операции животных выводили из опыта передозировкой наркоза.
Результаты исследований и их обсуждение
Проведенные морфологические исследования позволили проанализировать зависимость структурных изменений различных видов соединительнотканных трансплантатов при лазерном моделировании от их фиброархитектоники.
Так, трансплантаты твердой оболочки головного мозга, представляющие собой многослойную плотную соединительнотканную пластинку, в зоне реза трепаном выраженных повреждений не имеют. Наблюдается лишь незначительное продольное расщепление пучков коллагеновых волокон в месте сечения. Морфометрические исследования демонстрируют небольшое снижении плотности волокнистых структур в краевой зоне, а именно: показатель плотности волокнистых структур интактного участка составляет 53,7±3,32%, аналогичный показатель трансплантатов, моделированных трепаном соответствует 43,4±2,07%. Общая фиброструктура трансплантата, состоящая из плотных, параллельно лежащих пучков коллагеновых волокон и рыхлой сети эластических волокон, сохраняется полностью. Исследование экспериментальных образцов показало следующее: у трансплантатов ТМО по линии лазерного реза наблюдаются слабовыраженные деструктивные изменения в виде частичной гомогенезации пучков коллагеновых волокон. Максимальная ширина зоны деструкции достигает 4 мкм. Морфометрия краевой зоны трансплантатов, моделированных лазером, демонстрирует уплотнение волокнистых структур и уменьшение межпучкового пространства в зоне реза. Структура самого трансплантата остается сохраненной. Биомеханические исследования трансплантатов ТМО на прочность «шовной фиксации» показывают, что предел прочности контрольных образцов на 0,300 МПа выше экспериментальных, относительное удлинение контрольных образцов на 0,35% ниже экспериментальных, значение модуля упругости контрольных образцов выше аналогичного значения экспериментальных образцов на 0,341 МПа. Полученные данные свидетельствуют о том, что воздействие лазерного излучения на трансплантат практически не меняет его прочностных качеств для «шовной фиксации».
Проведенные морфологические исследования фиброархитектоники трансплантатов дермы опорных участков стопы показали, что в контрольных образцах данного трансплантата повреждений в зоне реза не наблюдается. Разнонаправленность коллагеновых и эластических волокон по линии реза сохраняется. При исследовании краевой зоны трансплантатов дермы, изготовленных при помощи лазера, наблюдается следующая картина: по линии прохождения лазерного луча образуются очаговые деструктивные изменения, ширина которых достигает 4-6 мкм. Выявленные локальные изменения в виде набухания коллагеновых волокон по линии реза не приводят к изменениям в целом фиброархитектоники трансплантата. Морфометрические данные подтверждают повышение плотности волокнистых структур по линии лазерного реза в 2 раза по сравнению с аналогичным показателем для трансплантатов, моделированных трепаном. Высокие пластические свойства трансплантатов дермы обусловлены особенностями ее фиброархитектоники, для которой характерен пространственный коллагеново-волокнистый остов, образованный разнонаправленными, извилистыми, способными к растяжению волокнами. Биомеханические испытания трансплантатов ДП на «прочность шовной фиксации» демонстрируют увеличение в 1,5 раза значения предела прочности и модуля упругости трансплантатов, моделированных лазером.
Сравнительный анализ структуры мембранных трансплантатов показал, что в образцах изготовленных вручную трепаном наблюдается незначительное продольное расщепление пучков коллагеновых волокон по линии реза, что не нарушает фиброархитектонику самой ткани в целом. Изучение экспериментальных образцов данного трансплантата выявило лишь очаговое набухание коллагеновых волокон в зоне прохождения лазерного луча (ширина зоны до 2 мкм), которое также не влияет на структуру самого трансплантата в целом. Морфометрический анализ показал, что плотность волокнистых структур трансплантатов ФКП в зоне лазерного реза почти в 2 раза выше аналогичного показателя образцов, моделированных трепаном. Биомеханические исследования краевой зоны трансплантатов ФКП демонстрируют сохранение прочностных свойств. Прочностные параметры трансплантатов ФКП, моделированных лазером идентичны аналогичным показателям трансплантатов ФКП, изготовленных трепаном, а именно: для контрольных образцов предел прочности составляет - 2,000±0,333 МПа, относительное удлинение - 1,272±0,225%, модуль упругости - 1,620±0,317 МПа; для экспериментальных образцов предел прочности - 2,050±0,369 МПа, относительное удлинение - 1,182±0.009%, модуль упругости - 1,688±0.282 МПа.
Сравнивая данные морфологических исследований структуры трансплантатов подкожной жировой клетчатки, изготовленных трепаном вручную и образцов, прошедших этап лазерного моделирования можно сказать следующее: ячеистость структуры трансплантата в обеих группах сохраняется, незначительные изменения претерпевают края образцов. В контрольных образцах жировые ячейки с оболочками и тяжи коллагеновых и эластических волокон рассечены по линии реза без изменения их структуры. В экспериментальных образцах по линии реза наблюдаются небольшие деструктивные изменения, которые имеют мозаичный вид. Максимальная ширина очаговой деструкции достигает 2 мкм. В целом фиброструктура трансплантата ЖК, моделированного лазерным лучом сохраняется. Морфометрическая оценка краевой зоны данного трансплантата следующая: плотность волокнистых структур по линии лазерного реза в 2 раза выше плотности волокнистых структур трансплантатов ЖК, моделированных трепаном.
Моделирование трансплантатов с подбором оптимального режима лазерной резки позволяет максимально сохранить структуру волокнистого остова исследуемых соединительнотканных биоматериалов. А.А. Стадниковым и соав., (2001, 2005) была проведена сравнительная морфометрическая оценка состояния стромальных элементов трансплантатов аорты и ТМО при выкраивании данных трансплантатов при помощи хирургического СО2-лазера, гидроножа и трепана. Указанными авторами отмечается, что наименьшие отклонения в структуре волокнистых компонентов соединительнотканных трансплантатов наблюдается при использовании лазерной технологии.
Изменения структуры трансплантатов по линии лазерного реза на наш взгляд - это суммарный конечный фотобиологический эффект, который формируется в результате процессов, возникающих непосредственно в самом объеме облученной ткани. Известно, что наиболее значительные повреждения возникают при поглощении первых 63% проходящей лазерной энергии (Богданович У.Я. и соавт., 1978; Плужников М.С., 2000). Выбор режима лазерного моделирования, позволяющего достигать оптимальный результат, в значительной степени определяется хромофорами ткани - молекулами, способными поглотить излучение и превратить его в тепло. Эффект воздействия зависит от соотношения целевых и конкурирующих хромофоров ткани (Москвин С.В., 2007, Пушкарева А.Е., 2008). Целевыми хромофорами для излучения СО2-лазера являются молекулы воды. Так, при 100 оС молекулы воды, содержащиеся в большинстве тканей, начинают испаряться, сильно увеличиваться в объеме, формируются газовые пузыри. Это, в свою очередь, приводит к повышению давления и вызывает механические разрушения и деструкцию ткани. Так формируется лазерный рез (Елисеенко В.И., 1989; Плужников М.С., 2000; Пушкарева А.Е., 2008). Наличие и количество молекул воды в составе основного вещества, в которое погружены пучки коллагенновых волокон, на наш взгляд, тоже являются слагаемым эффективного лазерного реза соединительнотканных трансплантатов. Основное вещество представляет собой оптически прозрачную гелеобразную субстанцию различной степени вязкости, невидимую на обычных гистологических срезах. Компонентами основного вещества являются углеводно-белковые комплексы (Слуцкий Л.И., 1969; Серов В.В., Шехтер А.Б., 1981; Ноздрин В.И. и соавт., 2005). Наиболее полно изучены углеводные компоненты этих соединений – гликозаминогликаны (ГАГ). ГАГи имеют несколько разновидностей, которые отличаются друг от друга химической структурой, степенью сульфатированности и молекулярной массой. Наибольшую величину молекул имеет гиалуроновая кислота. Молекулы гликозаминогликанов гидрофильны, связывают большое количество молекул воды и ионов, входящих во внеклеточную жидкость (Слуцкий Л.И., 1969; Серов В.В., Шехтер А.Б., 1981).
Во избежание нежелательной коагуляции, нами для каждого вида соединительнотканных трансплантатов подбирался оптимальный режим лазерного моделирования: режим импульса, мощность, частота, скорость и количество проходов лазерного луча. Кроме того, для охлаждения места воздействия применялось локальное орошение и обдув зоны лазерного реза.
Изменение фиброструктуры соединительнотканных трансплантатов после воздействия лазерного излучения зависит, на наш взгляд, от следующих факторов: 1) от пространственной ориентации и толщины пучков коллагеновых волокон; 2) от количества слоев пучков коллагеновых волокон, а также толщины моделируемой ткани; 3) количественного и качественного состава основного вещества. В зависимости от того, на сколько плотно располагаются пучки коллагеновых волокон и сколько слоев имеет ткань, определяется толщина поглощающего слоя, рассчитываются параметры лазерного излучения.
Полученные данные позволяют сделать следующие заключения. У изучаемых нами соединительнотканных трансплантатов, изготовленных из твердой оболочки головного мозга и дермы опорных участков стопы, выявленные изменения структуры зоны лазерного реза идентичны. В трансплантатах ТМО при относительно небольшой толщине (1 мм), плотном расположении пучков коллагеновых волокон, а также многослойности - доля основного вещества невысокая (Валишина А.Д., 1979; Улумбеков Э.Г., 1998; Омельяненко Н.П., Слуцкий Л.И., 2010). Чередование слоев пучков коллагеновых волокон и основного вещества приводит к образованию очаговых зон деструкции, то есть, лазерный луч, попав в плотную зону наложения друг на друга слоев пучков коллагеновых волокон, рассекая ткань разогревает ее и вызывает термическую деструкцию. В зоне основного вещества лазерный луч попадает в молекулы воды и без повреждений рассекает ткань. Поэтому в данных участках выраженные очаги деструкции отсутствуют.
Аналогичная картина наблюдается и в трансплантатах дермы опорных участков стопы, основная масса которых – коллагеновые волокна, образованные ими переплетающиеся пучки коллагеновых волокон, оплетенные сетью эластических волокон и небольшое количество основного вещества (Мулдашев Э.Р. и соавт., 1981; Нигматуллин Р.Т., 1996; Ноздрин В.И. и соавт., 2005; Кошевенко Ю.Н., 2006; Омельяненко Н.П., Слуцкий Л.И., 2010). Исследования зоны реза трансплантата дермы показывают, что здесь деструкция также имеет очаговый характер, то есть участки гомогенизированных коллагеновых волокон чередуются с участками волокон с сохраненной структурой. Ширина термической деструкции достигает 4-6 мкм. Мы предполагаем, что структурные изменения носят очаговый характер из-за хаотичного расположения волокнистых элементов, не имеющих какой-либо геометрической последовательности, а именно под действие лазерного излучения попадают пучки коллагеновых волокон П и Ш порядка, расположенные друг над другом. Участки, расположенные между коллагеновыми волокнами и заполненные основным веществом, термической деструкции не подвергаются.
Анализируя фиброархитектонику мембранных трансплантатов можно сказать, что они образованы волокнистой соединительной тканью, состоящей из двух слоев: наружного слоя - тонкого, состоящего из плотно лежащих коллагеновых волокон, образующих единый пласт и внутреннего слоя более объемного с множеством разнонаправленных коллагеновых волокон, пучков коллагеновых волокон I порядка, имеющих рыхлую бессистемную организацию (Слуцкий Л.И., 1969; Сорокин А.П., 1973; Шангина О.Р., 2007). Особенная структура ткани (двуслойность), высокий уровень гидратации внутреннего слоя и малая толщина трансплантата (0,1 мм) дали соответствующие результаты. Предполагаем, что незначительные структурные изменения возникают в наружном слое трансплантата ФКП, который имеет более плотную структуру, состоящую из компактно расположенных тонких пучков коллагеновых волокон с характерной для них хаотичностью и извитостью. Отсутствие нарушений в структуре внутреннего слоя, на наш взгляд, объясняется рыхлой организацией волокон и концентрацией основного вещества в данном слое.
Жировая ткань, с точки зрения оптических свойств, представляет собой неоднородную среду, способную поглощать, отражать и рассеивать излучение (Пушкарева А.Е., 2008). Фиброструктура трансплантата, изготовленного из подкожной жировой клетчатки, представлена крупными жировыми дольками, окруженными коллагеново-эластическими оболочками, а также соединительнотканными тяжами, состоящими из плотноупакованных коллагеновых пучков Ш порядка и сети эластических волокон (Кошевенко Ю.Н., 2006). Жировые ячейки содержат легкоплавкие жиры - триглицериды (температура плавления 15 оС). Известно, что при расщеплении легкоплавких жиров образуется вода, поэтому жировую клетчатку можно рассматривать как депо связанной воды. (Ноздрин В.И. и соавт., 2005). Толщина трансплантата ЖК составляет 5-7 мм. В результате лазерного воздействия ячеистость структуры трансплантата подкожной жировой клетчатки по линии реза сохраняется, но наблюдаются очаговые фрагменты коагуляции, расположенные, как правило, в зоне прохождения пучков коллагеновых волокон. Мы предполагаем, что молекулы воды, которые в жировых дольках содержатся в избытке, дают возможность лазерному лучу беспрепятственно рассекать жировые дольки и лишь пересекая плотные соединительнотканные коллагеновые тяжи лазерный луч вызывает слабую деструкцию в зоне их расположения.
Деструктивных изменений эластических волокон, связанных с воздействием лазерного луча мы не наблюдали. Очевидно, это связано с тем, что эластические волокна устойчивы к высоким температурам (Слуцкий Л.И., 1969).
Сохранение пластических свойств соединительнотканных трансплантатов является важным фактором, обуславливающим эффект их клинического применения. После пересадки в организме трансплантаты должны временно или постоянно выполнять различного характера механические нагрузки. Поэтому имплантированные биоматериалы должны обладать адекватными упруго-деформативными свойствами (Кардапольцева Г.В., Дунаева В.Г., 1975; Пуриня Б.А. и др. 1980; Нигматуллин Р.Т., 1996; Шангина О.Р., 2007 и др.). Данные, полученные в результате биомеханических испытаний «на прочность шовной фиксации» подтверждают, что упруго-прочностные свойства трансплантатов, моделирование формы которых было произведено при помощи лазерного луча не изменились, а у трансплантатов дермы опорных участков стопы наблюдалось даже увеличение биомеханических параметров в 1,5 раза по сравнению с контрольными образцами.
Полученные нами результаты морфометрических исследований краевой зоны трансплантатов демонстрируют уплотнение волокнистых структур по краю лазерного реза у всех исследуемых трансплантатов, что в свою очередь приводит к увеличению прочностных свойств трансплантатов Данные по изменению плотности волокнистых структур в краевой зоне представлены в таблице 8.
| Виды трансплантатов | Трансплантаты, моделированные трепаном | Трансплантаты, моделированные лазерным лучом |
|---|---|---|
| TMO | 43,4±2,07 | 74,7 ±10,41 |
| ДП | 49.1±2,33 | 96,5±1,78 |
| ФКП | 31,2±3,26 | 80,3±5,92 |
| ЖК | 14,1±2,02 | 27,8±3,22 |
При обезвоживании, лишении ткани молекул воды по линии лазерного реза, наблюдается эффект сморщивания, т.е. происходит сближение пучков коллагеновых волокон. Результаты наших исследований находят подтверждение в работах других авторов. По данным исследований, проведенных А.М. Хилькиным, А.Б. Шехтером и др. (1976), в обезвоженных коллагеновых пленках наблюдается возникновение случайных связей между наиболее близко расположенными агрегатами макромолекул коллагена, в результате чего коллагеновые пленки в сухом состоянии (лишенные воды) обладают значительной прочностью при растяжении. Происходит увеличение межмолекулярного сцепления в структуре коллагена. По нашему мнению, повышение прочности края трансплантата ДП, происходит за счет «спаивания-склеивания» коллагеновых волокон по краю трансплантата. Очевидно, происходит некая «структурная сшивка» волокон, что в итоге позволяет обеспечить более надежную шовную фиксацию трансплантата.
Анализируя полученные морфологические данные по фиброархитектонике, результаты морфометрии по состоянию волокнистых структур краевой зоны, данные по биомеханическим свойствам соединительнотканных трансплантатов, а также проведя ряд опытных исследований, можно сказать, что подобранные нами режимы лазерного моделирования являются оптимальными.
Для подтверждения сохранности регенераторных свойств соединительнотканных трансплантатов при лазерном моделировании в оптимальном режиме нами были проведены исследования по имплантации на животных.
Полученные результаты экспериментальных исследований свидетельствуют о том, что пересаженные на конъюнктиву глаза кролика трансплантаты, моделированные трепаном и лазерным лучом, постепенно в течение месяца резорбируются макрофагами и замещаются полноценным соединительнотканным регенератом. Динамика замещения биоматериалов по морфологической картине в обеих опытных группах и на всех сроках эксперимента идентична.
Результаты гистологических и электронно-микроскопических исследований показали, что уже через месяц после имплантации на конъюнктиву глазного яблока кроликов трансплантатов ФКП в обеих опытных группах выявились все признаки полного замещения трансплантатов. Пучки коллагеновых волокон в регенерате располагались гораздо плотнее, чем в соединительнотканной пластинке конъюнктивы в норме, но при этом новообразованная ткань была пронизана относительно большим количеством тонкостенных сосудов, характерных для соединительнотканной пластинки конъюнктивы. Через 60 суток структура регенерата уже полностью соответствовала окружающей ткани конъюнктивы, то есть была представлена васкуляризированной рыхлой соединительной тканью. В течение второго месяца цикл ремоделирования новообразованной ткани завершился полностью.
Выявленная схема процесса замещения трансплантата новообразованной тканью полностью укладывается в рамки уже изученного механизма действия аллогенных трансплантатов (Мулдашев Э.Р. 1994, Муслимов С.А. 2000, Мусина Л.А. 2007). Установлено, что процесс постепенной резорбции аллогенного трансплантата макрофагами и стимуляция последних продуктами деструкции трансплантата усиливает их влияние на структуру формирующейся ткани на месте трансплантации и индуцирует полноценную регенерацию тканей с формированием в ней всех составных элементов.
Таким образом, полученные результаты экспериментального исследования показывают, что использованные нами способы моделирования соединительнотканных трансплантатов для пластики конъюнктивы глазного яблока не оказывают отрицательного влияния на процессы их замещения и на регенерацию тканей.
Заключение
В заключении представляется целесообразным выделить некоторые преимущества моделирования соединительнотканных трансплантатов при помощи лазерного излучения.
Использование комплекса лазерного моделирования обеспечивает суперточную, высокопроизводительную резку биологических тканей на заданные геометрические формы, исключает загрязнение самой ткани, что особенно важно при выполнении микрохирургических операций и в совокупности позволяет обеспечить конечный эффективный результат хирургической коррекции.
При моделировании соединительнотканных трансплантатов трепаном в зоне реза наблюдается небольшое продольное расщепление пучков коллагеновых волокон, некая «бахромчатость», чего не происходит при выкраивании лазерным лучом. Кроме того, «структурная сшивка» коллагеновых волокон по краю трансплантата дермы приводит к повышению его пластических свойств, которые имеют значение при шовной фиксации краев трансплантата.
Моделирование формы трансплантатов с подбором оптимального режима лазерной резки и учетом особенностей фиброархитектоники различных соединительнотканных трансплантатов позволяет максимально сохранить их структуру и не оказывает отрицательного влияния на процессы замещения и регенерации тканей при пересадке.
Изменение структуры соединительнотканных трансплантатов, после воздействия лазерного излучения зависит от особенностей фиброархитектоники самой ткани, то есть пространственной ориентации коллагеновых волокон и толщины их пучков, количества слоев пучков коллагеновых волокон в ткани. Чем тоньше пучки коллагеновых волокон, шире межпучковые пространства и меньше толщина моделируемой ткани, тем менее выражены деструктивные изменения в зоне лазерного реза.
Моделирование формы при помощи трепана приводит к продольному расщеплению пучков волокон по линии реза у всех исследуемых соединительнотканных трансплантатов. При лазерном моделировании в зоне реза наблюдается минимальная очаговая деструкция пучков коллагеновых волокон, ширина которой варьирует от 2 до 6 мкм (для трансплантатов твердой оболочки головного мозга – 2-4 мкм, для трансплантатов дермы опорных участков стопы – 4-6 мкм, для мембранных трансплантатов – 1-2 мкм, для трансплантатов подкожной жировой клетчатки – 1-2 мкм). Деструктивные изменения в зоне лазерного реза сопровождаются уплотнением волокнистых структур соединительнотканных трансплантатов.
Биомеханические исследования подтверждают сохранение фиброархитектоники трансплантатов, моделированных лазерным лучом. Так, показатели прочности «шовной фиксации» краевой зоны трансплантатов твердой оболочки головного мозга и мембранного трансплантата не изменяются, для трансплантатов дермы опорных участков стопы - возростают в 1,5 раза по сравнению с контролем, что связано с высокой плотностью пучков коллагеновых волокон, которые в зоне реза подвергаются «структурной сшивке», обеспечивающей укрепление краевой зоны трансплантата.
При экспериментальной пересадке соединительнотканные трансплантаты, моделированные лазерным лучом, постепенно резорбируются макрофагами и замещаются полноценным соединительнотканным регенератом.
Одним из факторов, определяющих характер структурных изменений в трансплантате при моделировании, является мощность и скорость лазерного излучения. Опытным путем для каждого вида ткани разработан оптимальный режим лазерной резки, а именно: для трансплантатов твердой оболочки головного мозга - мощность 10Вт и скорость 3,5см/сек, в один проход лазерного луча; для трансплантатов дермы опорных участков стопы – мощность 30Вт и скорость 10см/сек, в один проход лазерного луча; для мембранных трансплантатов – мощность 10Вт и скорость 7см/сек, в три прохода лазерного луча; для подкожной жировой клетчатки – мощность 10Вт и скорость 7см/сек, в шесть проходов лазерного луча.
Литература
- Шангина О.Р., Гайнутдинова Р.Д. Лазерное моделирование трансплантатов для офтальмохирургии // Материалы научно-практической конференции Московского НИИ глазных болезней имени Гельмгольца. – Москва, 2008. - С. 89-91.
- Шангина О.Р., Гайнутдинова Р.Д. Лазерное моделирование соединительнотканных трансплантатов // Морфология, 2008. Т.133, №2. –С.153.
- Шангина О.Р., Гайнутдинова Р.Д., Хусаинова Л.Р. Влияние лазерного излучения на структуру соединительнотканных трансплантатов //Материалы Всероссийской конференции с международным участием. – Самара, 2008. -С.125-127.
- Гайнутдинова Р.Д. Применение лазерного излучения для моделирования соединительнотканных трансплантатов //Морфология, 2008. Т.133, №4. –С.62.
- Шангина О.Р., Гайнутдинова Р.Д. Сравнительная гистологическая характеристика структурных изменений различных соединительнотканных трансплантатов при воздействия лазерного излучения // Морфология, 2008. Т.133, №4. –С.103.
- Гайнутдинова Р.Д., Шангина О.Р. Морфологические изменения различных соединительнотканных трансплантатов после воздействия лазерного излучения //Морфологические ведомости, 2009. №3.–С.52-53.
- Мулдашев Э.Р., Нигматуллин Р.Т., Галимова В.У., Шангина О.Р. Гайнутдинова Р.Д., Гайфуллин С.Н., Мухаметов А.Р. Инновационные технологии в хирургии – альянс творчества и стандартизации // Материалы IV Межрегиональной научно-практической конференции «Метрология и инженерное дело в медико-биологической практике». – Оренбург, 2009. –С.60-62.
- Шангина О.Р., Хасанов Р.А., Лапчик Д.Р., Гайнутдинова Р.Д. Стандартизация деятельности тканевого банка ALLOPLANT ® //Материалы IV Межрегиональной научно-практической конференции «Метрология и инженерное дело в медико-биологической практике». – Оренбург, 2009. –С.88-90.
- Шангина О.Р., Гайнутдинова Р.Д., Кадыров Р.З. Применение лазерного излучения в процессе изготовления аллотрансплантатов для офтальмохирургии //Вестник Оренбургского Государственного Университета, 2009, №12. –С.157-159.
- Гайнутдинова Р.Д. Применение лазерных технологий в процессе изготовления трансплантатов // Материалы IV Всероссийского симпозиума «Актуальные вопросы тканевой и клеточной трансплантологии». –Санкт-Петербург, 2010. –С.46-47.
- Шангина О.Р., Гайнутдинова Р.Д. Морфологические исследования аллотрансплантатов фиброзной капсулы почки при экспериментальной пересадке // Морфология, 2010. Т.137, №4. –С.216-217.
- Шангина О.Р., Гайнутдинова Р.Д., Мусина Л.А, Муслимов С.А., Булгакова Л.А. Имплантация аллотрансплантатов моделированных разными способами на коньюнктиву глазного яблока. //Вестник Оренбургского Государственного Университета, 2010, №12. –С.236-238.
к содержанию | опубликовать статью
СТИМУЛЯЦИЯ РЕГЕНЕРАТОРНЫХ ПРОЦЕССОВ В ПОСЛЕОПЕРАЦИОННОЙ РАНЕ С ИСПОЛЬЗОВАНИЕМ АЛЛОГЕННОГО БИОМАТЕРИАЛА И ЭНЕРГИИ ЛАЗЕРНОГО ЛУЧА
Пантелеев В.С.
ГБОУ ВПО «Башкирский государственный медицинский университет Министерства здравоохранения и социального развития Российской Федерации»
Впервые использован аллогенный биоматериал с целью коррекции морфогенеза в процессе заживления ран, изучена морфология раневого процесса, состояние микроциркуляции и насыщения кислородом тканей в зоне раневых изменений при сочетанном применении аллогенного биоматериала и энергии лазерного излучения. Разработан метод введения аллогенного биоматериала в ткани области раны. Разработана методика лазерной шлифовки келоидных и гипертрофических рубцов с последующей коррекцией ранозаживления используя аллогенный биоматериал.
Актуальность Проблема патогенеза и лечения ран относится к числу наиболее важных разделов хирургии. Постоянное внимание к этой проблеме объясняется, прежде всего, тем, что представления о раневом процессе постоянно меняются вместе с развитием медицины, биологии и технических наук. Однако важнейшим положением о ране остается незыблемый факт общности биологических законов заживления раны любого генеза и локализации. Этот очевидный вывод определяет общность объективных критериев, оценки течения раневого процесса и принципиальных основ патогенетического лечения ран (М.И. Кузин, Б.М. Костюченок 1990). Существует множество разнообразных методов и способов лечения ран. Разработка и широкое внедрение их в клинику, обсуждение на различных хирургических форумах позволили признать приоритет метода активного хирургического лечения ран. В тоже время в соответствии с запросами практической хирургии возникает необходимость разработки и теоретического обоснования новых, более эффективных способов управления процессом заживления ран, созданию более оптимальных условий образования нежного и подвижного послеоперационного рубца, надежного в функциональном и косметическом от ношении (Ефимов Е.А., 1975, Воздвиженский И.С., 2001). По данным разных авторов от 25 до 60% больных, оперированных по поводу рубцовых деформаций, нуждаются в повторных операциях вследствие патологического рубцевания в послеоперационном периоде. От 4,2 до 16% случаев раны заживают путем формирования келоидного рубца. В результате заживления ран путем формирования грубых рубцов возникают определенные трудности. Грубые рубцы в области суставов приводят к нарушению функции и, как следствие этого, к снижению трудоспособности. Образование келоидных рубцов на видимых участках тела доставляет чувство дискомфорта в косметическом отношении. Даже самая высокая хирургическая техника не исключает образования в послеоперационном периоде деформирующего келоидного или гипертрофического рубца. По-видимому, максимальный лечебный эффект может быть достигнут лишь при учете многих обстоятельств: например, закономерностей патогенеза раневого процесса и индивидуальных особенностей организма больного. В связи с вышесказанным, поиск наиболее эффективных методов лечения ран продолжается (Горячев А.Н., 1990, Мулдашев Э.Р., 1997). Весьма перспективным направлением в этом поиске является разработка и внедрение в практику лечения новых препаратов, а также разработка и внедрение наиболее эффективных способов комбинированного лечения послеопера ционных ран любой локализации. Попытка получить более лучшие результаты в этих направлениях и легла в основу настоящего исследования.
Цель работы
Целью настоящего исследования является улучшение результатов лечения послеоперационных ран и профилактика келоидообразования, применяя в комплексе аллогенный биоматериал и энергию лазерного излучения.
Материалы и методы исследования
В работе проводится анализ лечения чистых послеоперационных ран у 120 больных, оперированных по поводу различных заболеваний. Среди них 62 женщины и 58 мужчин. Все больные были разделены на три группы.
Первая — контрольная. В первой группе при иссечении рубца использовался хирургический скальпель.
Во второй применяли диспергированный аллогенный биоматериал "Стимулятор регенерации" производства Лаборатории консервации тканей ФГБУ ВЦГПХ Минздравсоцразвития России, а для иссечения и шлифовки рубцов использовался хирургический лазер.
В третьей группе совместно с биоматериалом использовали лазерное излучение. Отдельно проведен анализ лечения 50 больных с келоидными и гипертрофическими рубцами, среди которых 27 женщин и 23 мужчины.
Для оценки послеоперационной раны использовались общепринятые методы обследования: осмотр, пальпация, перкуссия, методы лабораторного исследования.
Использовали следующие специальные методы обследования :
- Цитологическое исследование проводили по методу М.П. Покровской и М.С. Макарова (1942). Полученные мазки-отпечатки высушивали и фиксировали в смеси Никифорова с последующим окрашиванием по Романовскому-Гимзе.
- Морфологические исследования проводили на биопсийном материале, взятым пункционным способом в различные сроки лечения (3—4,6-7,11-12 сутки).
- Микробиологические исследования включали в себя качественное и количественное определение микроорганизмов путем посева на питательные среды.
- Для регистрации кожного кровотока в области раны использовали лазерный анализатор капиллярного кровотока ЛАКК-01, изготавливаемый НПП «ЛАЗМА» (г. Москва).
С помощью данного метода возможно проводить:
- Мониторинг состояния капиллярного кровотока и запись полученных данных в память компьютера, т.е. наблюдать в реальном масштабе времени изменения кровотока.
- Просмотр, редактирование, вычисление статистических характеристик показателей микроциркуляции, запись данных пациентов, диагноза, заключения.
- Амплитудно-частотный анализ колебаний и выявление гемодинамических ритмов кровотока.
Лазерная доплеровская флоуметрия (ЛДФ) позволят проводить неинвазивный контроль состояния микроциркуляции в реальном масштабе времени. ЛДФ основана на регистрации частотной характеристики лазерного луча, отраженного от движущихся компонентов крови, в основном эритроцитов. Изменения частоты отраженного лазерного излучения (эффект Доплера) прямо пропорционально скорости движения клеток крови в измеряемом объеме тканей (1-1,5мм3). Величина показателя микроциркуляции (ПМ), или перфузии крови, измеряется в условных единицах и пропорциональна скорости движения эритроцитов (Уэ), величине гематокрита (Ht) в микрососудах и количеству функционирующих капилляров (Nk) в исследуемом участке кожи:
IIM=Vэ*Ht*Nk
Исследование проводили после двадцатиминутной адаптации пациента в положении лежа на спине при температуре помещения 20-22°С. На кожу исследуемой области с помощью адгезивного кольца крепится датчик анализатора, в котором закреплен зонд, дополнительно фиксируемый в определенном статистическом положении при помощи штатива. Исходный кровоток характеризует состояние микроциркуляторного русла в покое и выражается в перфузионных единицах. Его регистрация проводится не менее 1 минуты.
Программное обеспечение анализатора ЛАКК-01 позволяет проводить спектральный анализ амплитудно-частотных составляющих колебаний кровотока. Программа машинной обработки результатов исследования позволяет анализировать особенности амплитудно-частотной характеристики доплерограмм. На основе выявленных особенностей В.И. Козловым предложена физиологическая классификация его нарушений: физиологическая норма, спастическая, спастикоатоническая, застойная и стазическая формы.
Возможности ЛДФ:
1. Оценка состояния микрососудов и кровотока в ране.
2. Диагностика расстройств микроциркуляции в патологическом очаге.
3. Наблюдение динамики микроциркуляции в ране в процессе проводимого лечения.
Для оценки состояния насыщения тканей кислородом в области краев раны использовали транскутанный оксимонитор ТСМ-2 фирмы «Radiomen) (Дания). Парциальное давление кислорода в тканях определяли на 3-, 7-, 12-е сутки после операции.
Результаты исследований и их обсуждение
Лечение послеоперационных ран
Традиционным способом лечилось 40 больных. Контрольная группа состояла из 20 женщин и 20 мужчин. Все 40 больных были оперированы в плановом порядке по поводу различных заболеваний брюшной полости и передней брюшной стенки. Рассечение кожи и подкожной клетчатки производилось обычным хирургическим скальпелем. После окончания основного этапа операции производилось послойное ушивание послеоперационной раны. Ежедневно проводились перевязки с обработкой краев послеоперационной раны 70° этиловым спиртом. Специального лечения, направленного на улучшение регенерации в ране, больные данной группы не получали. Швы с послеоперационной раны снимались на 8-10-е сутки. На 5-е сутки в ране имели место явления отека и начинали появляться грануляции. К 10 суткам рана заполнялась грануляциями и появлялась краевая эпителизация.
При лечении послеоперационных ран традиционным способом имеется снижение нейтрофильных лейкоцитов и флоры только к 11-12 суткам. Появление фибробластов и эпителия происходит на 5-6-е сутки.
При морфологическом исследовании биоптатов, взятых с краев послеоперационной раны, на 3-4 сутки традиционного лечения, отмечалось инфильтрирование тканей полинуклеарами, единичными макрофагами и лимфоцитами.
На 5-6 сутки при гистологическом исследовании в области краев после операционной раны появляются немногочисленные островки грануляционной ткани типичного строения, обильно инфильтрированные нейтрофилами. В инфильтрате имеются талинуклеары, макрофаги, гистиоциты, лимфоциты и плазматические единичные клетки.
На 11-12 сутки традиционного лечения послеоперационных ран имело место развитие грануляционной ткани в полном объеме и появление краевой эпителизации.
При оценке состояния микроциркуляции в зоне раневых изменений получили следующие результаты (табл. 1).
| Сроки наблюдения | Параметры микроциркуляции | |||||
|---|---|---|---|---|---|---|
| ПМ | СКО | Cv | Fv | Av | Ст | |
| Исходные данные | 10,2±1,2 | 10,2±1,2 | 9,8±1,3 | 4,0±0,1 | 1,4±0,2 | 12,1±0,8 |
| 3-4 сутки | 4,8±1,1 | 1,9±0,5 | 7,2±0,9 | 2,5±0,3 | 0,7±0,1 | 9,4±0,1 |
| 6-7 сутки | 6,9±0,9 | 2,2±0,3 | 8,1±0,6 | 3,1±0,5 | 1,1±0,1 | 10,7±0,3 |
| 11-12 сутки | 9,8±1,1 | 2,0±0,2 | 9,6±1,1 | 3,8±0,4 | 1,5±0,1 | 11,9±0,4 |
Лечение с применением аллогенного биоматериала получали 40 больных: 19 мужчин и 21 женщина. Все 40 больных были оперированы в плановом порядке. Для рассечения мягких тканей использовался обычный хирургический скальпель. После окончания основного этапа операции в края послеоперационной раны вводился аллогенный биоматериал, разведенный 1:10 в 0,5% растворе новокаина. Для этого нами использовался безигольный инъектор БИ-8. После этого производилось послойное ушивание послеоперационной раны. В после операционном периоде проводились ежедневные перевязки с обработкой краев послеоперационной раны 70° этиловым спиртом.
Швы с послеоперационной раны снимались на 7-9-е сутки. На 3-4 сутки в ране появлялись грануляции, а к 8-м суткам с краев раны наползал эпителий. Цитологическая картина в этой группе больных показывает, что концентрация микрофлоры становится меньше по сравнению с первой группой больных. Большее число макрофагов участвует в фагоцитозе. В раневом экссудате появляются гистиоциты по типу молодых полибластов в состоянии активного фаго цитоза. В последующем резко снижается содержание нейтрофильньгх лейкоцитов, которые расположены вместе с соединительнотканными элементами. Таким образом, при лечении послеоперационных ран с использованием аллогенного биоматериала, цитологическая картина показывает позитивные изменения соотношения клеточных форм, что свидетельствует о хороших регенераторных процессах в ране.
При гистологическом исследовании биоптатов из краев ран на 3-4 сутки после лечения с применением аллогенного биоматериала формирование грануляционной ткани происходило раньше чем в первой группе больных.
В области краев ран к 6-7 суткам происходит формирование грануляционной ткани с врастанием кровеносных сосудов. Имеется большое количество лимфоцитов, плазматических клеток и полинуклеаров. На 11-12 сутки происходит полное созревание грануляционной ткани, уменьшение количества клеточных элементов и сосудов. Наблюдается формирование продольных пучков коллагеновых волокон. Со стороны краев раны отмечается наползание эпителия с врастанием многослойного плоского эпителия.
С использованием аллогенного биоматериала наблюдается повышение показателей микроциркуляции в зоне раневых изменений (табл. 2).
| Сроки наблюдения | Параметры микроциркуляции | |||||
|---|---|---|---|---|---|---|
| ПМ | СКО | Cv | Fv | Av | Ст | |
| Исходные данные | 10,6±1,2 | 2,0±0,4 | 9,6±1,3 | 4,1±0,1 | 1,3±0,2 | 12,1±0,8 |
| 3-4 сутки | 6,1±0,99* | 2,1±0,2* | 8,3±1,1* | 3,2±0,2* | 1,0±0,2* | 10,2±0,2* |
| 6-7 сутки | 8,2±1,1* | 2,5±0,3* | 9,4±0,8* | 3,4±0,3* | 1,4±0,3* | 11,8±0,2* |
| 11-12 сутки | 10,4±1,2 | 2,2±0,2 | 9,6±0,7 | 4,0±0,5 | 1,6±0,3 | 12,0±0,1 |
Примечание: * — показатели достоверно (р<0,05) отличающиеся от данных контрольной группы (табл. 1).
Сочетанное лечение с применением терапевтического лазера и аллогенного биоматериала получали 40 больных. Группа состояла из 19 мужчин и 21 женщин. Все больные этой группы были оперированы в плановом порядке. Рассечение мягких тканей производилось с помощью хирургического скальпеля. После окончания основного этапа операции в края послеоперационной раны вводился аллогенный биоматериал, разведенный в 0,5% растворе новокаина 1:10 с помощью безигольного инъектора БИ-8. Рана зашивалась послойно. В послеоперационном периоде больным проводились ежедневные перевязки с обработкой раны 70° этилового спирта. Начиная со второго дня, после операции рану начинали облучать через повязку терапевтическим лазером (ALTO-терапевт) в инфракрасном режиме. Параметры излучения составили: поток плотности мощности 70мBт/см2, частота излучения 170 Гц с экспозицией 2 минуты на одно поле. Количество полей облучения зависело от размеров после операционной раны. Швы в данной группе больных с послеоперационной раны снимались на 7-8 сутки
Первые единичные грануляции начинали появляться уже к концу 2-х суток. К концу шестых, началу седьмых суток рана заполнялась полностью грануляциями и появлялась краевая эпителизация. При исследовании цитологической картины на 3--4 сутки в мазках-отпечатках обнаружено снижение палочковой и кокковой флоры, нейтрофильных лейкоцитов. Большинство препаратов на 6-7 сутки были представлены фибробластами и единичными дифференцированными элементами. К 11-12 суткам в мазках-отпечатках исчезала флора, определялись единичные деградирующие фибробласты, зато в большом количестве были представлены молодые эпителиальные клетки, т.е. наблюдалась картина дифференцирования рубцовой ткани.
При гистологическом исследовании биоптатов из краев ран на 3-4 сутки после сочетанного лечения раневой дефект заполнялся грануляционной тканью. Имелось большое количество полинуклеаров, лимфоцитов и гистиоцитов. На 6-7 сутки грануляции полностью заполняли раневой дефект с хорошо развитыми сосудами и начинали определяться коллагеновые волокна. К концу 11-12 суток полностью завершалась эпителизация. Сочетанное применение аллогенного биоматериала и энергии низкоинтенсивного лазерного изучения значительно повысило показатели микроциркуляции в области раны (табл. 3).
| Сроки наблюдения | Параметры микроциркуляции | |||||
|---|---|---|---|---|---|---|
| ПМ | СКО | Cv | Fv | Av | Ст | |
| Исходные данные | 10,9±1,2 | 2,1±0,4 | 9,8±1,3 | 4,3±0,1 | 1,6±0,2 | 12,6±0,8 |
| 3-4 сутки | 7,2±0,4* | 2,1±0,3* | 8,8±1,1* | 3,7±0,3* | 1,5±0,4* | 12,4±0,7* |
| 6-7 сутки | 9,1±0,5* | 2,9±0,2* | 9,7±1,2* | 3,7±0,3* | 1,5±0,4* | 12,4±0,7* |
| 11-12 сутки | 11,0±0,8 | 2,4±0,5 | 10,1±1,4 | 4,4±0,3 | 1,8±0.6 | 13,2±0,2 |
Примечание: * — показатели достоверно (р<0,05) отличающиеся от данных контрольной группы (табл. 1).
Полученные данные свидетельствуют о том, что самое высокое насыщение тканей кислородом в области раны происходит в III группе. На основании этого можно заключить, что в данной группе больных идет более быстрое восстановление микроциркуляции в области раны (табл. 4).
| Средние сроки (в сутках) | I группа | II группа | III группа |
|---|---|---|---|
| 3-4 сутки | 18,1 ±0,61 | 21,3 ±0,53 | 26,4 ±0,48 |
| 6-7 сутки | 20,9 ±0,74 | 25,9 ±0,94 | 31,3 ±0,21 |
| 11-12 сутки | 27,3 ±0,36 | 33,8 ±0,71 | 41,1 ±0,61 |
В результате лечения послеоперационных ран сочетанным способом с использованием аллогенного биоматериала и терапевтического лазера значительно позволяет сократить сроки заживления ран и уменьшить число осложнений со стороны раны.
| Осложнения | I группа | II группа | III группа |
|---|---|---|---|
| Инфильтрат в области раны | 4 | 1 | - |
| Нагноение раны | 2 | - | - |
| Серома | 3 | 1 | 1 |
| Гематома | 4 | 1 | - |
| Лигатурные свищи | - | - | - |
| Расхождение краев раны после снятия швов | 2 | - | - |
Лечение келоидных и гипертрофических рубцов
Комплексное лечение патологических рубцов с использованием низко- и высокоэнергетических лазеров, а также аллогенного биоматериала.
Всех больных с келоидными и гипертрофическими рубцами мы разделили на две группы по 25 человек в каждой.
Давность образования келоидных и гипертрофических рубцов составила от 1 до 10 лет. Площадь, занимаемая рубцами, составила от 2 до 16 см2, и в среднем составила 9,3 см2. Все больные жаловались на периодические боли и зуд в области рубцов, а также на чувство дискомфорта в косметическом отношении. В обеих группах все больные были оперированы.
В первой группе больных оперировали следующим образом. Под местной анестезией 0,5% раствора новокаина производили полное иссечение келоидного рубца хирургическим скальпелем в пределах здоровой кожи. После того в края раны вводился аллогенный биоматериал в разведении 1:10 с физиологическим раствором. Для этого использовался безигольный инъектор БИ-8. На рану накладывались первичные швы. В послеоперационном периоде больным про водились ежедневные перевязки с обработкой раневой поверхности 70° спиртом. На вторые сутки после операции все больные получали на рану лазеротерапию через повязку. Для этого использовался лазерный аппарат ALTO-терапевт. Параметры излучения составили: длина волны 0,863 мкм, плотность потока мощности 3-5мВт/см2 и временем экспозиции 2-4 минуты на одно поле. Количество полей облучения зависело от размеров раны. Количество сеансов составило от 7 до 12.
Во второй группе больных оперировали с применением хирургического лазера Ланцет-1.
Параметры лазерного излучения составили: длина волны 10,6мкм, выходная мощность 10-15 Вт/см2. После обезболивания 0,5% раствором новокаина производили операцию. Для этого использовали два способа удаления рубцов (paц, предложение № 2120 от 16.1199г. выданное Башкирским государственным медицинским университетом. Способ лечения и профилактики келоидных и гипертрофических рубцов.).
Первый способ заключается в полном иссечении келоидного рубца в пределах здоровой кожи. Для этого использовался сфокусированный луч хирургического лазера. По данной методике оперировались в основном больные с небольшими по размерам рубцами, что давало возможность наложения первичных швов без особого натяжения.
Второй способ заключается в так называемой лазерной шлифовке рубцов. Данный способ нами применялся у больных с наличием больших, деформирующих рубцов расположенных в основном над суставами. При данном способе производится непосредственное удаление (шлифовка) тканей рубца. Для этого использовали как сфокусированный, так и расфокусированный лучи хирургического лазера.
После удаления рубцовой ткани в края раны вводился аллогенный биоматериал по выше указанной методике. На рану накладывались первичные швы. Больным, которым производилась шлифовка рубцов, швы на рану не наклады вались, и заживление у них происходило под лазерным струпом. Начиная со второго дня, после операции, все больные данной группы получали лазеротерапию на рану также как и в первой группе.
Оценивая результаты лечения, в обеих группах больных мы получили следующие данные. При микробиологическом исследовании мы обращали внимание на содержание микрофлоры в 1 грамме ткани из раны. Данный показатель является информативным лабораторным тестом для прогнозирования возможного нагноения послеоперационной раны. В первой группе больных этот показатель на 2-е сутки после операции составил 102—103. Во второй группе больных на 2-е сутки после операции микробиологические посевы из раны дали отрицательный рост. Это говорит о том, что во время лазерной обработки происходит полное обеспложивание микроорганизмов в области раны. В первой группе больных после иссечения рубцов приходилось проводить гемостаз сосудов при помощи легирования. Во второй группе гемостаз полностью достигался при помощи фотокоагуляции лазерным лучом.
При гистологическом исследовании биоптатов взятых на 6-7 сутки из раны, отмечалось выраженное развитие грануляционной ткани с обилием сосудов в обеих группах больных. Кроме того, во второй группе больных к данному сроку появлялись коллагеновые волокна с правильным расположением, что говорит о стимулирующем действии хирургического лазера на процесс ранозаживления. В отдаленные сроки было осмотрено 39 человек (78%). Рецидив келоидообразования выявлен у трех больных (7,2%). Рецидив келоидообразования у данных больных мы связываем с незавершенным курсом лазеротерапии.
Выводы
- Использование диспергированного аллогенного биоматериала "Стимулятор регенерации" как самостоятельно, так и в комплексе с лазерным излучением является эффективным методом лечения послеоперационных ран кожи.
- С использованием аллогенного биоматериала и энергии лазерного излучения, состояние микроциркуляции и насыщение тканей кислородом (рО2) в зоне раневых изменений улучшается.
- Применение аллогенного биоматериала и энергии лазерного излучения в комплексном лечении послеоперационных ран приводит к достоверному улучшению регионарной гемодинами, возрастанию парциального давления кислорода в зоне раневых изменений, активации процессов репаративной регенерации соединительнотканных структур их ускоренной эпителизации с формированием полноценного в функциональном и косметическом отношении регенерата.
- Комплексное применение аллогенного биоматериала с энергией лазерного излучения в лечении послеоперационных ран позволяет предупредить образование грубых келоидных рубцов, а также сократить число нагноений раны.
- Используя высокоэнергегическое лазерное излучение, возможно производить шлифовку келоидных и гипертрофических рубцов бесконтактным способом. Заживление раны под лазерным струпом происходит первичным натяжением.
Практические рекомендации
- Применение диспергированного аллогенного биоматериала "Стимулятор регенерации" как самостоятельно, так и в комплексе с лазерным излучением, можно рекомендовать для лечения послеоперационных ран любого генеза и локализации в широкую клиническую практику.
- Способ комплексного лечения послеоперационных ран можно рекомендовать для применения в лечебных учреждениях, где имеются высоко- и низкоэнергетические лазерные аппараты.
- Использование аллогенного биоматериала в комплексе с высоко- и низкоэнергетическим лазерным излучением может применяться в лечении и профилактике келоидных и гипертрофических рубцов.
- Предложенный нами метод лечения келоидных и гипертрофических рубцов может быть использован как самостоятельно, так и в комплексе с другими методами в лечении рубцовых деформаций, в том числе и ожоговых.
Литература
- И.А. Сафин, В.П Соколов, B.C. Пантелеев, Опыт работы республиканского центра лазерной медицины. «Проблемы и перспективы работы специализированных медицинских центров. Всероссийская конференция. Самара. 1997г. с.107-108.
- B.C. Пантелеев, И.А. Сафин, В.П. Соколов. Применение Аллопланта и лазерного излучения в профилактике келоидов. Актуальные вопросы гнойной хирургии. Всероссийская конференция. Новосибирск. 1999г. а.87-88.
- И.А. Сафин, МП Соколов, B.C. Пантелеев. Применение Аллопланта и энергии лазерного излучения в профилактике келоидов. Международный конгресс по лазерной медицине здоровье-99. С. 110.
- И.А, Сафин, В.П. Соколов, B.C. Пантелеев. Лазеры в хирургии. Журнал. Здравоохранение Башкортостана 5/99. С.41-44.
- И.А. Сафин, B.C. Пантелеев, В.П. Соколов. Использование аллотрансплантата серии Аллоплант и энергии лазерного излучения в лечении ран. Актуальные вопросы диагностики и лечения заболеваний органов гепатопанкреатобиллиарной зоны. Республиканская конференция. Уфа. 2000г. с. 165.
- И.А. Сафин, В.П. Соколов, B.C. Пантелеев. Опыт работы центра лазерной медицины. Актуальные вопросы здравоохранения в РБ. Уфа. 2000г. с. 19-20.
- И.А. Сафин, B.C. Пантелеев. В.П. Соколов. Использование энергии лазерного излучения в сочетании со стимулятором регенерации Аллоплант при лечении гнойных ран. Республиканская конференция, посвященная 65-летию кафедры оперативной хирургии и хирургической анатомии. Уфа. 2000г. с.70-71.
- И.А. Сафин, В.П. Соколов, ВС. Пантелеев. Новые возможности использования лазерного излучения и биопланта в лечении ран. «Лазерные и информационные технологии в медицине XXI века». Международная научно-практическая конференция. Санкт-Петербург. 2001г. с.119-120.
- B.C. Пантелеев, И.А. Сафин, В.П. Соколов. Коррекция раневого процесса в целях профилактики келоидообразования путем применения лазерного излуче ния. Актуальные вопросы повышения квалификации врачей и провизоров. Республиканская конференция, посвященная 25—летию института последипломного образования. БГМУ. Уфа. 2001г. с.201-202.
- Опыт работы Республиканского центра лазерной медицины. Сборник тезисов посвященных 125-летию Республиканской клинической больницы им. ГГ. Куватова. Уфа. 2001г. С.24.
Рационализаторские предложения
- «Способ профилактики гипертрофических и келоидных рубцов» № 2120
- от16.11.99г.Уфа.БГМУ.
- «Способ лечения гнойных ран» № 2211 от 15.05.00г. Уфа. БГМУ.
- «Способ профилактики пареза кишечника и раневых осложнений в послеоперационном периоде» № 2315 от 23.02.01г.
- «Способ обработки раневой поверхности при вентральных грыжах» № 2312 от 23.02.01г. Уфа. БГМУ.
к содержанию | опубликовать статью
КОМПЛЕКСНОЕ ЛЕЧЕНИЕ ТРОФИЧЕСКИХ ЯЗВ НИЖНИХ КОНЕЧНОСТЕЙ С ИСПОЛЬЗОВАНИЕМ СТИМУЛЯТОРА РЕГЕНЕРАЦИИ АЛЛОПЛАНТ И ЭНЕРГИИ ЛАЗЕРНОГО ИЗЛУЧЕНИЯ
Соколов В. П.
ГБОУ ВПО «Башкирский государственный медицинский университет Министерства здравоохранения и социального развития Российской Федерации»
На основании проведенных исследований доказана эффективность применения стимулятора регенерации Аллоплант в лечении трофических язв нижних конечностей. Выявлено, что стимулятор регенерации Аллоплант оказывает стимулирующее влияние на репаративные процессы в трофической язве. Разработан метод введения стимулятора регенерации Аллоплант в ткани области трофической язвы. Впервые доказано с использованием гистологических и цитологических методов исследования, что применение стимулятора регенерации Аллоплант и энергии лазерного излучения наиболее эффективно при лечении трофических язв нижних конечностей.
Актуальность Проблема лечения трофических язв нижних конечностей представляет одну из актуальных задач современной медицины, так как до сих пор в лечении этой патологии остается много нерешенных вопросов. Это объясняется значительным распространением заболевания (ими страдает до5'% взрослого населения), резистентностью к терапии и длительностью нетрудоспособности. Почти каждый десятый человек, страдающий хронической венозной недостаточностью нижних конечностей, из-за наличия трофической язвы становится инвалидом (Аскерханов Р.П.,1979).
Образовавшиеся трофические язвы вследствие длительности существования дефекта кожного покрова и .ослабления репаративных процессов и них, значительных дистрофических и рубцовых изменений в окружающих тканях не способны к стойкой самостоятельной эпителизации, а существующие современные методы их лечения недостаточно эффективны [Васютков В.Я., 1977, Григорян P.M., 1991, Кузин М.И., 1970, Шалимов А.А., 1981].
Современная концепция лечения трофических язв определяет два основных направления - консервативное и оперативное. Однако, несмотря на многообразие существующих методов как оперативного, так и консервативного лечения, частота рецидивов по литературным данным составляет при хирургических методах от 9,2% до 31,6% [Даудерис И.П., 1984, Вилянский М.П., 1988], а при консервативном - от 38% до 100% случаев [Мазаев П.Н., 1987].
Успех хирургических методов лечения во многом зависит от этиологических причин и возможности их коррекции, а так же от степени подготовленности трофических язв к операции. Оперативные пособия необходимо производить после очищения язв от гнойно-некротических масс, стихания воспалительных процессов в окружающих тканях. [Джитава И.Г., 1984]. Для достижения этой цели используются разнообразные физические, химические, биологические методы. К методам очищения язв от гнойно-некротических тканей относятся механические (инструментальная некрэктомия) [Тимебулатов В.М. и соавт.,1992], химические (энзимотерапия) [Водолазская Л.В.,1982, Герцен А.В., 1988], термические (лазерная некрэктомия) [Кошелев В.Н., 1985, Бабаева О.Б., 1988]. Для стимуляции регенерации используют большой арсенал средств и методов (медикаментозные, химические, Физические). Несмотря на все вышесказанное поиск наиболее эффективных методов и патогенетической терапии продолжается.
Весьма перспективным направлением в этом поиске является разработка и внедрение в практику лечения новых препаратов, а так же разработка и внедрение наиболее эффективных способов комбинированного лечения трофических язв.
Попытка получить лучшие результаты в этих направлениях и легла в основу настоящего исследования.
ЦЕЛЬ ИССЛЕДОВАНИЯ
Целью настоящего исследования является разработка и внедрение в клинику стимулятора регенерации Аллоплант и энергии лазерного излучения при комплексном лечении трофических язв.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
В работе проводится анализ результатов лечения 136 больных с трофическими язвами нижних конечностей, в числе которых 71 женщина и 65 мужчин. Более 67% из них - люди трудоспособного возраста.
Сопутствующие заболевания выявлены у 63% больных, среди которых: ишемическая болезнь сердца составляет 37%, гипертоническая болезнь -19%, ожирение-18%, сахарный диабет-10%, облитерирующий атеросклероз нижних конечностей - 8 %, прочие - 8%.
Гиперпигментация кожи и индурация подкожной жировой клетчатки наблюдались у 71% больных. Аллергический дерматит - у 39%. Площадь трофических язв варьировала от 1 до 201 см2 и составляла в среднем 16,2 - 1,4 см2.
Для диагностики заболеваний использовались общепринятые методы обследования: анамнестические данные, осмотр, пальпация, перкуссия, аускультации, методы лабораторного исследования.
Из специальных методов обследования для оценки состояния венозного кровообращения нижних конечностей использовались функциональные пробы Троянова-Тренделенбурга, Шварца, Майерса. Мейо-Пратта, Дельбе-Пертеса и др. Использовали восходящую флебографию с введением рентгеноконтрастного препарата в венозное русло.
Цитологическое исследование проводили по методу М.П.Покровской и М.С.Макарова (1942). Полученные мазки-отпечатки высушивали и фиксировали в смеси Никифорова с последующим окрашиванием по Романовскому-Гимзе.
Морфологические исследования проводили на биопсийном материале, взятом в различные сроки ( до начала лечения, на 4-5, 9-11 сутки от начала лечения, а в III, основной группе и сразу после лазерной некрэктомии). Материал брали со дна и краев трофической язвы.
Микробиологические исследования включали в себя качественное и количественное определение микроорганизмов путем посева на питательные среды.
Для регистрации скорости уменьшения раневой поверхности использовали метод, предложенный Л.Н.Поповой в 1942 году.
Кроме этого использовали реовазографические, иммунологические и другие методы исследования.
В первой группе больных (40 человек) лечение трофических язв проводили традиционным методом: язву обрабатывали раствором антисептика, некротизированные ткани удаляли механическим путем, на язвы накладывали повязки с протеолитическими ферментами. В фазе регенерации применялись мазевые повязки.
Во второй группе (46 больных) для ускорения репаративных процессов применялся диспергированный аллогенный биоматериал «Cтимулятор регенерации» серии Аллоплант, который представляет собой продукт специальной запатентованной физико-химической обработки аллогенных тканей, взятых у трупа (производится в Лаборатории консервации тканей ФГБУ ВЦГПХ Минздравсоцразвития России). Препарат содержит такие компоненты внеклеточного матрикса, как коллаген, протеогликаны, гликопротеины, гликозаминогликаны и относится к группе тканевых стимуляторов, которые, перевариваясь ферментами организма и рассасываясь, стимулируют репаративные процессы и постепенно замещаются собственными тканями организма. Препарат имеет вид мелкодисперсного порошка и упакован во флаконы по 5мл. Стерилизован гамма-излучением. Препарат разводили из расчета 1:10 в 0,5% растворе новокаина и вводили в ткани области трофической язвы при помощи безигольного инъектора БИ-8.
Аутодермопластика при не полном заживлении трофических язв произведена 28 больным (7 из контрольной группы, 9 из второй и 12 из третьей группы).
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЙ И ИХ ОБСУЖДЕНИЕ
В первой группе больных средняя скорость уменьшения площади язв составляла 2,66±0,15% (см.таб. 1).
| Симптомы | Средние сроки, сут |
||
|---|---|---|---|
| I группа | II группа | III группа | |
| Уменьшение болей | 14,7±0,9 | 6,9±0,7 Р<0,01 | 5,1+0,4 Р<0,01 |
| Появление единичных грануляций | 6,7±0,4 | 3,9±0,3 Р<0,01 | 2,1±0,15 Р<0,01 |
| Очищение от некротических масс | 7,6+0,5 | 4,9±0,3 Р<0,01 | - |
| Заполнение грануляциями и появление краевой эпителизации | 18,0±1,1 | 9,1 ±0,4 Р<0,01 | 7,3±0,4 Р<0,01 |
| Скорость уменьшения площади язв в регенеративном периоде,% | 2,66±0,15 | 4,3±0,3 Р<0,05 | 6,4±0,35 Р<0,05 |
К 30 суткам лечения в большинстве мазков-отпечатков основными клеточными элементами были фибробласты, молодой и слущивающийся эпителий, которые свидетельствовали о продолжающемся регенеративном процессе (см. таб. 2).
| Элементы цитограмм | При поступлении | 9-10 сутки | 19-20 сутки | 21-30 сутки |
|---|---|---|---|---|
| Флора | ||||
| Кокковая | ++++ | +++ | ++ | +- |
| Палочковая | +++ | ++ | + | - |
| Фагоцитированная | - | ++ | + | - |
| Лейкоциты | ||||
| Нейтрофилы | ++++ | ++++ | ++ | +- |
| Фагоцитирующие | - | + | ++ | +- |
| Эозинофилы | - | - | + | - |
| Лимфоциты | - | + | - | - |
| Гистиоциты | ||||
| Полибласты | - | ++ | + | +- |
| Вакуолизированные | - | +++ | + | +- |
| Макрофаги | - | + | - | - |
| Соединительнотканные клетки | ||||
| Профибробласты | - | + | + | + |
| Фибробласты | - | + | ++ | ++ |
| Эпителий | ||||
| Молодой | - | - | + | ++ |
| Слущивающийся | - | - | - | + |
В результате применения Стимулятора регенерации во второй группе язва достаточно быстро очищалась от гнойно-некротических масс (в среднем за 5 суток), ускорялось появление единичных грануляций (на 4 сутки) и значительно сокращался период заполнения; язвы зрелой грануляционной тканью и появление краевой эпителизации (в среднем на 9 сутки от начала лечения), в результате чего длительность репаративного периода уменьшилась в 2 раза по сравнению с контрольной группой. Скорость уменьшения площади язвы составляла 4,3_+0,3% (см. таб. 1).
| Элементы цитограмм | При поступлении | 9-10 сутки | 19-20 сутки | 21-30 сутки |
|---|---|---|---|---|
| Флора | ||||
| Кокковая | ++++ | +++ | + | + |
| Палочковая | +++ | + | - | - |
| Фагоцитированная | - | ++ | +- | - |
| Лейкоциты | ||||
| Нейтрофилы | ++++ | +++ | + | - |
| Фагоцитирующие | - | ++ | + | - |
| Эозинофилы | - | + | - | - |
| Лимфоциты | - | + | - | - |
| Гистиоциты | ||||
| Полибласты | - | ++ | + | - |
| Вакуолизированные | - | ++ | + | - |
| Макрофаги | - | + | + | - |
| Соединительнотканные клетки | ||||
| Профибробласты | - | + | ++ | ++ |
| Фибробласты | - | +- | ++ | ++ |
| Эпителий | ||||
| Молодой | - | - | ++ | +++ |
| Слущивающийся | - | - | + | ++ |
При гистологическом исследовании на 4-5 сутки лечения вокруг аллотрансплантанта появляются очаги грануляционной ткани; на 9-11 сутки происходит созревание грануляционной ткани, формирование пучков коллагеновых волокон. Преобладание в большинстве мазков-отпечатков фибробластов, молодого и слущивающегося эпителия наблюдалось в этой группе на 19-20 сутки (см. таб. 3).
В третьей группе (50 больных) проводилось комплексное лечение с использованием наряду с медикаментозным, энергию лазерного излучения и Стимулятор регенерации Аллоплант.
На следующие сутки после госпитализации больного в стационар, под внутривенным наркозом, или под местной анестезией (в зависимости от состояния больного и величины трофической язвы) производилась лазерная некрэктомия трофической язвы. Удаление некротизированных тканей в зоне трофической язвы проводилось углекислотными лазерами "Скальпель-1" или "Скальпель-3", с плотностью потока мощности 60-70 вт/см2. При этом все некротические ткани и гной превращались в аэрозольные и газообразные продукты и удалялись из операционного поля дымоотсосом. Тонкий коагуляционный струп удалялся марлевой салфеткой, смоченной в 3% растворе перекиси водорода.
Сразу после некрэктомии в ткани области трофической язвы вводился Стимулятор регенерации Аллоплант. Начиная со следующего дня, поверхность язвы подвергалась облучению гелий-неоновым лазером с длиной волны 0,633мкм, плотностью мощности 3-5 мвт/см, временем облучения от 2 до 5 минут. За курс лечения больные получали от 10 до 15 сеансов лазеротерапии. Замечено, что под воздействием излучения гелий-неонового лазера активизируется пролиферативная фаза воспаления, ускоряются процессы трансформации грануляционной ткани в фиброзную.
В динамике цитологической картины в первые дни после некрэктомии отмечается скудость клеточных элементов, а к 9 суткам в мазках-отпечатках определялись единичные деградирующие фибробласты, в большом количестве были представлены молодые эпителиальные клетки, т.е. наблюдалась картина дифференцирующей покровной ткани (см. таб.4).
При гистологическом исследовании биоптатов из трофических язв на 4-5 сутки определяется грануляционная ткань с большим количеством сосудов, что говорит о высокой репаративной активности. На 9-11 сутки определяется формирующаяся эпителиальная ткань, а с краев язвы наползает многослойный плоский эпителий. К 16 суткам язва эпителизируется и в биоптатах определяется многослойный плоский эпителий. Средняя скорость уменьшения площади трофической язвы составила 6,4±0,35% (см. таб.1).
По нашим данным средняя продолжительность пребывания больных в стационаре в контрольной группе составила 32,13± 1,7, во второй группе -28,3±1,1, а в третьей группе - 16,23±1,3 дня.
| Элементы цитограмм | При поступлении | 9-10 сутки | 19-20 сутки | 21-30 сутки |
|---|---|---|---|---|
| Флора | ||||
| Кокковая | ++++ | - | + | - |
| Палочковая | +++ | - | - | - |
| Фагоцитированная | - | - | +- | - |
| Лейкоциты | ||||
| Нейтрофилы | ++++ | ++ | + | - |
| Фагоцитирующие | - | - | + | +- |
| Эозинофилы | - | - | + | - |
| Лимфоциты | - | - | + | - |
| Гистиоциты | ||||
| Полибласты | - | - | + | - |
| Вакуолизированные | - | - | + | - |
| Макрофаги | - | - | + | - |
| Соединительнотканные клетки | ||||
| Профибробласты | - | - | + | ++ |
| Фибробласты | - | - | +- | ++ |
| Эпителий | ||||
| Молодой | - | - | - | +++ |
| Слущивающийся | - | - | - | +- |
При изучении отдаленных результатов ремиссия достигнута в контрольной группе у 49,8%, во второй группе - у 60%, в третьей группе - у 63,2%.
У больных с трофическими язвами большой площади ( более 16см" в контрольной группе и более 25см" в основных) полного заживления язв не наступало, в этих случаях производилась аутодермопластика.
Аутодермопластика произведена 28 больным (7 из контрольной группы, 9 из второй и 12 их третьей группы).
Средние сроки выполнения пластической операции со дня поступления больного в клинику в контрольной группе составили 19±2,4 дней, во второй группе - 12+1,9 дней, в третьей группе - 1,6±0,5 дней.
| Сроки | I группа | II группа | III группа | |||
|---|---|---|---|---|---|---|
| К-во больн. | Рецидивы | К-во больн. | Рецидивы | К-во больн. | Рецидивы | |
| 1 год | 30 | 5(16,7%) | 35 | 3(8,6%) | 38 | 3(7,9%) |
| 2 года | 30 | 7(23,3%) | 35 | 7(20%) | 38 | 7(18,4%) |
| 3 года | 30 | 15(49,8%) | 35 | 14(40%) | 38 | 14(36.8%) |
Такая разница в сроках объясняется тем, что в контрольной группе по данным цитологического исследования длительное время (до 18-19 дня) сохраняется картина гнойно-воспалительного процесса, тем самым создавая условия для отторжения кожного трансплантата. Во второй группе, в результате применения протеолитических ферментов и Стимулятора регенерации сроки значительно сокращаются. В третьей группе аутодермопластика проводилась сразу после лазерной некрэктомии и введения Стимулятора регенерации Аллоплант.
Важным критерием прогнозирования результата аутодермопластики мы считали определение количества микроорганизмов в 1г. ткани. По результатам этого исследования и определялись сроки проведения аутодермопластики.
Анализ ближайших результатов показал, что полное приживление трансплантата в основной группе имело место в 91,6% случаев, частичное отторжение - в 8,4%, тогда, как в контрольной группе полное приживление отмечено в 71,4% случаев, частичное отторжение - в 14,2%, полное отторжение - в 14,2% случаев.
Средние сроки стационарного лечения с учетом предоперационного и послеоперационного периодов в контрольной группе составили 35,5*1,7 дней, во второй группе- 28,6±1,9 дня и в третьей группе - 15,8*1,3 дня.
Консервативное лечение трофических язв нижних конечностей обусловленных хронической венозной недостаточностью не может гарантировать от рецидивов, так как не устраняет причин их возникновения. Более стойкая ремиссия трофических язв может быть достигнута только при воздействии на этиопатогенетическое звено, что возможно при оперативном вмешательстве.
Нами выполнено 46 оперативных вмешательств по поводу хронической венозной недостаточности у больных в возрасте от 28 до 70 лет. Из них 41 больной (89,1%) были в трудоспособном возрасте. Среди больных, оперированных по поводу трофических язв 19 страдали варикозной болезнью, 27 - посттромботической.
Объем хирургического вмешательства предусматривал проведение флебэктомий комбинированным способом с надфасциальной перевязкой коммуникантных вен по Коккету и субфасциальной перевязкой коммуникантных вен по Линтону. Оперативное вмешательство проводили, не дожидаясь полного заживления трофических язв,.после освобождения язв от некротических тканей и гноя и купирования воспалительных процессов в окружающих язву тканях. Кожный разрез выполняли с учетом локализации язвы, участков гиперпигментации кожи и индурации подкожной жировой клетчатки. В послеоперационном периоде продолжалось лечение трофических язв.
При анализе ближайших результатов оперативного лечения хронической венозной недостаточности, осложненной трофическими язвами и оперированных по Линтону, осложнения в виде краевого некроза отмечены у 1 (10,9%) больных, нагноение субфасциального пространства имело место у 1 (2,8%) пациента из всех оперированных больных.
Отдаленные результаты оперативного лечения прослежены в сроки от 1 до 3 лет у 37 (80,4%) больных из 46. Хорошие отдаленные результаты в течение 3 лет наблюдались у 25(67,6%) больных, удовлетворительные - у 9 (24,3%) больных, неудовлетворительные - у 3 (8,1%) больных.
В результате оперативного лечения у 91,9% больных достигнута стойкая ремиссия заболевания. Наилучший результат дает комплекс лечебных мероприятий, включающий: общее медикаментозное лечение, местное воздействие на трофическую рану энергии лазерного излучения и Стимулятора регенерации Аллоплант, хирургическую коррекцию хронической венозной недостаточности.
ЗАКЛЮЧЕНИЕ
Использование Стимулятора регенерации Аллоплант как самостоятельно, так и в комплексе с высоко- и низкоэнергетическим лазерным излучением является эффективным методом лечения трофических язв нижних конечностей.
Проведенные морфологические исследования трофических язв в ходе лечения с применением Стимулятора регенерации и энергии лазерного излучения свидетельствуют об активизации обменных процессов в ране: более интенсивная васкуляризация, раннее появление и созревание грануляционной ткани и ее трансформация в фиброзную, ускорение краевой эпителизации.
Комплексное применение Стимулятора регенерации с высоко- и низкоэнергетическим лазерные воздействием на трофическую язву позволяет ускорить процессы регенерации в 2 раза по сравнению с контрольной группой.Применение комплексного лечения трофических язв разработанным нами способом позволило добиться ремиссии в отдаленном периоде в 62,5% случаев, а в сочетании с хирургической коррекцией венозного кровотока - в 91,9% случаев.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
Результаты проведенных исследований позволяют рекомендовать в широкую клиническую практику метод лечения трофических язв нижних конечностей с использованием Стимулятора регенерации Аллоплант, поскольку метод прост и доступен для хирургических отделений стационаров и хирургических кабинетов поликлиник, как применяя самостоятельно, так и вместе с низкоэнергетическим лазерным излучением.
Метод комплексного лечения трофических язв нижних конечностей можно рекомендовать для применения в хирургических отделениях стационаров, где имеются хирургические лазерные установки «Скальпель-1» , «Скальпель-3», «Ромашка».
Оба метода могут быть применены в качестве предоперационной подготовки хирургической коррекции венозного кровотока, или, как самостоятельные методы при наличии противопоказаний или отказе больного от операции.
Список литературы
- Возможности лазерного излучения в терапии остеомиелита /Р.Ш.Азаматов, Р.Ш.Сакаев, В.П.Соколов //Тезисы докл., Всесоюзн. конф., «Актуальные проблемы применения магнитных и электромагнитных полей в медицине» - Л.,- 1990, - С. 128-129.
- Внутрисосудистое лазерное облучение крови при гнойно-септических заболеваниях /И.А.Сафин, Р.З.Хусаинов, В.П.Соколов //Юбилейный сборник научных трудов хирургов Республики Башкортостан - Уфа, - 1995. -С. 77.
- Комбинированный метод лечения знойных заболеваний мягких тканей с использованием высоко- и низкоэнергетических лазеров /И.А.Сафин, Р.З.Хусаинов, В.П.Соколов //Юбилейный сборник научных трудов хирургов Республики Башкортостан. - Уфа, -1995.-С.78.
- Лечение трофических язв нижних конечностей /Р.З.Хусаинов, В.П.Соколов, Р.С.Мингазов //Тезисы докл. Всероссийск. симпозиума «Новые технологии в хирургии». - Уфа. - 1996. - С. 224-226.
- Опыт работы республиканского центра лазерной медицины /И.А.Сафин, М.А.Нартайлаков, В.П.Соколов, А.Х.Мустафин и др. //Тезисы Всероссийск. конф. «Проблемы и перспективы работы специализированных медицинских центров». - Самара. - 1997. - С. 107-108.
- Применение высокоэнергетических и низкоэнергетических лазеров в сочетании с биоСтимулятором серии Аллоплант в комплексном лечении трофических язв нижних конечностей /В.П.Соколов, И.А.Сафин, М.А. Нартайлаков, С.А.Муслимов и др.//Тезисы докл. IV междунар. конгресса «Проблемы лазерной медицины». - М.-Видное. - 1997. - С. 157.
- Применение высокоэнергетического и низкоэнергетического лазеров в сочетании со Стимулятором регенерации серии Аллоплант при комплексном лечении трофических язв нижних конечностей /И.А.Сафин, В.П.Соколов //Труды ассоциации хирургов республики Башкортостан за 1997г. - Уфа. - 1998. - С. 102-106.
Рационализаторские предложения
- «Способ лечения гнойно-некротических ран» Удостоверение № 1732, выдано 31 января 1997 года Башкирским государственным медицинским университетом. В соавторстве с А.Х.Мустафиным, В.Д.Дорофеевым.
- «Способ комплексного лечения трофических язв нижних конечностей» Удостоверение № 1759, выдано 2 апреля 1997 года Башкирским государственным медицинским университетом. В соавторстве с И.А.Сафиным, А.Х.Мустафиным.
к содержанию | опубликовать статью
ПРИМЕНЕНИЕ БИОСТИМУЛЯТОРА РЕГЕНЕРАЦИИ АЛЛОПЛАНТ ПРИ ЭКСПЛАНТАЦИОННОЙ ГЕРНИОПЛАСТИКЕ
Шавалеев Р. Р.
ГБОУ ВПО «Башкирский государственный медицинский университет Министерства здравоохранения и социального развития Российской Федерации»
Автором предложено решение одного из важных аспектов проблемы хирургического лечения больных сложными дефектами брюшной стенки путем модуляции местных регенеративных процессов непосредственно в зоне герниопластики с целью формирования функционально адекватных соединительнотканных структур. Разработан способ эксплантационной герниопластики с применением биоматериала Аллоплант (Патент РФ № 2365344 от 29.05.2008). В экспериментальных условиях изучена динамика морфологических изменений в зоне герниопластики с использованием ДБМА. В клинической практике отработана методика безинъекционного использования регулятора регенеративного процесса (ДБМА) и фиксация его медицинским клеем «Сульфакрилат» в зоне применения эксплантата при герниопластике
Актуальность Работа посвящена одной из актуальных проблем брюшной хирургии – диагностике и лечению послеоперационных вентральных грыж (ПВГ) и в частности, сложных дефектов брюшной стенки (СДБС), к которым относят большие и огромные, многократно рецидивирующие грыжи. Значимость этой проблемы постоянно растет в связи с увеличением числа и объема операций на органах живота (В.Д. Федоров, А.А. Адамян, Б.Ш. Гогия, 2000). Успех любой пластической операции на передней брюшной стенке во многом зависит от правильного выбора способа операции и ее технического исполнения (В.Н. Егиев и соавт., 2002; В.А. Зотов и соавт., 2006; R.E. Stoppa, 1995; P.K. Amid, 2004). Важнейшим мотивом настойчивых изысканий при решении данной проблемы является возможность снизить количество возвратов грыж, что имеет большое практическое значение и оправдывает дальнейшие поиски в этом направлении.
Одним из реальных путей решения этой проблемы является использование синтетических сетчатых протезов для герниопластики (В.И. Белоконев, 2000; О.В. Галимов, Т.Н. Хафизов, М.В. Тимербулатов, 2004; U.Klinge et al., 1999; G.Pascual et al., 2008), в том числе обладающих антибактериальным действием (В.В. Плечев и соавт., 2000).
Процесс приживления эксплантатов при этом изучен далеко не полно. Возможности управления формированием полноценного рубца в зоне герниопластики путем применения биологически активных препаратов, таких как Диспергированный биоматериал Аллоплант (ДБМА), могут обеспечить желаемые благоприятные результаты (Р.Т. Нигматуллин, 1996; С.А. Муслимов, 2000; Р.З. Мусин, 2001).
Патогенетический подход к разработке системы хирургического лечения и реабилитации больных грыжами призван обеспечить снижение числа послеоперационных осложнений и рецидива заболевания, поэтому поиск надежных средств и технически не сложных методов лечения и профилактики развития послеоперационных грыж остается актуальным направлением исследований.
Цель исследования – улучшение результатов лечения больных сложными дефектами брюшной стенки при эксплантационной герниопластике.
МАТЕРИАЛЫ И МЕТОДЫ ИССЛЕДОВАНИЯ
Экспериментальное исследование для сравнительного изучения реакции воспринимающего ложа на имплантацию сетчатого протеза «Абактолат» и эксплантата с обработкой по предложенной методике выполнено на 20 серых кроликах массой от 3,0 до 5,0 кг. Методика операции заключалась в том, что поверх апоневроза справа от белой линии живота фиксировали синтетическую сетку (10 мм в диаметре) из нитей «Абактолат» (группа № 1), слева поверх апоневроза проводили имплантацию аналогичной сетки, обработанной диспергированным биоматериалом Аллоплант (одобренного Экспертным Советом по биомедицинской этике Башкирского государственного медицинского университета Федерального агентства по здравоохранению и социальному развитию.
Сертификат соответствия № РОСС RU.ИМ02.В16288 от 22.06.2009 г. по 22.06.2012 г.) и нанесенным на поверхность трансплантата 2,5% раствором медицинского клея «Сульфакрилат» (группа № 2). Животные выводились из опыта в сроки 14–28–60–120–180–360 суток. Все манипуляции выполнялись с учетом требований международных принципов Хельсинской декларации от 2000 г. о гуманном отношении к животным и положений, регламентируемых приложением № 8 «Правил гуманного отношения к лабораторным животным» и другим нормативным документам. Блоки участка брюшной стенки с заключенными в нем протезами были подвергнуты морфологическому исследованию.
Морфологическое исследование проводилось на базе отдела морфологии ФГУ ВЦГПХ (Всероссийского центра глазной и пластической хирургии) и включало в себя методы световой микроскопии.
Для гистологического исследования кусочки тканей фиксировали в 10% нейтральном формалине, после обезвоживания в серии спиртов возрастающей концентрации, заливали в парафин по общепринятой методике. Срезы готовили на микротоме LEICA RM 2145 (Германия) и окрашивали гематоксилином и эозином для общего обзорного исследования и по методу Ван-Гизон для изучения соединительной ткани. Микроскопические исследования проводились с использованием светового микроскопа AXIO IMAGER-Z1 фирмы «CARL ZEISS» (Германия). Препараты фотографировали фотоаппаратом NICON В-100 (Япония). Всего выполнено 158 микроснимков гистологических препаратов.
Цитологические исследования образцов экссудата из вакуумдренажных трубок проводилось в условиях лаборатории электронной микроскопии отдела морфологии ФГУ ВЦГПХ (Всероссийского центра глазной и пластической хирургии) с использованием светового микроскопа LSM 5 PASCAL фирмы «CARL ZEISS» (Германия).
Бактериологические исследования выполнены в бактериологической лаборатории клиники БГМУ. Посевы материала для выявления и идентификации вида микрофлоры проводились по стандартной методике (Приказ Минздрава СССР № 535 от 22 апреля 1985 г. и методическое письмо Горьковского НИИЭМ, 1988 г.).
Клинический раздел исследования основан на анализе 250 историй болезней пациентов послеоперационными вентральными грыжами, оперированных в клинике в 2000-2008 годах с применением эксплантатов «Абактолат» по принятой в клинике методике (группа сравнения). Основную группу составили 53 пациента сложными дефектами брюшной стенки, которым выполнена эксплантационная герниопластика протезом «Абактолат» с аппликацией в ячейки сетки стимулятора регенерации Аллоплант и фиксацией его медицинским клеем «Сульфакрилат» в период 2006–2008 годов.
Статистическая обработка полученных данных. Количественные показатели, полученные в ходе исследования, обработаны методами вариационной статистики. Рассчитывались средняя арифметическая (М) вариационного ряда и средняя ее ошибка (m), коэффициент различия средних величин по критерию Стьюдента (t). Различие средних величин считалось достоверным при p0,05. Для оценки различий распределения частот в отдельных выборках использовался критерий (λ) А.Н. Колмогорова – Н.В. Смирнова (С. Гланц, 1999; О.Ю. Реброва, 2002; В.З. Кучеренко, 2006) и непараметрический критерий Манна-Уитни (U). Компьютерная обработка первичных данных проводилась с использованием программ Microsoft Excel 2007 и Statistica 5.5.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ И ИХ ОБСУЖДЕНИЕ
Разработка способа эксплантационной герниопластики с применением биоматериала Аллоплант
Разработан способ применения ДБМА при хирургическом лечении больных сложными дефектами брюшной стенки. Способ заключается в укреплении линии швов капроновым эксплантатом с пролонгированным антибактериальным действием соразмерно дефекту передней брюшной стенки. Затем в ячейки протеза и в ближайшие ткани вокруг него имплантировался стимулятор регенерации Аллоплант предварительно разведенный в 3 мл физиологического раствора для получения необходимой консистенции. С целью фиксации имплантированного биологического материала и профилактики его аспирации по дренажу, поверх протеза наносился тонкий слой медицинского клея «Сульфакрилат». (Патент на изобретение № 2365344 от 29.05.2008 г.).
Результаты гистологического исследования
На 28 сутки (группа № 1) со стороны апоневроза уже успевала сформироваться широкая полоса относительно плотной соединительнотканной капсулы, отграничивающей образовавшийся очаг воспаления, что не позволяло воспалительным инфильтратам, распространяющимся со стороны сетки, проникнуть вглубь пучков мышечных волокон (рис. 1).
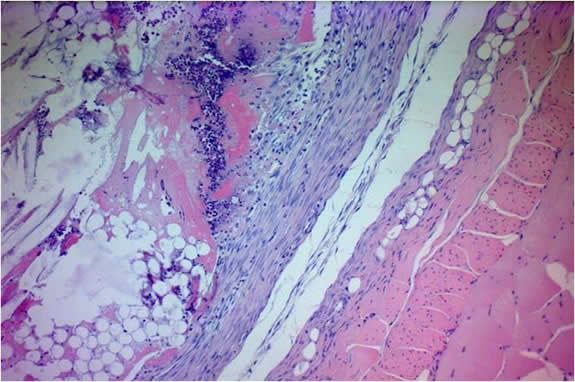 |
|---|
| Рис. 1 Формирование плотной соединительнотканной капсулы вокруг зоны имплантации. Группа № 1, 28 сутки после имплантации. Окраска гематоксилином и эозином. Увел. Х100 |
В группе № 2 на 28 сутки (рис. 2) со стороны апоневроза уже формировалась узкая полоса плотной соединительнотканной капсулы, от нее вглубь сетки начинали врастать тяжи коллагеновых волокон, которые постепенно обволакивали отдельные ячейки сетки или их группы.
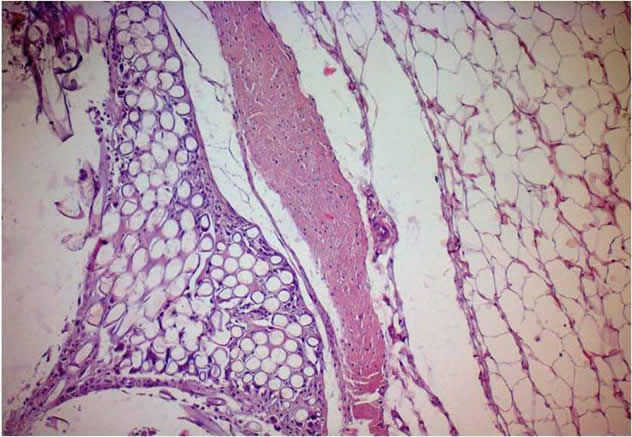 |
|---|
| Рис. 2 Формирование тонкой соединительнотканной капсулы вокруг сетки со стороны апоневроза. Группа № 2, 28 сутки после имплантации. Окраска гематоксилином и эозином. Увел. Х100 |
К 4 месяцам (группа № 1) в тех участках, где воспалительные процессы были менее выражены, между ячейками сетки врастали тонкие тяжи коллагеновых волокон, которые разделяли сетку на отдельные изолированные зоны. Внутри этих зон продолжали выявляться очаговые воспалительные клеточные инфильтраты (рис. 3).
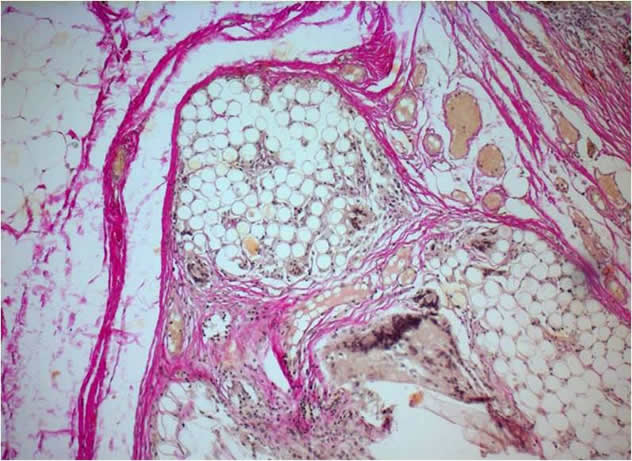 |
|---|
| Рис. 3. Тонкие тяжи коллагеновых волокон, разделяющие сетку на отдельные зоны. Группа № 1, 4 месяца после имплантации. Окраска по методу Ван-Гизон. Увел. Х100 |
Через 4 и 6 месяцев (группа № 2) площадь разрастания волокон соединительной ткани вокруг сетки и внутри нее продолжала увеличиваться, а пучки коллагеновых волокон продолжали врастать между отдельными участками сетки и даже между отдельными ее нитями. Выраженных воспалительных явлений в зоне имплантации сетки и вокруг нее не отмечалось (рис. 4, 5).
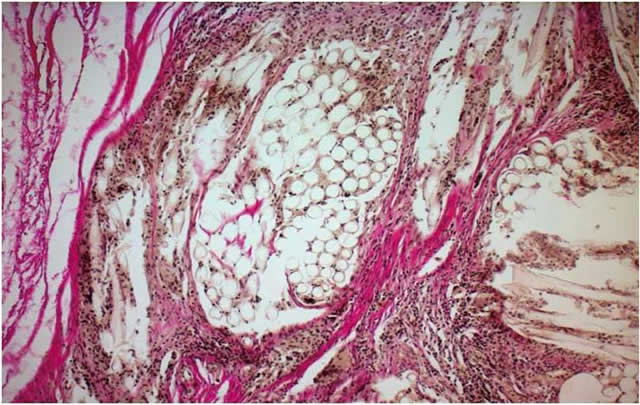 |
|---|
| Рис. 4 Тяжи новообразованной соединительной ткани вокруг ячеек сетки. Группа № 2, 4 месяца после имплантации. Окраска по методу Ван-Гизон. Увел. Х100 |
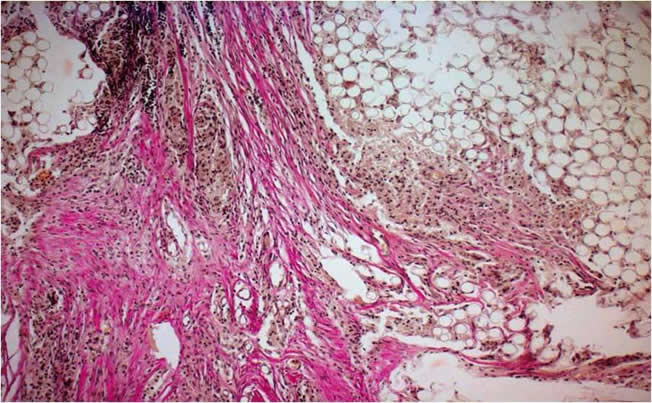 |
|---|
| Рис. 5 Увеличение площади новообразованной соединительной ткани между ячейками сетки. Группа № 2, 6 месяцев после имплантации. Окраска по методу Ван-Гизон. Увел. Х100 |
Через 12 месяцев между ячейками сетки (группа №1) по периферии со стороны апоневроза врастание тяжей коллагеновых волокон между ячейками имплантированной сетки было слабо выраженным. Сохранялись признаки воспалительной реакции в виде клеточной инфильтрации макрофагами, лимфоцитами, плазматическими клетками (рис. 6).
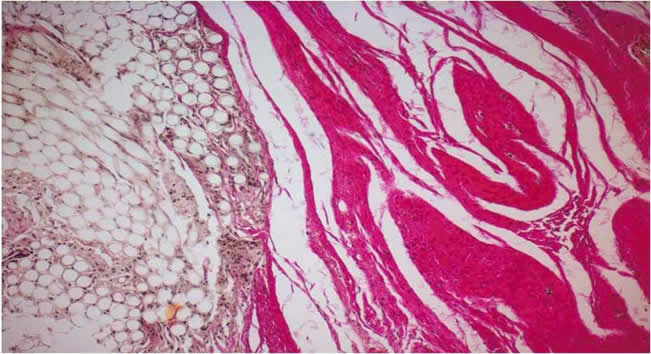 |
|---|
| Рис. 6 ТСлабо выраженное врастание коллагеновых волокон между ячейками имплантированной сетки со стороны апоневроза. Группа № 1, 12 месяцев после имплантации. Окраска по методу Ван-Гизон. Увел. Х100 |
Через 12 месяцев между ячейками сетки (группа № 2) определялись большей частью пучки однонаправленных коллагеновых волокон, плотно обхватывающих ячейки имплантированной сетки. Отмечалось созревание соединительной ткани с упорядочиванием волокон и циркулярной их ориентацией вокруг отдельных зон сетки. В этот срок регенерат представлен зрелой соединительной тканью с правильной ориентацией коллагеновых волокон, хорошей васкуляризацией (рис. 7).
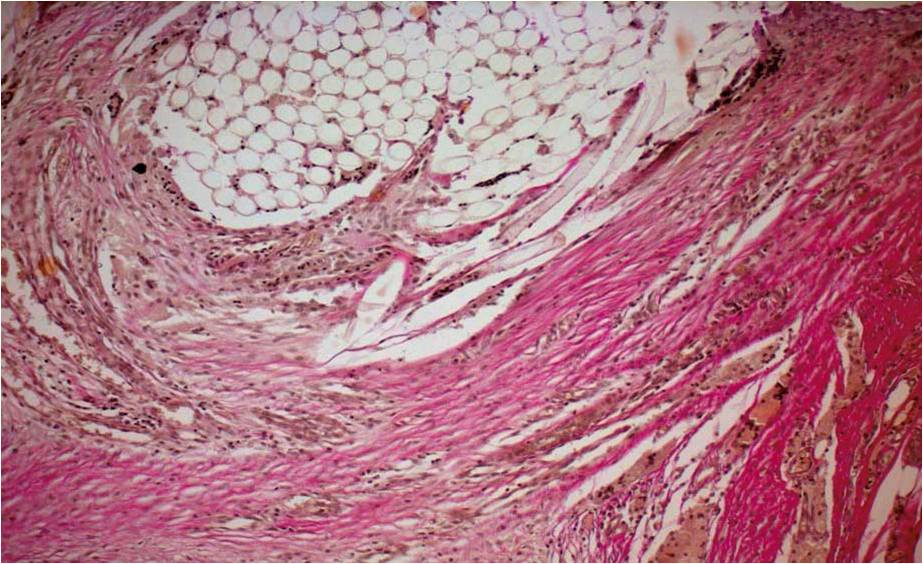 |
|---|
| Рис. 7 Циркулярное расположение соединительнотканных пучков вокруг ячеек сетки. Группа № 2, 12 месяцев после имплантации. Окраска по методу Ван-Гизон. Увел. Х100 |
В аналогичные сроки в препаратах группы №1 в гистологических срезах определялась грубая рубцовая ткань с хаотичным расположением коллагеновых волокон, процессы дифференцировки и перестройки которой еще не завершены. Сохраняются признаки воспалительной реакции в виде клеточной инфильтрации макрофагами, лимфоцитами, плазматическими клетками (рис. 8).
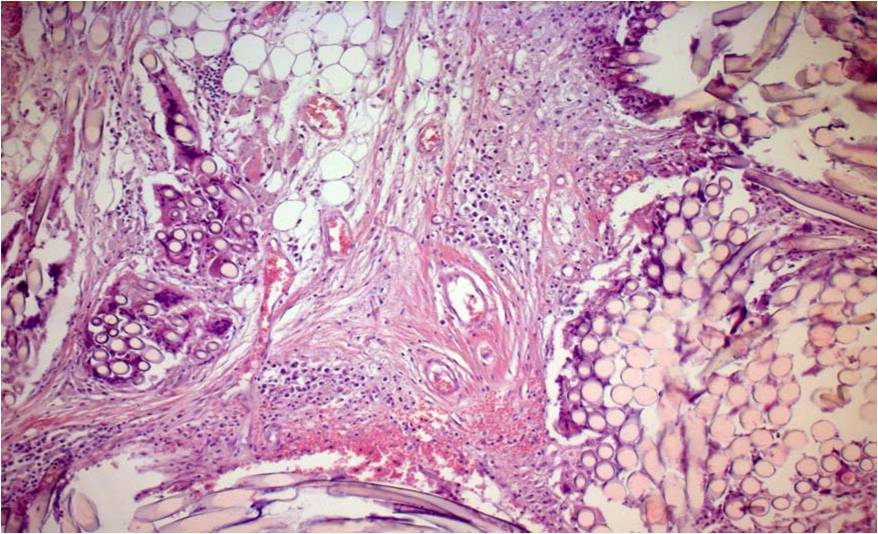 |
|---|
| Рис. 8 Соединительная ткань из разнонаправленных коллагеновых волокон с прослойками крупноячеистой васкуляризированной жировой ткани. Группа № 1, 12 месяцев после имплантации. Окраска гематоксилином и эозином. Увел. Х100 |
Полученные результаты свидетельствуют о том, что при применении сетки с аллогенным биоматериалом в течение года отмечается созревание соединительной ткани с упорядочиванием коллагеновых волокон и циркулярной их ориентацией вокруг отдельных участков сетки. Использование при имплантации сетки ДБМА благоприятствовало снижению воспалительной реакции и создавало условия для стимуляции репаративного процесса с формированием соединительнотканного регенерата, аналогичного по структуре и функции собственному апоневрозу.
Результаты цитологического исследования Изучено цитологическое исследование образцов экссудата из вакуум-дренажных трубок на 1-, 2-, 4-е сутки послеоперационного периода на предмет обнаружения частиц алломатериала в исследуемых образцах, которое показало отсутствие элементов биостимулятора в оттекающей жидкости.
Результаты бактериологического исследования Для выяснения характера микрофлоры раневого экссудата, поступающего по вакуум-дренажам у оперированных больных основной группы, было проведено бактериологическое исследование для выявления и идентификации вида микрофлоры. Полученные результаты показали стерильность извлеченного из вакуум-дренажных трубок материала во всех пробах.
Результаты лечения С применением разработанной методики обработки сетчатого трансплантата в 2006–2008 гг. оперативное пособие выполнено 53 пациентам сложными дефектами брюшной стенки, возрастной категории от 26 до 79 лет. Среди этих больных было 17 (32%) мужчин и 36 (68%) женщины (1:2) разного возраста. Система обследования, предоперационной подготовки, алгоритм выбора способа герниопластики, послеоперационного ведения больных основной группы и группы сравнения существенно не отличались. Сформированная группа сравнения сопоставима с основной группой по возрасту, полу, структуре заболеваемости грыжами различной локализации, состоит из 250 пациентов СДБС, оперированных с применением методов трансплантационной герниопластики и использованием капронового эксплантата с пролонгированным антибактериальным действием «Абактолат» в 2000–2008 гг.
При сравнении больных обеих групп по возрасту значительных различий в распределении не выявлено (рис. 9).
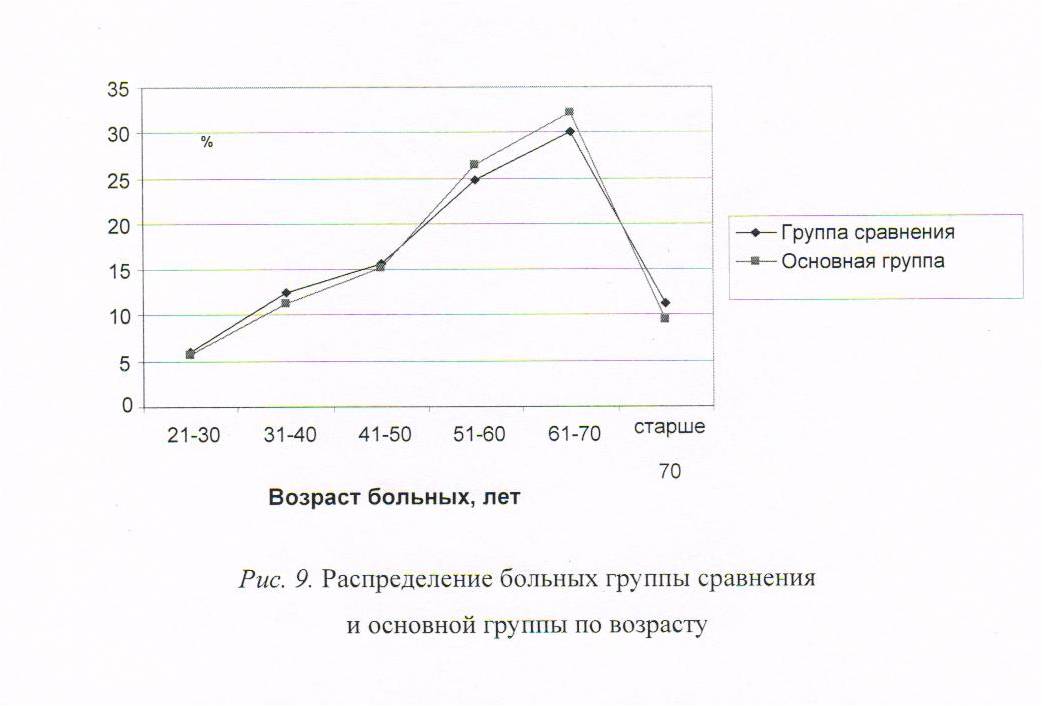 |
|---|
При сравнении средних величин (М±m) возраста в группе сравнения и сновной группе (54,62±2,67 и 54,81±4,52) соответственно получена величина критерия t=0,036 υ= 301 (p=0,971), то есть статистически значимое различие величин отсутствует. Изучение распределения частот по признаку возраста по критерию Колмогорова-Смирнова (λ) установило, что отклонения в распределении являются случайными с высокой степенью ответственности оценки (λ=0,32 p>0,05). Соотношение больных по полу в обеих группах близко 1:2.
Распределение больных в клинических группах по величине и рецидивности ПВГ характеризуется неоднородностью. Заметна отчетливая тенденция к увеличению доли, как грыж больших и огромных размеров, так и рецидивных грыж в основной группе по сравнению с группой сравнения (рис. 10).
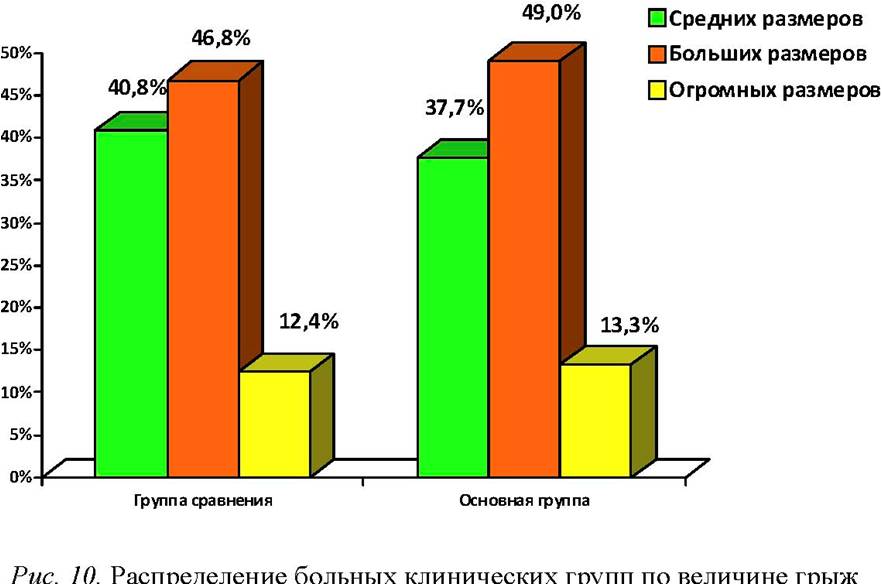 |
|---|
Сроки восстановления функции желудочно-кишечного тракта в послеоперационном периоде (М±m) представлены в табл. 1.
| Признак | Группа сравнения | Основная группа | t | p |
|---|---|---|---|---|
| Появление перистальтики | 1,48±0,2 суток | 0,72±0,3 суток | 2,11 | 0,036 |
| Начало отхождения газов | 2,72±0,1 суток | 2,1±0,2 суток | 2,77 | 0,006 |
| Появление самостоятельного стула | 4,52±0,2 суток | 3,72±0,3 суток | 2,22 | 0,027 |
Имеется статистически достоверное различие всех трех пар признаков, что свидетельствует о сокращении сроков восстановления функции кишечника в основной группе.
Проведен анализ средних величин сроков нахождения вакуум-дренажей у больных обеих групп. Средние сроки (М±m) составили в группе сравнения 7,4±1,6 суток, в основной группе – 3,2±1,2 суток. Рассчитанный критерий t=2,2 при υ= 301 (р=0,028). Имеется статистически достоверное сокращение сроков дренирования в основной группе.
Таким образом, анализ группы сравнения и основной группы показал, что по половым и возрастным критериям обе группы были достаточно однородны.
По признаку величины рецидивности грыж основная группа может быть оценена, как более сложная. Результаты хирургического лечения больных обеих клинических групп представлены в таблице 2.
| Показатели | Группа сравнения | Основная группа | ||
|---|---|---|---|---|
| кол-во | % | кол-во | % | |
| Оперировано больных | n=250 | n=53 | ||
| Выполнено грыжесечений: | 250 | 53 | ||
| – по поводу больших и огромных ПВГ | 148 | 59,2 | 33 | 62,2 |
| – по поводу рецидивных ПВГ | 69 | 27,6 | 17 | 32,1 |
| Послеоперационная летальность | 4 | 1,6 | 0 | 0 |
| Послеоперационные осложнения: | ||||
| – нагноения ран | 5 | 2,1 | 0 | 0 |
| – инфильтраты | 0 | 0 | 2 | 3,8 |
| – атония кишечника | 53 | 21,2 | 0 | 0 |
| – легочные осложнения | 43 | 17,2 | 0 | 0 |
| Изучено отдаленных результатов | 221 | 89,8 | 53 | 100 |
| Выявлено рецидивов грыж | 6 | 2,7 | 1 | 1,9 |
Оценка отдаленных результатов в обеих группах представлена в табл. 3.
| Результаты | Группа сравнения (n=221) | Основная группа (n=53) | p-уровень значимости по критерию χ2 | ||
|---|---|---|---|---|---|
| абс. ч. | % | абс. ч. | % | ||
| Хорошие | 183 | 82,8 | 44 | 83,0 | 0,239 |
| Удовлетворительные | 32 | 14,5 | 8 | 15,1 | 0,149 |
| Неудовлетворительные | 6 | 2,7 | 1 | 1,9 | 0,887 |
Обращает на себя внимание отсутствие легочных и раневых осложнений, более раннее восстановление работы кишечника, отсутствие летальных исходов у больных основной группы и снижение уровня рецидива грыж в отдаленные сроки наблюдения с 2,7 до 1,9%. Учитывая, что структура основной группы по величине и рецидивности грыж является более сложной, полученные результаты можно считать объективными.
Заключение
При изучении результатов герниопластики с применением эксплантата, обработанного по методике «Абактолат», гнойные раневые осложнения отмечены у 5 больных (2,1%). Рецидив грыжи наступил у 6 больных (2,7%), в число которых вошли все 5 больных, имевших нагноения. При повторных операциях установлено неполное прилегание краев трансплантата к апоневротическому слою брюшной стенки, отмечено неравномерное распределение рубцовой соединительной ткани по всей поверхности трансплантата, не имевшей направленной структуры соединительнотканных волокон, что можно считать основными причинами развития рецидива заболевания.
Разработанная методика эксплантационной герниопластики протезом «Абактолат» с аппликацией в ячейки сетки диспергированного биоматериала Аллоплант и фиксацией его медицинским клеем «Сульфакрилат» технически проста и не увеличивает продолжительность операции.
Имплантация трансплантата с использованием аллогенного диспергированного биоматериала, сопровождается менее интенсивной и менее продолжительной воспалительной фазой, более короткими сроками формирования плотной оформленной соединительной ткани вокруг отдельных участков протеза, ранним созреванием соединительной ткани с упорядочиванием коллагеновых волокон и циркулярной их ориентацией вокруг отдельных участков сетки в сравнении с применением эксплантата, обработанного по методике «Абактолат».
Применение разработанной методики хирургического лечения больных сложными дефектами брюшной стенки с применением эксплантата, обработанного ДБМА и фиксированного медицинским клеем «Сульфакрилат», позволило предотвратить развитие гнойных раневых осложнений и уменьшить рецидив грыж до 1,9%.
Практические рекомендации
При герниопластике с применением сетчатых синтетических протезов целесообразно применение разработанного нами способа аппликации в ячейки протеза диспергированного биоматериала Аллоплант и фиксации его медицинским клеем «Сульфакрилат».
Все операции необходимо завершать установкой 1 или нескольких вакуумренажных трубок и удалять их на 3–4 сутки послеоперационного периода. При образовании особо значительных по величине подкожных карманов следует применять способ наложения сквозных провизорных швов, завязываемых на марлевых шариках поверх кожи с целью ликвидации полостей.
Наличие элементов диспергированного биоматериала Аллоплант и стерильность отделяемого из вакуум-дренажных трубок следует проводить в сроки до 4 суток послеоперационного периода под контролем цитологии экссудата и УЗИ.
Диспансерное наблюдение за пациентами, оперированными с применением разработанной методики, необходимо осуществлять в сроки до 3-х лет после выписки, путем приглашения на осмотр в клинику.
Литература
- Шавалеев, Р.Р. Применение сетчатого эксплантата с антибактериальным действием в хирургии сложных форм паховых грыж / Р.Р. Шавалеев, Д.В. Феоктистов // Материалы 67-й Республиканской итоговой научнопрактической конференции студентов и молодых ученых Республики Башкортостан. – Уфа, 2002. – С. 72–73.
- Юнусов, В.М. Новые пластические материалы в хирургии сложных дефектов передней брюшной стенки / В.М. Юнусов, Р.Р. Шавалеев // Материалы 67-й Республиканской итоговой научно-практической конференции студентов и молодых ученых Республики Башкортостан. – Уфа, 2002. – С. 79–80.
- Шавалеев, Р.Р. Профилактика отторжений трансплантатов при герниопластике / Р.Р. Шавалеев, Т.Ш. Хакамов, Х.М. Белхароева // Вопросы теоретической и практической медицины: материалы 72-й итоговой Респ. науч. конференции студентов и молодых ученых. – Уфа, 2007. – С. 306–307.
- Корнилаев, П.Г. Новые технологии в трансплантационной герниопластике / П.Г. Корнилаев, Р.Р. Шавалеев // Научный прорыв 2007: сборник научных трудов конференции ученых Республики Башкортостан, посвященной Году 450-летия Единства Башкортостана с Россией, 75-летию БГМУ, Дню Республики. – Уфа, 2007. – С. 91–92.
- Корнилаев, П.Г. Экспериментально-морфологическое обоснование применения диспергированного биоматериала Аллоплант в трансплантационной герниопластике // П.Г. Корнилаев, Р.Р. Шавалеев, Л.А. Мусина // Морфологические ведомости. – 2009. – № 3: Клиническая анатомия и экспериментальная хирургия в 21 веке: труды Всероссийской научной конференции (14–16 октября 2009 г., Оренбург). – С. 202–203.
- Корнилаев, П.Г. Хирургическая реабилитация больных вентральными грыжами / П.Г. Корнилаев, Р.Р. Шавалеев, Т.Ш. Хакамов // Международный журнал по иммунореабилитации. – 2009. – Т. 11, № 1. – С. 100–101.
- Корнилаев, П.Г. Применение биостимулятора Аллоплант в трансплантационной герниопластике / П.Г. Корнилаев, Р.Р. Шавалеев, Д.В. Феоктистов // Медицинский вестник Башкортостана. – 2009. – Т. 4, № 6. – С. 105–107.
- Способ эксплантационной герниопластики с применением биоматериала Аллоплант: пат. № 2365344 / Корнилаев П.Г., Плечев В.В., Шавалеев Р.Р., Феоктистов Д.В. // Изобретения полезные модели: официальный бюллетень федеральной службы по интеллектуальной собственности, патентам и товарным знакам. – М., 2009. – № 24. – С. 1.
- Морфологическая картина воспринимающего ложа на фоне применения диспергированного биоматериала Аллоплант в трансплантационной герниопластике / Корнилаев П.Г., Шавалеев Р.Р., Мусина Л.А., Феоктистов Д.В. // Медицинский вестник Башкортостана. – 2010. Т. 5, № 3. – С. 64–66.
к содержанию | опубликовать статью
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ НЕДОСТАТОЧНОСТИ ЗАМЫКАТЕЛЬНОГО АППАРАТА ПРЯМОЙ КИШКИ С ПРИМЕНЕНИЕМ БИОМАТЕРИАЛОВ АЛЛОПЛАНТ
Булгаков А. В., Мулдашев Э.Р.
ГБОУ ВПО «Башкирский государственный медицинский университет Министерства здравоохранения и социального развития Российской Федерации»
ФГБУ Всеросийский центр глазной и пластической хирургии Минздравсоцразвития России
Разработан новый способ передней леваторопластики с формированием сухожильного центра промежности под названием " Способ хирургического лечения последствий послеродовых травм промежности". А.С. №15020I3 от 28.08.1989 Бюл. №3I. Впервые в пластической проктологии использованы аллотрансплантаты для восстановления анатомических структур ЗАПК. Аргументирована необходимость индивидуального подбора биоматериаловов для восстановления ЗАПК в зависимости от объема, локализации и характера повреждения. Доказана надежная приживляемость имплантированных биоматериалов.
Актуальность Недостаточность замыкательного аппарата прямой кишки (НЗАПК) относится к числу заболеваний, которые не только приносят человеку физические страдания, но и приводят его к социальной изоляции. При этом недуге больной, находясь в полном расцвете сил и сохраняя трудоспособность, исключается из активной трудовой деятельности и становится нетерпимым даже в быту. Поэтому возвращение к труду и полноценной жизни этого контингента больных приобретает социально-экономическое значение.
НЗАПК встречается в 7-9% всех проктологических больных / Аминев A.M., 1963; Федоров В.Д.,1978; Дульцев Ю.В.,1981; Gabriel W. B., 1963; Collins C.D.,1969/. Этот термин подразумевает более широкие нозологические формы, проявляющиеся не только симптомокомплексом анальной инконтененции, но и недостаточностью мышц тазового дна, выпадением прямой кишки, ректоцелле / Даниэль-Бек К.В.,1958; Канделис В.Л.,1972; Волков А.В.,1982; Goligher J. С . 1975; Keighley M.R. I984 /.
Среди различных форм НЗАПК наибольший удельный вес приходится на травматическую недостаточность анальных сфинктеров - 60-75% / Усков А.Г. ,1974; Калаев Т.Н., 1985; Corman M.L.,I985; Реzini M.E., 1987 /.
Применение любого способа лечения, выполненного без учета индивидуальных особенностей состояния анальных сфинктеров, состояния тазового дна, приводило к тому, что у 40-60% больных отмечались неудовлетворительные результаты /Федоров В.Д. ,1979; Саламов К.Н., Г980; Дульцев Ю.В.,1981; Процента В.М.,1987; Duhamel B., I983 /.Столь высокий процент объясняется не только выбором неадекватного способа лечения, но и, в значительной степени, отсутствием материалов, обладающих стойкими фиксирующими свойствами и способностью замещения объемных дефектов тканей промежности и ее перегородки.
В этой связи теоретически значимым представляется применение нового способа передней леваторопластики с использованием для восстановления сухожильного центра промежности биоматериалов Аллоплант для регенеративной хирургии. Именно это и предопределило актуальность данного исследования.
Цель исследования. Данная работа проводилась с целью уменьшения рецидивов НЗАПК после оперативной коррекции и улучшения результатов операции.
Материалы и методы исследования
Клиническая характеристика больных и методы исследования
Клинические исследования проведены на 168 пациентах, из которых у 50 проведены операции традиционными способами. Среди всех оперированных больных женщин было 151 (89,9%). Возраст больных колебался от 11 до 72 лет. Средний возраст женщин составлял 34 года, мужчин 40 лет.
Наиболее частой причиной НЗАПК явились послеродовые травмы промежности, а именно: разрывы промежности, ректо-вагинальные свищи, ректоцелле, травмы мышц и связочного аппарата тазового дна (92,3%).
Пациенты с рецидивами инконтененции составили 18 человек; с объемными дефектами ректо-вагинальной перегородки в виде ее перерастяжения при ректоцелле, отсутствием части ее при ректо-вагинальных свищах и послеродовых разрывах промежности -135 (80,4%).
При этом виде сочетанных поражений требовалось произвести не только мышечную коррекцию, но и укрепить ректо-вагинальную перегородку трансплантатами.
Все больные в порядке утяжеления симптомокомплекса инконтененции, разделены на следующие группы: I.Ректоцелле -26 человек; 2.Травматическая недостаточность сфинктеров -13 человек; 3.Послеродовые разрывы промежности -70 человек; 4.Ректо-ваги-нальные свищи -44 человека: 5. Недостаточность мышц тазового дна с выпадением прямой кишки и анальной инконтененцией- 15 человек.
1 группа. В большинстве случаев ректоцелле сопровождалось не только повреждением и расхождением лонно-ректальной мышцы, но и слабостью анальных сфинктеров. В трех случаях - наблюдалась слабость связочного аппарата матки, тазового дна в виде выпадения матки, влагалища, цистоцелле. Особенностью этой группы явился более зрелый возраст, старше 50 лет, что имело значение в состоянии фибро-эластического аппарата тазового дна и прямой кишки. После многократных родовых травм, возрастных изменений в тканях, тазовое дно - перерастянуто, апоневроз Денонвилье - истончен, мышечный тонус - ослаблен. Такие больные требовали более объемных оперативных вмешательств.
2 группа. В эту группу отнесены обширные травмы анальных сфинктеров на протяжении с Рубцовыми изменениями мышц. Она характеризовалась неоднократно проведенными ранее пластическими операциями, направленными на коррекцию анальных сфинктеров.
3 группа. Больные с послеродовыми разрывами промежности с недостаточностью сфинктеров составила наиболее многочисленную группу. Характерной чертой этой группы явилось нарушение сухожильного центра промежности с разрывом лонно-ректальной порции леваторов. У 42 больных дефекты промежностной перегородки достигали от 2 до 5 см. Наряду с этим, отмечалось истончение оставшейся ректо-вагинальной перегородки, что способствовало пролапсу стенок прямой кишки и влагалища.
4 группа. Группа пациентов с ректо-вагинальными свищами характеризовалась наиболее высоким процентом /28,13 %/ больных неоднократно перенесших пластические операции. В 84,1% ректо-вагинальные свищи сопровождались недостаточностью анальных сфинктеров 2-3 степени, что требовало обязательной коррекции их. Сложность и риск оперативного вмешательства были прямо пропорциональны величине дефекта ректо-вагинальной перегородки, высоте расположения свища, толщине перегородки. У 2-х больных ректо-вагинальные свищи сформировались после кольпопоэза из брюшины. Этим пациентам требовалась не только пластика свища, но и одновременно - формирование влагалища.
5 группа. Больные с недостаточностью мышц тазового дна, замыкательного аппарата прямой кишки и выпадением прямой кишки явились наиболее сложным контингентом в восстановительном плане. Фаза декомпенсации выпадения наблюдалась у 13 больных. Эта группа пациентов требовала коррекции ЗАПК на нескольких уровнях.
Согласно классификации НИИ проктологии МЗ РСФСР, больные с НЗАПК были: по форме- с органическими изменениями ЗАПК; по этиологии - травматическими поражениями; по степени выраженности разрыва промежности П1-1У степени, ректоцелле-П-Ш степени, инконтененции -2-2 степени. По локализации нарушения мышечных структур: передняя, боковая, задняя. По протяженности - от 1/4 до 1/2 окружности включительно. По уровню: сфинктеры, мышцы тазового дна, фиброзный каркас тазового дна.
При поступлении больным проводили общеклинические, биохимические исследования. Исследовали состояние сердечно-сосудистой системы. Иммунологический статус после имплантации аллотрансплантатов определялся реакцией пассивной гемоаглютинацки /ГОТА/ по Бойдену с эритроцитарным диагностикумом. В сыворотке крови титр антител не превысил 17+ 0,18, при Р=0,01, что свидетельствовало об отсутствии гуморального иммунного ответа на трансплантат.
Кроме того, для оценки функционального состояния ЗАПК проводили сфинктерометрию по A.M. Аминеву. Показатели ее исчислялись: тоническое от 40,33+14,16 до 258,00+34,82 ; максимальное от 49,00+17,04 до 340,00±40,00 ; волевое от 8,67+4,35 до 82,00+10,62 при Р= 0,05.
Показатели сфинктероманометрии варьировали: в покое от 35,25+9,25 до 198,14+20,10 мм вод.ст.; при сокращении от 43,50+11,44 до 246,14+19,58 мм вод.ст., при Р=0,05.
Эксперименты на животных проводились на 17 кроликах, которым расщеплением ректо-вагинальной перегородки создавалась модель "ложа" для имплантации биоматериалов. Животные выводились из эксперимента в различные сроки. Ткани ректо-вагинальной перегородки после аллотрансплантации подвергались гистологическому анализу через 2-3 недели,1,2,6,12 месяцев.
Характеристика и свойства аллотрансплантатов. Известно применение аллотрансплантатов соединительно-тканной природы в челюстно-лицевой хирургии и офтальмохирургии. Наиболее полно отвечают требованиям хирургии следующие аллотрансплантаты: аллосухожильные нити для хирургии, биоматериал для каркасной пластики, Аллоплант для коррекции немышечных дефектов промежности. Производство их налажено в лаборатории биоматериалов Всероссийского центра глазной и пластической хирургии в г.Уфе.
Аллосухожильные нити для хирургии обладают способностью удерживать ткани в сильно натянутом состоянии, не прорезаясь через них. Сравнительные биомеханические исследования показали, что аллосухожильные нити по прочности несколько превышают прочность шелка, почти в 1,5 раза прочнее кетгута и в 5-6 раз прочнее нитей, изготовленных из сухожилий других локализаций. Аллосухожильные нити мало растяжимы: относительное удлинение в среднем составляет 17%, в то время они го гибкости подобны шелку, хорошо удерживаются в узле. Сравнительные экспериментально-морфологические исследования на лабораторных животных /кроликах/ показали, что сроки рассасывания аллосухожильных нитей 1-2 года. Потеря прочности на 20% у аллосухожильных нитей наступает на 14-2I сутки и в течение всего остального срока адаптации и рассасывания аллосухожилъных нитей почти не меняется.
Аллоплант для коррекции немышечных объемных дефектов промежности представляет собой консервированный биологический материал, получаемый на основе донорской дермы и жировой клетчатки, характеризующийся способностью к хорошему приживлению, длительному рассасыванию и замещению собственной соединительной тканью реципиента со стойкими восстановлением объемных параметров замещаемой области. Обладает особенностью строения: сильно развита соединительнотканная строма, обеспечивая ей каркасные свойства и хорошую моделируемость трансплантата. В ячейках стромы располагаются жировые дольки. Последние обильно васкуляризированы, строма имеет многочисленные мало и бессосудистые зoны. Аллоплант для коррекции немышечных объемных дефектов промежности тканей имеет следующие преимущества, позволяющие широко использовать в пластической хирургии: хорошая моделируемость, прочность шовной фиксации, хорошая вживляемость, низкие антигенные свойства.
Биоматериал для каркасной пластики представляет собой консервированный аллогенный материал, по своим структурным биомеханическим свойствам наиболее оптимальный для выполнения опорной и каркасной пластики. Биомеханические исследования показали, что прорезыванию данного биоматериала швами из аллосухожильных нитей толщиной 3/0 не происходит даже при нагрузке 7,5 кг. В сравнении, например, с аллогенной твердой мозговой оболочкой, прорезывание которой теми же швами наблюдается при нагрузке 1,75 кг.
РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
Экспериментальные исследования Гистологически через 2-3 недели биоматериалы сохраняют свою фиброструктуру. Вокруг них - небольшой отек и клеточный инфильтрат. Сосуды микроциркулярного русла тканевого ложа расширены, выявляются умеренно выраженные периваскулиты. Клеточный инфильтрат состоит преимущественно из нейтрофилов, лимфоидных клеток фибробластического ряда.
Через 1-2 месяца отмечается умеренный отек, набухание волокон, интенсивная пикринофилия, аргентофилия. Тяжи фибробластов и новообразованных капилляров врастают в межпучковое пространство трансплантатов. Процессы замещения более интенсивные в аллосухожильных нитях. Тканевое ложе представлено хорошо васкуляризированной соединительной тканью. В прилежащей собственно дерме кожи выявляется слабо выраженная сосудистая реакция, умеренные периваскулиты, слабая инфильтрация ложа лимфоидными клетками, макрофагами и недифференцированными клетками фибро-бластического ряда.
Через 3 месяца трансплантаты интимно сращены с окружающей слизистой тканью и мышцей, но полностью не замещены. В толще пучков и между пучками определяется ярко-красная сеть фуксиновых волокон и врастающие тяжи фибробластов. Биоматериал для каркасной пластики фрагментирован врастающими тяжами новообразованной соединительной ткани. Весь трансплантат инфильтрирован фибробластами. В тканевом ложе трансплантатов и в прилежащей ткани отмечается интенсивный фибриллогенез и умеренная сосудистая реакция с незначительными периваскулитами.
Через 6 месяцев процессу замещения трансплантатов новообразованной соединительной тканью выражены более интенсивно.
Через год на месте имплантация аллосухожильных нитей и биоматериала для каркасной пластики образовался хорошо васкуляризированный регенерат. Аллосухожильные нити имеют однонаправленный характер хода коллагеновых волокон, различной степени зрелости. Фиброархитектоника регенерата на месте имплантации биоматериала для каркасной пластики практически не отличается от окружающей ткани. Вокруг регенерата тонкая прослойка соединительнотканной капсулы, обеспечивающая плотное сращение более рыхлого регенерата с окружающей тканью.
Таким образом, экспериментально-морфологические исследования показывают, что изученные биоматериалы в ранние сроки приживления вызывают умеренную воспалительную реакцию и сращены с тканевым ложем. Сами биоматериалы замещаются медленно в течение года, в результате чего их прочностные свойства не изменяются на всем процессе замещения.
Клинические исследования. В хирургическом лечении НЗАПК с применением биоматериалов выполнялись три основных принципа:
- Учет объема и уровня повреждения структур.
- Тщательный подбор объемозамещающих, фиксирующих аллопластических материалов с целью оптимального замещения и коррекции замыкательного аппарата.
- Максимальное восстановление поврежденных анатомических структур.
Опираясь на свойства биоматериалов и экспериментальные данные, разработан новый способ леваторопластики с восстановлением сухожильного центра промежности - А.С. №1502013 от 28.08.89года, Бюл.№31. "Способ хирургического лечения последствий послеродовых травм промежности".
Способ осуществляется следующим образом: делают поперечный разрез истонченной промежностной перегородки, длиной 4-5сы. Острым путем "расщепляют" промежностную перегородку на глубину 8-9 см. Обнажают сохранившиеся в передне-боковых отделах лонно-ректальные порции леваторов. Средней режущей иглой проводят аллосухожильные нити, начиная из глубины раны, через нижние слои обнаженных леваторов по обеим сторонам. Интервал между швами 20-25 мм. Аллосухожильные нити поочередно связывают, но не срезают. Для фиксации достаточно 3-4 нитей, толщиной 2-3 мм, длиной 200мм. По величине мышечного дефекта промежностной перегородки формируют пластину из биоматериала для каркасной пластики, которая будет использована в качестве каркаса в среднем его размеры 50x20x2,5.Аллосухожильные нити проводят режущей иглой через биоматериал для каркасной пластики, отступя 3-4 мм от средней линии последнего, соответственно по углам первоначального лигирования. Трансплантат укладывают на ранее ушитые леваторы. В последующем, поочередно, начиная из глубины раны, аллосухожильные нити проводят через верхне-боковые слои оставшихся леваторов. Сухожильные полосы поочередно связывают до сопоставления лонно-ректальных порций леваторов с обеих сторон. Анальные сфинктеры, после их адаптации ушивают аллосухожильными нитями.
Положительный эффект достигается за счет применения стабильной фиксации перемещенных мышц с помощью биоматериала для каркасной пластики и аллосухожильных нитей. Биоматериал, в данном случае, выполняет каркасную роль. В сочетании с фиксацией смещенных леваторов аллосухожильными нитями, стойкими к рассасыванию, новый способ позволяет восстановить разрушенный сухо жильный центр промежности и укрепить более физиологичной тканью слабое место тазовой диафрагмы. В результате этого достигается стабильная фиксация, так как лонно-ректальная порция леваторов, уложенная поверх и снизу биоматериала для каркасной пластики и фиксированная к ней алло сухожильными нитями, прочно остается в этом положении в связи с уменьшением сил растяжения мышц за счет передачи их на биоматериал для каркасной пластики. Для ускорения процесса васкуляризации биоматериала для каркасной пластики, регенерации его и фиксации к нему леваторов, биоматериал укрывают со всех сторон хорошо кровоснабженными нерасщепленными мышцами. В конечном итоге быстрая васкуляризация тканей способствует уменьшению атрофии перемещенных мышц и увеличению силы мышечного сокращения за счет общего увеличения мышечной массы. Биоматериал для каркасной пластики предупреждает прорезывание швов. Данный способ леваторопластики целесообразно применять для пластики послеродовых разрывов промежности с недостаточностью сфинктеров, для пластики ректо-вагинальных свищей любых диаметров, сочетанных с мышечным дефектом, для пластики ректоцелле.
Кроме того, при истончении ректо-вагинальной перегородки для ее укрепления использовали Аллоплант для коррекции немышечных объемных дефектов промежности, который фиксировали к леваторам аллосухожилиями /Рац. предложение "Способ хирургического лечения ректоцелле" от 4.11,89 года/.
При выпадении прямой кишки в сочетании со слабостью мышц тазового дна потребовалась коррекция на нескольких уровнях, включая и внутрибрюшинную фиксацию ее. Важным дополнением комбинированной операции явилось формирование анального канала передне-задней сфинктеролеваторопластикой в сочетании с имллантацией в супралеваторное пространство объемного биоматериала в симметричных областях. Таким образом, добивались щелевидной формы проксимального отдела анального канала. При сокращении леваторов достигался дополнительный супралеваторный механизм замыкания за счет улучшения герметичности в проксимального отдела анального канала /Рац.предложение "Лечение недостаточности замыкательного аппарата прямой кишки" от 6.12.89 года/. Хирургическая коррекция НЗАПК проведена 168 дольным, из них 118 больным - с биоматериалами, 50- традиционными способами.
При ректоцелле выполнены следующие оперативные вмешательства: имплантация Аллопланта для коррекции немышечных объемных дефектов промежности в расщепленную ректо-вагинальную перегородку, кольпоррафия, сфинктеролеваторопластика, кольпоррафия, передняя сфинктеролеваторопластика с укреплением аллосухожилями, передняя леваторопластика.
При коррекции послеродовых разрывов промежности проведены: передняя сфинктеролеваторопластика с фиксацией мышц аллосухожилиями, передняя леваторопластика по-нашему способу-10; сфинктеролеваторопластика с укреплением промежностной перегородки объемными биоматериалами и фиксацией мышц аллосухожилиями; передняя сфинктеролеваторопластика по Тэт Лоусон в модификации НИИ проктологии.
При хирургической коррекции ректо-вагинальных свищей выполнены: передняя сфинктеролеваторопластика с фиксацией аллосухожилиями; рассечение, расщепление промежностной перегородки, сфинктеролеваторопластика с фиксацией аллосухожиллями; рассечение, расщепление промежностной перегородки, имплантация объемного аллотрансплантата, сфинктеролеваторопластика о фиксацией аллосухожилием; передняя леваторопластика по нашему способу; послойное ушивание свища; пластика свища с низведением слизистой.
При коррекция анальных сфинктеров проведены следующие операции: сфинктеропластика с ушиванием кетгутом, дексоном; сфинктеропластика с фиксацией аллосухожилием; переднезадняя сфинктеролеваторопластика с фиксацией аллосухожилиями на фоне выведенной сигмостомы.
При хирургическом лечении выпадения прямой кишки проведены внутрибрюшинная фиксация прямой кишки, передняя и задняя сфинктеролеваторопластика с фиксацией аллосухожилиями; передняя, задняя сфинктеролеваторопластика с фиксацией аллосухожилиями и имплантацией аллопланта для коррекции периферических нервов в супралеваторное пространство, стенозирующая операция типа Тирша.
Исходы лечения Непосредственные результаты лечения НЗАПК у больных, коррегированных биоматериалами, характеризовались более благоприятными данными: количество послеоперационных осложнений снизилось более чем вдвое / 39 и 15 /, рецидивы уменьшились с 17% до 3,5%. Хорошие и удовлетворительные результаты отмечены в 96,6% при применении биоматериалов, по сравнению с 67,9% - традиционными способами.
Данные функционального исследования свидетельствуют о преимуществах биоматериалов. Так, например, максимальное сокращение при сфинктерометрии возросло с 315,00+21,72 до 500,00+30,86 при Р=0,05. прирост силы максимального сокращения составил 90,2%по сравнению с 89,8% при обычных способах пластики. Сфинктероманометрия: при сокращении с 255,88+ 29,57 до 489,75+29,43 мм вод.ст. при Р=0,05. Прирост составил при применении биоматериалов 91% по сравнению с 82,4%.
Заключение
Посттравматическая недостаточность замыкательного аппарата прямой кишки в 93,5% обусловлена объемными дефектами тканей, потерей фиброэластических свойств каркаса прямой кишки, степень которых зависит от характера травмы, локализации и объема дефекта. Они наиболее выражены при перерастяжении и разрыве мышц, сухожильного центра промежности в родах.
Аллосухожильные нити, рассасывающиеся в течение 2 лет, являются наиболее надежным фиксирующим материалом при передней леваторопластике с формированием каркаса из биоматериала для каркасной пластики по нашей методике, а также радикальным вариантом восстановления сухожильного центра промежности.
Биоматериалы вызывают умеренную воспалительную реакцию с образованием в окружающих тканях соединительнотканной капсулы и окончательно замещаются без отторжения в течение 2 лет.
Изучение ближайших и отдаленных результатов лечения больных с недостаточностью замыкательного аппарата прямой кишки, коррегированных биоматериалами Аллоплант, показало, что количество послеоперационных осложнений уменьшилось на 50%, рецидивы снизились с I8% до 3,5%, полное восстановление функции замыкательного аппарата прямой кишки наблюдали у 96,6% в сравнении с 67,9% пациентов, оперированных без биоматериалов.
Практические рекомендации
Учитывая, что НЗАПК обусловлена объемными дефектами тканей, потерей фибро-эластических свойств каркаса прямой кишки, с целью уменьшения послеоперационных осложнений и улучшения результатов операции, можно рекомендовать:
1. Целесообразно рассматривать НЗАПК как "поломку" на нескольких уровнях и требующую в каждом случае индивидуального подхода к коррекции.
2. Для замещения дефектов тканей ректо-вагинальной перегородки следует использовать Аллоплант для коррекции немышечных объемных дефектов промежности соединительнотканной природы.
3. Для фиксации мышц, подверженных нагрузке, могут быть использованы аллосухожильные нити для хирургии, которые являются для этого наиболее оптимальным вариантом.
4. При передней леваторопластике целесообразно формировать сухожильный центр промежности по нашему способу.
5. Опираясь на свойства биоматериалов в послеоперационном периоде допустимо более активное ведение больных.
Литература
- Хирургическое лечение недостаточности замыкательного аппарата прямой кишки с применением биоматериалов// Актуальные вопросы проктологии: Тез. докл. Всесоюз. конф.- Киев,1989.-197-199.
- Лечение ректо-вагинальных свищей //Актуальные вопросы проктологии:Тез.докл.Всероссийской конф.-г.Уфа,1987.-79.
- Способ хирургического лечения последствий послеродовых травм промежности //А.С.№1502013 от 22 апр.1989,Бюл.«31,89.
- Хирургическое лечение недостаточности замыкательного аппарата прямой кишки с применением аллопластических материалов// Актуальные вопросы хирургии сердечно-сосудистой системы и отдельных областей: Тез.докл.ХУ1 конф.хирургов БАССР.- г.Уфа, 1989.-74-76.
к содержанию | опубликовать статью
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ЭХИНОКОККОЗА ЛЕГКИХ У ДЕТЕЙ
Гумеров М. И., Гумеров А.А., Ишимов Ш.С, Мамлеев И.А.
ГБУЗ Республиканская детская клиническая больница, (г. Уфа)
Автором разработана методика проведения эхографии грудной клетки у детей с эхинококкозом легких. Описаны эхографическая семиотика, а также особенности эхографической картины эхинококковых кист в легком в зависимости от стадии развития паразита и характера осложнений. Научно обоснована необходимость и продолжительность предоперационной подготовки и послеоперационного ведения при осложненном эхинококкозе легких. Разработан и внедрен в практику метод видеоторакоскопической эхинококкэктомии у детей с неосложненным эхинококкозом легких.
Список сокращений
- БДС – большой дуоденальный сосок
- ЖВП – желчевыводящие пути
- ЖКБ - желчнокаменная болезнь
- СТД - сменный транспеченочный дренаж
Актуальность Эхинококкоз является тяжелым распространенным паразитарным заболеванием и продолжает оставаться серьезной медицинской и народнохозяйственной проблемой во многих странах мира, в том числе и в Республике Башкортостан (Ишимов Ш.С. и соавт., 1995; Шамсиев A.M.и соавт., 1999; Поляков В.Е. и соавт.,2002; Keshmir M et al., 1999; By Muharren et al., 2000; Prisday et al., 2000). В связи с неблагоприятной санитарно-эпидемиологической обстановкой и улучшением диагностики число больных с эхинококкозом ежегодно увеличивается. (Магомедов С.З., 2000).
Полиморфизм клинических проявлений эхинококкоза легких (ЭЛ) создает трудности для своевременного выявления данной категории больных. Это порождает немало ошибок и осложнений, частота которых колеблется от 26 до 52% (Исламбеков Э.С. и соавт., 2000; Dogan R et al., 1989; Kennedy D., Sharma O.P., 1990). Больные подвергаются многократному обследованию и лечению в различных лечебных учреждениях. Нередко заболевание расценивается как деструктивная пневмония, экссудативный плеврит, абсцесс легкого, пиопневмоторакс (Пулатов А.Т., 1998; Gouliamos A.D. et al., 1991; Skerrett S.J., Plarill J., 1992).
Основным методом диагностики ЭЛ является рентгенологический. Однако многообразие рентгенологической картины, особенно при осложненном эхинококкозе легких, вызывает большие диагностические трудности. Повторное исследование ведет к возрастанию лучевой нагрузки. Поэтому поиск щадящих методов исследования представляется весьма актуальным (Ч.Б. Кулиев и соавт., 2000; Каплун С.С. и соавт. 2000).
В этом плане перспективным является метод эхографии. Целесообразность его использования в педиатрической практике была доказана при острой деструктивной пневмонии, плеврите (Дворяковский И.В., и соавт., 1988; Гумеров Р.А., 2000;Васильева Н.П. и соавт., 2001).
В литературе продолжается дискуссия по поводу продолжительности и объема предоперационной подготовки больных при осложненном эхинококкозе легких у детей (Султанов Ф.Ш., 1998; Рахимов Р.С. и соавт., 2001; Исламбеков Э.С. и соавт., 2000;).
Несмотря на значительное количество работ, посвященных хирургическому лечению ЭЛ, на сегодняшний день проблема оперативного лечения ЭЛ у детей еще далека от своего окончательного решения (Аскеранов Г. О. и соавт., 2000; Пулатов А.Т. 2001).
В последние годы в литературе появляются сообщения единичных авторов о видеоторакоскопической эхинококкэктомии легких у взрослых больных (Кротов Н.Ф. и соавт., 1999-2000; Prisadov G et al, 2000).
У детей практически не изучена возможность торакоскопического лечения ЭЛ, не разработана методика видеоторакоскопической операции, не определены показания и противопоказания к ее выполнению.
Все вышеизложенное послужило поводом для углубленного изучения вопросов, направленных на улучшение диагностики и хирургического лечения эхинококкоза у детей.
Целью работы явилось улучшение результатов лечения эхинококкоза легких у детей путем совершенствования диагностики и хирургического лечения.
Материал и методы исследования
Клиническая характеристика больных Для выполнения поставленной цели нами проанализированы результаты лечения 103 детей с эхинококкозом легких, находившихся в клинике детской хирургии Башкирского государственного медицинского университета на базе Республиканской детской клинической больницы за период 1980-2001гг. Возврат больных колебался от 1 года до 15 лет.
Основное количество детей с эхинококкозом легких оказалось в возрасте от 10 до 14 лет (49,5%). Мальчиков было в 2,5 раза больше (69,9%), чем девочек (30,1%). Правое легкое поражено эхинококкозом чаще (60,2%), чем левое легкое (39,8%).
В большинстве случаев встречались одиночные кисты (84,5%), множественные кисты имели 15,5% детей. Двустороннее поражение эхинококком отмечено у 13 (12,6%о) детей. У 19 (17,4%) пациентов эхинококкоз легкого сочетался с поражением печени. Чаще наблюдались гигантские кисты -40,8%, средние - 39,5%, реже малые кисты - 23,9%.
По расположению в ткани легкого чаще отмечалось центральное расположение кист (65,1%), это относилось в основном к большим и средним кистам (табл. 1).
| Размер кисты | Расположение кист | ||
|---|---|---|---|
| центральное | периферическое | Всего | |
| Малые | 5 | 19 | 24 (23,3%) |
| Средние | 21 | 16 | 37 (35,9%) |
| Большие и гигантские | 41 | 1 | 42 (40,81%) |
| Итого | 67 (65,1%) | 36 (34,9%) | 103 (100%) |
К малым отнесены кисты, локализующиеся от поверхности паренхимы легкого на глубине более 2 см и выступающие из - под паренхимы не более чем на 1/3.
К периферическим относили малые кисты, покрытые легочной тканью толщиной менее 2 см, или фиброзная капсула которых видна на поверхности легкого, а также кисты, выступающие из под паренхимы легкого более чем на 1/3 часть.
Кроме клинико-лабораторных методов исследования использовались: обзорная рентгенография грудной клетки и брюшной полости, ультразвуковое исследование.
Эхография грудной клетки детям с подозрением на эхинококк легкого проводили на эхокамерах "SSD - 2000", "SSD- 500" фирмы Aloka (Япония) конвексными и линейными датчиками частотой 3,5; 5 и 7,5 МГц без предварительной подготовки больного.
Обследование проводили в положение больного лежа, на спине, животе правом и левом боку, сидя.
Продольные срезы осуществляли по стандартным топографо-анатомическим линиям (околопозвоночным, лопаточным, подмышечным, среднеключичным и окологрудинным) сначала конвексным датчиком частотой 5,0 МГц. При выявлении патологического очага для его детализации проводили поперечные, продольные и косые срезы под различными углами линейным датчиком частотой 7,5 МГц.
Исследование начинали от нижних межреберий в направлении снизу вверх. Верхние отделы легких визуализировали из над - и подключичных ямок с использованием различных углов ввода луча. Для выявления патологии нижних отделов легких и плевральных полостей в качестве акустического окна использовали печень и селезенку. Для этого датчик устанавливали субкостально с максимальным наклоном оси сканирования вверх и ориентацией ультразвукового луча в область плеча одноименной стороны, что позволяло оценить наддиафрагмальное пространство. Далее он становился продольно по средней подмышечной линии с обеих сторон, что также позволяло отчетливо визуализировать базальные отделы легких и плевральных полостей. Исследование проводили при спокойном дыхании ребенка, при необходимости - на глубине вдоха.
Статистическую обработку данных проводили методом сравнения средних показателей с использованием t- критерия Стьюдента - Фипера и вычисления коэффициента линейной корреляции Пирсона (г). Статистический анализ проводили с использованием пакета компьютерных программ MS Excel 5,0 .
Результаты исследования и их обсуждение
Как и большинство авторов (Пулатов A.T., 1983; Аскеров Г.Р. и соавт., 2000; Гаджимирзаев ГА. и соавт., 2000) мы придерживаемся деления клинического течения ЭЛ на 3 стадии по А.В. Мельникову (1935).
Бессимптомное течение ЭЛ отмечено нами у 16 (16,7%) детей. Однако у 9 больных нам удалось выявить скрытые симптомы, незамеченные лечащими врачами: периодически возникающие кратковременные боли в грудной клетке, ухудшение аппетита, кашель, недомогание, потливость.
Основными жалобами во второй стадии заболевания в 47 наблюдениях (45,6%) были боли в грудной клетке на стороне поражения различной интенсивности, усиливающиеся при подвижных играх и физической нагрузке. У 17 пациентов отмечался упорный сухой кашель, который плохо поддавался медикаментозной терапии. У трети детей наблюдали аллергические проявления. Следует отметить, что пациенты нередко отмечали снижение аппетита, общую слабость, повышенную утомляемость, потливость.
Среди 103 пациентов с ЭЛ в 40 (38,7%) случаях диагностированы различные осложнения, из них наиболее часто (23 детей) наблюдали прорыв кисты в бронх. У 12 больных отмечалось нагноение без перфорации хитиновой оболочки, у 5 больных - прорыв в плевральную полость.
Клиническое проявление прорыва эхинококкоза в бронх сопровождалось повышением температуры тела до 38-39° С, приступом сильного кашля с выделением большого количества прозрачной или мутной жидкости с обрывками хитиновой оболочки вместе с мокротой. Провоцирующим моментом прорыва кисты в бронх в большинстве случае были простудные заболевания, травма грудной клетки (падение с небольшой высоты, прыжки).
Нагноения кисты (12) характеризовались признаками острого воспалительного процесса. Дети жаловались на повышение температуры тела (до 38-39 С), сухой кашель, боли в пораженной стороне грудной клетки, усиливающиеся при глубоком дыхании, общую слабость, отсутствие аппетита.
Прорыв эхинококковой кисты легкого в плевральную полость развивается остро и проявляется клиникой плевро-пульмонального шока. Отмечается резкая боль в грудной клетке, беспокойство, многократная рвота, затрудненное дыхание - одышка, слабость, заторможенность. Вскоре к указанным симптомам присоединяются аллергические проявления.
Диагностика эхинококкоза легких у детей, особенно при присоединении осложнений, представляет определенные трудности, о чем свидетельствует анализ клинического материала.
В процессе лечения 103 детей с эхинококкозом легких диагностические ошибки были допущены врачами различных лечебных учреждений' в 63 наблюдениях (61,7%). До поступления в РДКБ в течение длительного времени (от нескольких суток до двух месяцев и более) больные подвергались многократному обследованию и лечению в детском соматическом и хирургических отделениях по поводу различных заболеваний. У 21 ребенка (20,4%) с диагнозом плеврит, пиопневмоторакс и абсцесс легкого хирургами неоднократно (2-5) производились пункции, а в 12 наблюдениях произведено дренирование плевральной полости.
Правильный диагноз был поставлен врачами направляющих лечебных учреждений у 51 ребенка (49,5%), остальные пациенты поступили с различными диагнозами. Среди 52 детей у 28 эхинококкоз легкого трактовался как деструктивная пневмония и ее осложнения.
В диагностике эхинококкоза легких основным методом является рентгенологическое исследование грудной клетки.
При неосложненном эхинококкозе эхинококковая киста представляет собой круглую, либо овальную гомогенную более или менее интенсивную тень с четкими краями на фоне легочной ткани.
При прорыве эхинококковой кисты в бронх на рентгенограмме определяется уровень жидкости и газовый пузырь над ней или вместо горизонтального уровня жидкости наблюдается волнистость или выпуклость, что обусловливается спадением хитиновой оболочки паразита - симптом «плавающей хитиновой оболочки», или симптом «серповидного просветления».
Эти изменения напоминают деструктивную пневмонию и ее осложнения, что вызывает определенные сложности в диагностике ЭЛ.
Прорыв эхинококковой кисты в плевральную полость рентгенологически напоминает картину плеврита.
Необходимо отметить, что любой метод рентгенологического исследования обязательно оценивается не только с точки зрения его диагностической значимости, но и с точки зрения его лучевой нагрузки на исследуемого, что заставляет искать безвредные для ребенка методы исследования.
Наиболее простым и неинвазивным методом диагностики ЭЛ является ультразвуковое исследование. Эхография грудной клетки для диагностики ЭЛ нами проводилось у 65 детей.
Молодые эхинококковые кисты у 13 детей визуализировались в виде округлых анэхогенных образований без четкой капсулы. Их трудно было дифференцировать с бронхогенными, а также с ложными кистами легких, заполненными жидкостным содержимым.
Зрелая эхинококковая киста (42 наблюдения) имела гиперэхогенную капсулу, представляющую собой хитиновую оболочку паразита.
У 11 больных зрелая эхинококковая киста по периферии имела двойной контур: внутренний гиперэхогенный (хитиновая капсула гельминта) и наружный гиперэхогенный, представляющий фиброзную оболочку, которая образуется в органе (в данном случае в легком) вокруг эхинококкового пузыря. Эти две оболочки (хитиновая и фиброзная) отделялись между собой гипо-эхогенным ободком.
В большинстве случаев (39 детей) в просвете кисты определялась взвесь ("эхинококковый песок"). В отдельных случаях эхинококковые кисты имели концентрическое строение за счет фрагментов отслоившейся хитиновой оболочки.
При прорыве эхинококковой кисты в бронх у 7 детей в кисте определялись густая взвесь и пузырьки воздуха в виде гиперэхогенных линейных структур с акустической тенью в виде «хвоста кометы».
При прорыве в плевральную полость эхинококковая киста имела неправильную овальную форму и неровные контуры. Одномоментно в заднем реберно-диафрагмальном синусе плевральной полости было обнаружено небольшое количество свободной жидкости и нити фибрина в виде гиперэхогенных линейных эхоструктур, тянущихся под различными углами между плевральными листками.
В 5 случаях при эхографии рядом с кистой выявлен участок ателектазированной легочной ткани в виде образования треугольной формы однородной структуры, похожей на печеночную ткань.
Таким образом, эхографическая семиотика и особенности эхографической картины ЭЛ зависит от степени развития паразита и имеющихся осложнений.
Изменения лабораторных показателей при эхинококкозе неспецифичны. В анализе периферической крови повышение количества эозинофилов обнаружено у 46% детей, лейкоцитоз выявлен у 31,6% больных, ускоренная СОЭ -у 53,3% пациентов.
Продолжительность предоперационной подготовки была различной и зависела от общего состояния ребенка, от характера и давности имеющихся осложнений.
Детям с неосложненным ЭЛ предоперационную подготовку осуществляли по общехирургическим правилам в течение 3-4 дней, включая десенсибилизирующую терапию.
Все дети с осложненными формами эхинококкоза легкого поступили в клинику в экстренном порядке в тяжелом и очень тяжелом состоянии.
Тяжесть состояния пациентов была обусловлена острой дыхательной недостаточностью по обструктивному и рестриктивному типам, гиповолеми-ей, эндотоксикозом и дефицитом жидкости. Перечисленные моменты указывали на необходимость предоперационной подготовки, направленной на коррекцию вышеперечисленных нарушений.
При прорыве эхинококковой кисты в плевральную полость проводили плевральную пункцию с целью ликвидации рестриктивной острой дыхательной недостаточности. В 5 наблюдениях потребовалась фибробронхоскопия, с целью санации ТБД с последующей респираторной терапией - ИВЛ в течение 5 часов.
В качестве инфузионного лекарственного средства первоочередного применения был использован инфузионный коллоидный раствор на основе гидроксиэтилированного крахмала второго поколения (ИНФУКОЛ HES 200/0,5 ГЭК 6%), являющийся оптимальным раствором для лечения гиповолемии, а также профилактики и лечения нарушений микроциркуляций (Контакевич М.М., 1999; Лекманов А.У., 1999). Согласно нашим исследованиям пациентам с осложненными формами ЭЛ в предоперационной подготовке необходим объем инфузии из расчета от 7 до 14 мл/кг со скоростью 0,2 - 0,3 мл/кг/час.
По данным пульсоксиметрии, через 9-18 часов после проведенных мероприятий в предоперационной подготовке отмечалось улучшение и стабилизация показателей ЧСС и SpО (р<0,05).
Таким образом, интенсивная терапия в предоперационном периоде у детей с осложненными формами 2 позволяет проводить торакотомию по экстренным и срочным показаниям через 18 часов после поступления в стационар.
Из существующих способов операции при ЭЛ мы использовали способы по Дельбе ( у 63), А.В.Вишневскому (у 18) и А.Т. Пулатову (у 13). У 9 детей нами выполнена видеоторакоскопическая эхинококкэктомия. Резекция доли легкого проведена только у 2 пациентов.
Техника выполнения вышеперечисленных традиционных операций хорошо описана в литературе (Пулатов А.Т., 1983; Абдуфаттаев Т.А., 1989; Каримов Ш.И. и соавт.,2000). Важным этапом операции при ЭЛ является ушивание бронхиальных свищей (БС), которые нами диагностированы у 88% оперированных. Количество БС колеблется от 1 до 13; у 21,6% наблюдались - одиночные, у 78,4% - множественные бронхиальные свищи.
Основываясь на клинико-экспериментальной работе (Абзалетдинова А. М., 1997) по использованию аллотрансплантата для пластики культи бронха при нагноительных заболеваниях легких у взрослых больных, с целью профилактики рецидива бронхиального свища мы использовали аллотрансплантат для замещения объемных дефектов тканей серии Аллоплант. Аллоплант разработан во Всероссийском центре пластической хирургии глаза (г. Уфа). Бронхиальный свищ ушивали отдельными узловыми швами викрилом 5/0 на атравматической игле по типу: Аллоплант - бронх, бронх - Аллоплант, при этом узел завязывали над Аллоплантом (рацпредложение № 2519 от 03.09.2002г.). Подобным способом произведено ушивание 16 бронхиальных свищей у 4 больных с осложненным эхинококкозом легкого.
Видеоторакоскопическая эхинококкэктомия легких
Одним из последних и перспективных достижений торакальной хирургии являются видеоторакоскопические операции (ВТО). Особенно привлекательны такие операции в детской хирургии из-за их меньшей инвазивности, легкого течения послеоперационного периода, быстрой реабилитации (Кротов Н.Ф., и соавт., 1999, 2000; Мамлеев И.А., 2000).
Показанием к торакоскопической эхинококкэктомии легкого служит наличие небольших (до 40,0 мм в диаметре) неосложненных, периферически расположенных кист.
Противопоказанием к торакоскопической эхинококкэктомии легкого служит наличие больших кист (более 70 мм в диаметре), а также центрально расположенных кист, рецидивных кист, осложненных нагноением.
Методика видеоторакоскопической эхинококкэктомии легких включает в себя 5 последовательных этапов:
1. Введение первого троакара, создание пневмоторакса, ревизия плевральной полости.
2. Введение рабочих троакаров.
3. Собственно эхинококкэктомия.
4. Уменьшение размеров остаточной полости.
5. Ушивание троакарных ран.
Видеоторакоскопическая эхинококкэктомия легких выполнялась под общим обезболиванием с раздельной искусственной вентиляцией легких двухпросветной трубкой и полным отключением оперируемого легкого в положении больного на здоровому боку или на спине в зависимости от локализации кист.
Операционная бригада при всех операциях состояла из хирурга и двух ассистентов. На первом этапе первый торакопорт (10 мм) и оптическая система вводились в стандартной точке в области угла лопатки при отведенной вверх руке. Однако при решении вопроса о точке введения торакопорта следует учитывать зону локализации кисты. После ревизии плевральной полости и пересечения возможных спаек осуществляли поиск кисты. При этом, как правило, выявляли типичный симптомоком-плекс эхинококковой гидатидозной кисты - наличие участка фиброзной оболочки эхинококка белесоватого цвета, локализованных спаек, участков ателектазированной легочной ткани сероватого цвета.
На втором этапе дополнительно вводили три 5- и 10-мм инструментальных троакара.
На третьем этапе для соблюдения принципов анти - и апаразитарной хирургии обкладывали кисты марлевыми салфетками, пропитанными раствором формалина. Затем производили чрезкожную пункцию длинной и широкой иглой полости эхинококковой кисты в точке, соответствующей наименьшему расстоянию до объекта вмешательства. Электроотсосом производили эвакуацию по игле содержимого кисты. Одновременно эндоскопический аспиратор подводили к точке пункции кисты с целью профилактики излития эхинококковой жидкости в плевральную полость. Полученная из полости кисты жидкость направлялась на экспресс - исследование на предмет наличия сколексов. Далее в полость вводили аналогичное количество антипаразитарной композиции, состоящей из формалина и глицерина с экспозицией в 10,0 мин. Затем жидкость эвакуировали. Игла извлекалась, а место пункции захватывалась фиксирующим граспером.
На следующем этапе вмешательства проводилась тракция фиброзной оболочки в костальном направлении и рассечение ее коагуляционным электродом, а затем формировалось окно. В просвет кисты вводили аспиратор, удаляли остатки жидкости, хитиновую оболочку осторожно отслаивали от фиброзной. Затем в полость кисты вводили широкий торакопорт (до 18,0 мм) и хитиновую оболочку захватывали зажимом типа Babcock или EndoLung и извлекали наружу. Важным моментом является правильное введение торакопорта в полость кисты - дистальный конец последнего должен находиться в ее просвете, что исключает контакт хитиновой оболочки с плевральной полостью. По торакопорту проводили дополнительную санацию полости кисты антипаразитарной композицией. Далее фиброзную капсулу рассекали и полость кисты визуализировали при помощи оптической системы. Высокое видеоразрешение и увеличение позволяло выявить и удалить мелкие дочерние кисты, а также «гидатидозный песок», который указывает на зрелость ларвоцисты. При видеоскопии полости кисты можно визуализировать и мелкие бронхиальные свищи и подвергнуть их ушиванию. Наш небольшой опыт свидетельствует о целесообразном применении эндоскопического ручного шва. Фиброзную капсулу иссекали в пределах здоровой ткани легкого. Возможно проведение эндоскопического капитонажа, однако это не является обязательным этапом вмешательства. На этом этапе анестезиолог переводит пациента на режим двулегочной вентиляции и хирургом осуществляется контроль за аэростазом. Мелкие свищи электрокоагулировали, более крупные свищи ушивали. Полость кисты дренировали широкой трубкой. Плевральную полость промывали раствором антисептика и дренировали из отдельного доступа. Отверстия от торакопортов ушивали.
Применение эндоскопической технологии при гидатидозной форме эхинококкоза у 9 детей позволило избежать широкой торакотомии и значительно снизить травматичность оперативного вмешательства. Кроме того, отмечается минимальная кровопотеря, уменьшается расход медикаментов, сокращается длительность пребывания больного в стационаре, отмечается хороший косметический эффект.
У большинства больных (98,4%) выполнена щадящая органосохраняющая операция. Даже при сохранении ателектазированных участков легкого или при наличии значительного изменения доли легкого органосохраняющая операция себя оправдала.
Большое значение в профилактике послеоперационных осложнений и благоприятном исходе операций у больных с ЭЛ имеет правильная организация послеоперационного периода. При этом основные усилия были направлены на поддержание адекватного газообмена и гемодинамики в первые сутки после операции и на профилактику аспирационных и гнойных осложнений.
Послеоперационное ведение детей с ЭЛ включало: анальгезию, антибактериальную и десенсибилизирующую, инфузионную и симптоматическую терапию.
В раннем послеоперационном периоде все пациенты были помещены в анестезиолого-реанимационное отделение. Средний койко-день составил 2,5 ± 0,6.
Показатели гемодинамики в первые 8 часов после операции указывали на гипердинамический тип кровообращения - увеличение ЧСС (р<0,01), АДс и САД (р<0,05).
К концу первых суток показатели ЧСС оставались повышенными (р<0,01), но уменьшались. На 2-е и 3-й сутки после торакотомии отмечалась достоверная нормализация параметров гемодинамики: ЧСС, АДс и САД (р<0,05).
Показатели кислотно-основного состояния у больных с эхинококкозом легких в послеоперационном периоде представлены в таблице 2.
| Показатель | До операции | 1 сутки | 2 сутки | 3 сутки | |
|---|---|---|---|---|---|
| 8 часов | 18 часов | ||||
| рН | 7,36 ±0,07 | 7,29 ± 0,07* | 7,31 ±0,05 | 7.40 ± 0,03 | 7,38 ± 0,02 |
| рО мм рт ст | 89,3 ± 1,9 | 72,2 ±2,8** | 76,8±3.1** | 80,9 ±2,1* | 85,3 ± 2,0 |
| рС02 мм рт ст | 34,5 ± 2,3 | 40,5 ± 1.8* | 37,6 ±2,0 | 36.2 ±2,8 | 37,0 ± 1,8 |
| BE | -2,9 ± 0,8 | -7,3 ± 1,0** | -5,1 ±0.8* | -4.1 ±1,0 | -3,8 ±1,1 |
| Sp02% | 96,2 ± 1,0 | 92,4 ±0,5** | 92,5 ± 0,7** | 94,1 ±1,0 | 95,5 ±1,2 |
* - р<0.05 - достоверные различия с до операционными данными;
** - р<0,01 - достоверные различия с до операционными данными.
В первые сутки послеоперационного периода у пациентов отмечался смешанный ацидоз, снижение рО2 и SpC2 % (p<0,01). На 2-е сутки показатели рО2 оставались ниже дооперационных (р<0,05).
В послеоперационном периоде у пациентов, оперированных методом видеоторакоскопии, показатели SpCb были выше (р<0,05), чем у детей после традиционной торакотомий . Послеоперационное обезболивание у 75 больных (71,9%) осуществлялось наркотическим анальгетиком (промедолом), а у 29 пациентов - сочетанием наркотического анальгетика (промедола) и ненаркотического (противовоспалительного) анальгетика из группы нестероидных противовоспалительных средств (НПВС) кетопрофеном. Первое введение этого препарата осуществляли в конце операции, в последующем назначение данных препаратов проводили по показаниям, используя шкалу оценки боли, разработанную Hannallak et al. (1991).
Как видно из таблицы 3, у пациентов без введения кетопрофена в конце операции надобность в обезболивании возникала уже через 1 час (5-6 баллов). При введении кетопрофена в конце торакотомий послеоперационное обезболивание приходилось делать через 3-4 часа, с суммой баллов 5.
| Время после торакотомий | Количество детей по бальной оценке боли | |||||
|---|---|---|---|---|---|---|
| 0 баллов | 2 балла | 3 бала | 4 балла | 5 баллов | более 6 баллов | |
| Послеоперационное обезболивание промедолом (n = 70) | ||||||
| 1 час | 3 | 2 | 1 | 6 | ||
| 2 часа | 6 | 5 | ||||
| 3 часа | 7 | 6 | ||||
| 4 часа | 2 | - | ||||
| 6 часов | 1 | - | ||||
| Послеоперационное обезболивание в комбинации с кетопрофеном (введение препарата в конце торакотомий) (n = 29) | ||||||
| 1 час | 6 | 3 | - | - | ||
| 2 часа | 4 | - | ||||
| 3 часа | 10 | 1 | ||||
| 4 часа | 10 | - | ||||
| 6 часов | 4 | - | ||||
Кратность применения наркотических анальгетиков после проведения торакотомий у детей с ЭЛ представлено в таблице 5, из которой можно заключить, что сочетание их с кетопрофеном уменьшает частоту введения промедола до одного раза в сутки. Сохранение двигательной активности больного на фоне адекватной длительной анальгезии являлось весьма благоприятным фактором, оказывающим влияние на течение послеоперационного периода и тем самым позволило нам улучшить исходы хирургического вмешательства.
| Кратность введения анальгетика | Количество детей | ||
|---|---|---|---|
| 1 сут | 2 сут | 3 сут | |
| Послеоперационное обезболивание промедолом (n=30) | |||
| 1 раз в сутки | - | 15 | 3 |
| 2 раза в сутки | 19 | 14 | - |
| 3 раза в сутки | 8 | 1 | - |
| 4 раза в сутки | 3 | 3 | 3 |
| Послеоперационное обезболивание в комбинации с кетопрофеном (n=29) | |||
| 1 раз в сутки | 18 | 4 | - |
| 2 раза в сутки | 10 | 3 | - |
| 3 раза в сутки | 1 | - | - |
| 4 раза в сутки | - | - | - |
В послеоперационном периоде у 12 больных (14,6%) возникли различные осложнения. У двух больных развилась эмпиема плевры, у 4-х - пневмония. Бронхиальные свищи выявлены у 4-х детей, оперированных по поводу осложненного ЭЛ, ателектаз легкого у 2-х..
Отдаленные результаты хирургического лечения изучены у 79 оперированных нами больных в сроки от 3 мес. до 17 лет.
Хорошие результаты отмечены у 65 больных. Удовлетворительные результаты были отмечены у 10. Неудовлетворительные результаты получены у 4 пациентов, у которых возникли рецидивы эхинококкоза легких, оперированных по поводу осложненных и множественных эхинококкозов легких.
Заключение
Внедрение в практику лечебно - диагностических мероприятий, включающих эхографию, совершенствование техники операции, адекватное предоперационное и послеоперационное ведение улучшают исходы хирургического лечения ЭЛ.
Основной причиной диагностических ошибок является: недостаточное знание практическими врачами клинико - рентгенологической картины эхинококкоза легких, поверхностное обследование, неверная трактовка объективных данных, а также отсутствие настороженности в отношении ЭЛ.
Изучение клинической картины ЭЛ выявило, что данное заболевание у детей в 16,9% случаев протекает бессимптомно, в то же время у 38,9% детей наблюдаются различные осложнения, которые протекают как деструктивная пневмония и ее осложнения, что требует от педиатров и хирургов активного выявления и своевременного оперативного лечения.
Эхографическая семиотика эхинококкоза легкого зависит от стадии паразита и характера осложнений. Патогномоничным симптомом для зрелого эхинококкоза легких является наличие гиперэхогенной капсулы (хитиновая оболочка).
Предоперационная подготовка при осложненном эхинококкозе легких проводится с целью ликвидации острой дыхательной недостаточности, гиповолемии, эндотоксикоза и дефицита жидкости. Продолжительность ее должна быть не более 18 часов.
Операцией выбора у детей с эхинококкозом легких является органосохраняющая операция, выполненная нами у 98,1% больных. Видео- торакоскопическая операция применяется при наличии небольших до 40-50 мм в диаметре, неосложненных и периферически расположенных кист.
Практические рекомендации
- Высокая информативность, простота и безопасность эхографии позволяет рекомендовать комплексное ультразвуковое исследование легких при подозрении не только на эхинококкоз, но и другой патологии легких и плевры.
- Учитывая то, что у 17,4% наблюдается сочетанное поражение эхинококкозом легких и печени, при выявлении эхинококкоза легкого необходимо проводить УЗИ брюшной полости.
- Следует повысить «эхинококковую» настороженность врачей лечебно - профилактических учреждений, принимая во внимание распространенность ЭЛ в республике Башкортостан и их рост в последние годы.
- Детей с осложненным эхинококкозом легких следует оперировать после предоперационной подготовки с целью коррекции частоты сердечных сокращений и насыщения кислорода в артериальной крови в течение 9-18 часов.
- Методом выбора при лечении эхинококкоза легких у детей является органосохраняющая операция. Имеющийся ателектаз и невенти-лирующаяся доля (участок) легкого после операции расправляется в течение 3-5 суток.
- Применение аллотрансплантата серии Аллоплант при ушивании бронхиальных свищей с осложненным ЭЛ предупреждает прорезывание швов и рецидив свища
Литература
- Эхинококкоз легкого у детей// Международный конгресс ИНТЕРАСТМА-98, 20-21 октября 1998// YIII национ. конгресс по болезням органов дыхания. IY национал, конгресс по муковисцидозу, Москва, 22-24 октября 1998 г. Сборник резюме С. 306 (соавт.: Гумеров А.А., Ишимов Ш.С., Шангареева Р.Х.).
- Хирургическое лечение изолированного и сочетанного эхинококкоза у детей// Вопросы детской хирургии и пограничных областей: Матер. межрегион. научно-практич. конфер., посвящ. 40-летию детской хирургич. службы Удмуртии, Ижевск, 1998 г. С. 73-74 (соавт.: Гумеров А.А., Шангареева Р.Х., Ишимов Ш.С., Мамлеев И.А., Сатаев В.У.).
- Клиника осложненного эхинококкоза легкого у детей// Межрег. науч.-практич. конф. "Здоровье детей и подростков в соврем. соц.-эконом. и экологич. условиях", Уфа, 1999. С. 77-78 (соавт.: Гумеров А.А., Ишимов Ш.С, Шангареева Р.Х.).
- Особенности клиники осложненного эхинококкоза легких у детей "Неотложные состояния у детей// Матер. YI конгресса педиатров. Москва, 6-8 февраля 2000 г. С. 95 (соавт.: Гумеров А.А., Ишимов Ш.С, Хасанов Р.Ш., Шангареева Р. X.).
- Эхинококкоз легкого у детей, осложнения, лечение// Материалы международ. научно- практич. конф. Тезисы докладов. Махачкала, 2000 г. С. 45 - 46 (соавт:. Гумеров А.А., Шангареева Р.Х., Хасанов Р.Ш.)
- Возможности эхографии при эхинококкозе легких у детей// Акт. вопр. повышения квалификации врачей и провизоров. Нов. тех. в медицине. Матер. регион. наук.- пр. конфер. посвящ. 25 - летию ИПО БГМУ, Уфа, 2001, С. 105 (соавт.: Васильева Н.П., Гумеров А.А., Одилов А.Х.)
- Особенности клинической картины прорыва эхинококковой кисты в бронх у детей. Настоящее и будущее детской хирургии// Матер. конфе-рен., посвящ. 70-летию кафедры хирургических болезней детского возраста РГМУ, Москва, 4-5 декабря 2001, С.78 (соавт.: Гумеров А.А., Хасанов Р.Ш., Ишимов Ш.С, Васильева Н.П., Сабиров М.Ш.).
- Видеоторакоскопическая коррекция гидатидозной формы эхинококкоза// Тез. докл. 5-ой Всероссийской конф. хирургов и симпозиума ассоциации колопроктологов России, Уфа, 2001, С. 10. (соавт.: Гумеров А.А., Н.П. Васильева, И.А. Мамлеев, В.У. Сатаев, В.В. Макушкин).
- Эхографический контроль за состоянием плевральной полости после торакальных операций у детей// Тез. докл. 5-ой Всероссийской конф. хирургов и симпозиума ассоциации, колопроктологов России, Уфа, 2001, С. 262 (соавт.: Гумеров А.А., Н.П. Васильева, И.А. Мамлеев, Р.Ш. Хасанов.).
- Диагностические ошибки при эхинококкозе легких у детей// Мат.науч.-практ. конф., посвящ. 30-летию со дня открытия РДКБ, 19-20 июня 2002 года. Уфа, 2002. - С. 162-164. (соавт.: Гумеров А.А., Ишимов Ш.С, Шангареева Р.Х.).
- Выбор метода лечения при эхинококкозе у детей // Тр. ассоциации хирургов РБ, Уфа, 1998г., т. 3, С.85-86 (соавт.: Гумеров А. А., Ишимов Ш. С, Шангареева Р. X., Мамлеев И. А., Сатаев В. У.).
Методические рекомендации
Клиника, диагностика эхинококкоза легких у детей (соавт.: Гумеров А.А., Хасанов Р.Ш., Ишимов Ш.С, Мамлеев И.А., Шангареева Р.Х.). Уфа, 2002.-22 с.
Рационализаторское предложение
Способ ушивания бронхиального свища при эхинококкозе легких у детей. Удостоверение на рационализаторское предложение № 2519 от 03.09. 02г,. выданное Башкирским государственным медицинским университетом (соавт.: Гумеров А.А., Ишимов Ш.С, Мамлеев И.А.).
к содержанию | опубликовать статью
ПУТИ ПРЕДУПРЕЖДЕНИЯ ФОРМИРОВАНИЯ РУБЦОВЫХ СТРИКТУР ВНЕПЕЧЕНОЧНЫХ ЖЕЛЧНЫХ ПРОТОКОВ И МЕТОДЫ ИХ ХИРУРГИЧЕСКОЙ КОРРЕКЦИИ
(Экспериментально - морфологическое и
клиническое исследование)
Палтусов А. И.
ГБОУ ВПО «Башкирский государственный медицинский университет Министерства здравоохранения и социального развития Российской Федерации»
Автором разработан и анатомически обоснован аллогенный мембранный биоматериал для герметизации и восстановления анатомической целостности билиодигестивного анастомоза. На основании приведенных клинических исследований обоснована возможность профилактики и лечения рубцовых стриктур желчевыводящих путей с использованием аллогенного мембранного биоматериала.
Актуальность Желчно-каменная болезнь – одна из наиболее часто встречающихся в практике врача патологий печени и желчевыводящих путей. По данным Гальперина Э.И. (2001), до 10% населения мира страдают данной патологией, при этом показатель заболеваемости за каждое последнее десятилетие возрастает примерно в 2 раза (Галеев М.А.,1997; Тимербулатов В.М.,1999; Еременко В.П.,1999). Рост хирургической активности в связи с увеличением количества больных с заболеваниями желчевыводящей системы влечет за собой возрастание числа пациентов с неудовлетворительными результатами после операций на желчной системе.
Количество пациентов, которым операция не принесла ожидаемого улучшения, достигает 15%. Одной из причин неблагоприятных результатов хирургических вмешательств на желчных путях является развитие рубцовых стриктур в результате их травмы или неправильной хирургической тактики. На долю посттравматических рубцовых стриктур приходится 90-97 % от всех выявленных рубцовых поражений желчных путей. Лечение больных с рубцовыми стриктурами внепеченочных желчевыводящих путей относится к наиболее сложным проблемам в хирургии желчных путей. Несмотря на многочисленные модификации и усовершенствования техники операций на желчевыводящих путях, таких как билиодигестивные анастомозы, пластика холедоха, реканализация холедоха и других, частота первичных и рецидивных стриктур остается высокой. Летальность в этой группе больных достигает 18,4%, осложнения при операциях возникают в 47% случаев, а рецидивы стриктур после проведенного хирургического вмешательства наступают в 5,8- 35% наблюдений.
Рубцовая стриктура желчевыводящих путей нередко возникает после холецистэктомии и резекции желудка, при которых чаще всего возможно случайное повреждение желчевыводящих путей. Частота ятрогенных повреждений желчных протоков при холецистэктомии и резекции желудка уже многие десятилетия остается величиной постоянной: 0,4-2,0% - при холецистэктомии, 0,1-0,6% - при резекции желудка. В результате тысячи больных ежегодно становятся инвалидами из-за развития рубцовой стриктуры желчных протоков с её непременными атрибутами: механическая желтуха, гнойный холангит, наружный желчный свищ, билиарный цирроз печени, портальная гипертензия и многократные повторные операции (Гальперин Э.И., 1996; Horvath K.D.,1993). На сегодняшний день разработаны и используются различные способы лечения и профилактики рубцовых стриктур желчных протоков в том числе с применением разнообразных аутологичных трансплантатов, а также путем усовершенствования техники хирургических вмешательств: внедрения микрохирургической техники, создания арефлюксных анастомозов и других (Каган И.И., 1996; Карабасов А.Е., 2001; Мохов Е.М., 2002).
Однако, несмотря на указанные достижения, требуется дальнейшая разработка и усовершенствование оперативных методов лечения больных с рубцовыми стенозами желчевыводящих путей, а также профилактика рубцовых стриктур общего желчного протока после оперативных вмешательств. Учитывая изложенное мы обратили внимание на мембранный биоматериал производимый на основе серозных оболочек в тканевом банке Всероссийского центра глазной и пластической хирургии г. Уфы. На наш взгляд применение биоматериала из серозных оболочек для решения обсуждаемой проблемы представляется наиболее обоснованным.
Цель исследования
Целью настоящего исследования являются улучшение результатов хирургического лечения больных с патологией желчевыводящих путей и профилактика формирования рубцовых стриктур желчевыводящих путей путем разработки анатомически обоснованного способа формирования билиодигестивного анастомоза с использованием аллогенного мембранного биоматериала.
Материалы и методы экспериментальных исследований
В соответствии с целью и задачами исследования проведены эксперименты на 110 белых крысах – самцах линии ’’Вистар’’ весом 180-210г.
Лабораторные животные по методике операции были разделены на 2 группы. В опытной группе операция наложения холедоходуоденоанастомоза производилась с применением аллогенного мембранного биоматериала, обработанного по запатентованной технологии Аллоплант (производство Лаборатории консервации тканей ФГБУ ВЦГПЗ Минздравсоцразвития России), с помощью которого герметизировали зону анастомоза.
В контрольной группе операция холедоходуоденостомия выполнялась по аналогичной методике, без использования аллогенного биоматериала. Герметизации анастомоза при этом достигалась наложением серо-серозных швов между желчным протоком и кишкой.
Из эксперимента животные выводились путем декапитации на 7, 14, 30, 60-е сутки. Участок созданного холедоходуоденоанастомоза с окружающими тканями вырезался, фиксировался в 10% нейтральном формалине с последующей заливкой материала в парафин. Приготовленные срезы толщиной 5-6 мкм окрашивались гематоксилином и эозином и по Ван-Гизону. При этом оценивали динамику регенерации соединительной ткани, реакцию на аллогенный биоматериал в области анастомоза. Морфометрия проводилась с использованием программы Bio-Vision.
Статистическая обработка полученных результатов выполнялась с использованием программы «Statistika-5».
Материал и методы клинических исследований
В основу клинического материала, используемого в работе, положены результаты обследования и хирургического лечения 179 больных с заболеваниями желчных протоков, требующими наложения билиодигестивного анастомоза, а также с повреждениями и рубцовыми стриктурами внепеченочных желчных протоков, находившихся на стационарном лечении в Республиканской клинической больницы им Г.Г. Куватова и хирургического отделения Отделенческой больницы ст.Уфа за период с 1995 по 2003год.
Все пациенты нами были разделены на две клинические группы. В первую группу вошли пациенты с заболеваниями желчевыводящих путей, которым проводилось оперативное лечение с наложением билиодигестивного анастомоза. Во вторую группу вошли пациенты, которым проводились реконструктивные операции на желчевыводящих путях при повреждениях или уже сформированном рубце желчных протоков.
Каждая группа была разделена на две подгруппы: в основных подгруппах оперативное лечение выполняли с применением аллогенного мембранного биоматериала Аллоплант (производства Лаборатории консервации тканей ФГБУ ВЦГПЗ Минздравсоцразвития России) и подгруппах сравнения (контрольных), операции выполнялись по традиционным методикам. В основной подгруппе первой группы (31 пациент) операцию наложения билиодигестивного анастомоза дополняли герметизацией зоны анастомоза аллогенным мембранным биоматериалом. В основной подгруппе второй группы (40 пациентов) выполнялись реконструктивные операции на желчных путях также с применением аллогенного мембранного биоматериала Аллоплант.
Пациенты основных подгрупп оперированы в 1998-2003 годы.
Пациенты контрольных подгрупп пролечены в 1995-2003 годы.
Разница во временных промежутках в основной и контрольной подгруппах обусловлена единственной причиной – применением аллогенного мембранного биоматериала в клинической практике.
Результаты экспериментальных исследований
В опытной группе на 7-е сутки в микропрепаратах определяется выраженная инфильтрация. Размеры аллотрансплантата в целом сохранены. Аллотрансплантат находится в состоянии плотной адгезии с тканевым ложем на всем протяжении. Область тканевого ложа инфильтрирована преимущественно сегментоядерными лейкоцитами, недифференцированными соединительнотканными клетками и макрофагами. В последующем (14-е сутки) в краевых зонах трансплантата определяется фибробластическая и макрофагальная инфильтрация. В эти сроки отмечены начало созревания соединительной ткани и синтез компонентов внеклеточного матрикса. Аллогенный биоматериал подвергается активному замещению. На 30-е сутки в микропрепаратах определяется уменьшение воспалительных процессов в тканевом ложе трансплантата. Фибробласты контактной зоны активно синтезируют коллагеновые волокна и с периферии постепенно замещают аллотрансплантат. В трансплантате выявляется большое количество макрофагов, снижается количество фибробластов (рис1, 2).
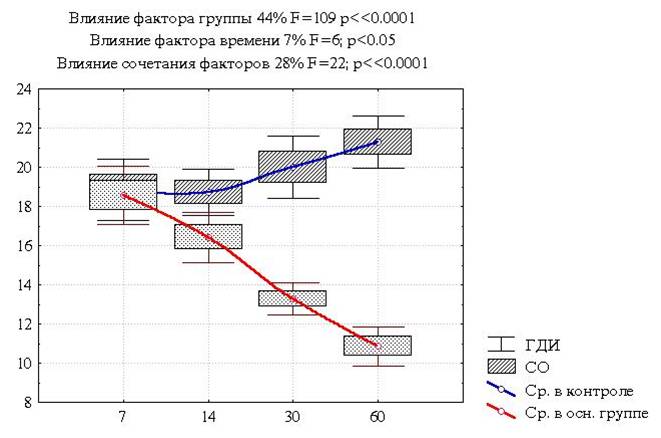 |
|---|
| Рис 1 Плотность фибробластов в опытной и контрольной группах эксперимента в динамике. По вертикали – количество клеток на единицу площади (о,15мм ²), по горизонтали – сроки эксперимента в сутках. |
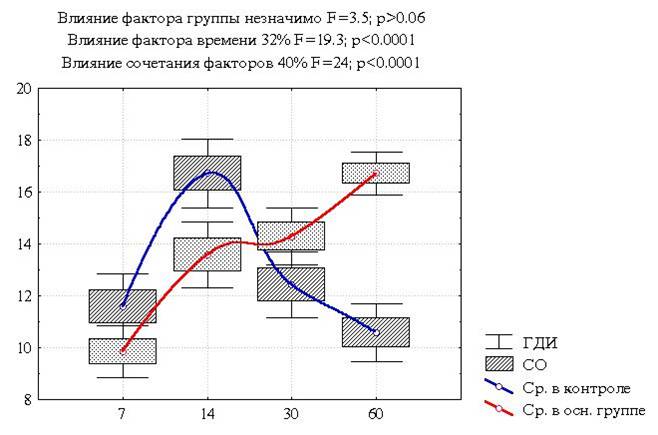 |
|---|
| Рис 2 Плотность макрофагов в опытной и контрольной группах эксперимента в динамике. По вертикали – количество клеток на единицу площади (о,15мм ²), по горизонтали – сроки эксперимента в сутках. |
Формирующиеся коллагеновые фибриллы ориентированы вдоль коллагеновых волокон трансплантата. Новообразованные коллагеновые фибриллы располагаются рядом с сохранившимися волокнами, замещение их происходит постепенно. Между пучками волокон трансплантата определяется рыхлая волокнистая соединительная ткань. Структура печени не изменена. На 60-е сутки трансплантат замещен тканями реципиента. Образовавшийся регенерат представляет собой рыхлую волокнистую оформленную соединительную ткань. Фрагменты трансплантата не определяются. Регенерат структурно оформлен на всем протяжении и соответствует размерам трансплантата. Структура печени сохранена, явлений холестаза нет.
В печени наблюдается деструкция части гепатоцитов их кариолизис. На 30-е сутки отмечается уменьшение воспалительной реакции вокруг анастомоза. Инфильтрация ткани представлена всеми типами клеток фибробластического дифферона, среди которых преобладают фибробласты. Клетки увеличены в размерах, вытянуты. Вокруг желчевыводящего протока формируется плотная неоформленная волокнистая соединительная ткань.
В печени нарастают явления интерстициального отека и холестаза. На 60-е сутки зона анастомоза представлена плотной неоформленной волокнистой соединительной тканью с признаками фиброза. Резко выражены признаки холедохостаза. В печени сохраняются признаки деструкции гепатоцитов и нарушения их цитоархитектоники.
На рис.1 показано достоверное увеличение количества фибробластов в контрольной серии в сроки от 7 до 60 суток по сравнению с опытной группой. В то же время количество макрофагов на 30 – 60-е сутки достоверно увеличивается в опытной группе (рис.2).
Таким образом, экспериментальные исследования показали, что использование аллогенного мембранного биоматериала при формировании холедоходуоденоанастомоза способствует его герметизации и стимулирует созревание рыхлой волокнистой соединительной ткани, а также препятствует образованию грубого рубца в зоне анастомоза.
Результаты клинического исследования
Анализ результатов лечения больных с билиодигестивными анастомозами, оперированных по традиционной методике (первая группа, контрольная подгруппа)
В данной подгруппе операции выполнялись традиционным способом без использования аллогенного биоматериала. В табл.1 приведен анализ послеоперационных осложнений.
| Виды послеоперационных осложнений | Количество осложнений |
|---|---|
| Специфические | |
| Гнойный холангит | 1 |
| Несостоятельность швов анастомоза | 4 |
| Поддиафрагмальный абсцесс | 1 |
| Желчеистечение и формирование свища | 1 |
| Неспецифические | |
| Застойная пневмония | 2 |
| Инфаркт миокарда | 1 |
| Тромбофлебит вен голени | 2 |
| Ранняя спаечная непроходимость кишечника | 1 |
| Нагноение послеоперационной раны | 5 |
| Эвентрация | 2 |
| Всего: | 20 |
Таким образом, в данной подгруппе осложнения составили 33,3%, из них специфические были в 11,66% случаев, неспецифические – в 21,66%. Несостоятельность швов анастомоза встретилась в данной подгруппе в 4 случаях. В трех случаях несостоятельность швов ликвидирована консервативными методами лечения. В одном случае потребовалось оперативное лечение - реконструкция билиодигестивного анастомоза. Произведены так же две релапаротомии больным по поводу подпеченочного абсцесса и ранней спаечной непроходимости кишечника. Двое больных оперированы по поводу эвентрации кишечника, им произведено устранение эвентрации. Отмечены следующие непосредственные результаты лечения.
У всех больных (n=60) после операции отмечалась лихорадка, продолжительностью до 5 суток имела место в 2 случаях, до 10 суток - у 40 66,6%, свыше 10 суток - у 18 30% больных. Во всех случаях наблюдалось подтекание желчи по «страховочному» дренажу: до 5 суток - у 37 61,6% пациентов до 10 суток - у 20 33,3%, свыше 10 суток - у 3 5%. Частота послеоперационных осложнений составила 33,3%, из них специфические осложнения были в 11,66% случаев, неспецифические – в 21,66%. Средний послеоперационный койко-день составил (при n-60) 22,2. Летальных случаев не наблюдалось.
В сроки от 1 года до 8 лет после оперативного лечения сделан анализ состояния здоровья у 60 больных, выписанных из отделения, путем опроса, анкетирования и проведения общеклинических и специальных методов исследования у части пациентов с удовлетворительными и неудовлетворительными результатами лечения. Хороший результат признавался, если больные сохраняют трудоспособность, у них отсутствуют приступы холангита, болевых ощущений нет. Он отмечен у 21 (35%) больного. Удовлетворительный, если больные сохраняют трудоспособность или имеют 11-111 группы инвалидности, проявления холангита у них наблюдаются не чаще 1-2 раза в год или они имеют постоянные болевые ощущения, вынуждающие при обострениях проводить амбулаторное или стационарное лечение. Удовлетворительный результат отмечен нами у 26(43,7%) больного. Неудовлетворительный результат, если отмечаются стеноз анастомоза, внутрипеченочный холелитиаз, абсцессы печени, гибель пациента в отдаленном периоде от печеночно-почечной недостаточности. Неудовлетворительный результат отмечался у 13 (21,3) пациентов. Трем пациентам из контрольной подгруппы потребовалась повторная операция в связи со стриктурой анастомоза и развитием внутрипеченочного холелитиаза. Стриктура развилась в сроки от 2 до 4 лет после первичной операции. У трех больных развился билиарный цирроз печени с периодическими обострениями, которые купируются консервативными мероприятиями. И у 6 пациентов периодически рецидивирует холангит.
Анализ результатов лечения больных с билиодигестивными анастомозами, оперированных с использованием аллогенного мембранного биоматериала (первая группа основная подгруппа)
В данную подгруппу включены пациенты, у которых хирургическое вмешательство проводилось с использованием аллогенного мембранного биоматериала Аллоплант, производимого на основе серозных оболочек. Нами разработаны медико-технические требования для производства данного биоматериала, определены оптимальные размеры 20х50х2мм. Данные параметры аллогенного мембранного биоматериала позволяют проводить герметизацию зоны анастомоза независимо от уровня поражения и индивидуальных особенностей организма. Кроме того, аллогенный мембранный биоматериал отличается пластичной моделируемостью, что является необходимым условием для герметизации анастомоза. Достаточная прочность шовной фиксации и хорошие адгезивные свойства в совокупности с адекватными биомеханическими свойствами позволяют рекомендовать данный трансплантат для реконструктивных операций на желчевыводящих путях. Учитывая показания для применения данного биоматериала в номенклатуре производимых биоматериалов в тканевом банке Всероссийского центра глазной и пластической хирургии, он включен под названием «Биоматериал для формирования билиодигестивного анастомоза».
В табл. 2 приводится анализ осложнений у больных, оперированных с использованием указанного биоматериала.
| Виды послеоперационных осложнений | Количество осложнений |
|---|---|
| Специфические | |
| Несостоятельность швов билиодигестивного анастомоза | - |
| Подпеченочный абсцесс | 1 |
| Желчеистечение и формирование свища | - |
| Неспецифические | |
| Застойная пневмония | 1 |
| Ранняя спаечная непроходимость кишечника | 1 |
| Нагноение послеоперационной раны | 2 |
| Гематома послеоперационной раны | - |
| Всего: | 5 |
В послеоперационном периоде выполнена релапаротомия по поводу ранней спаечной кишечной непроходимости. Несостоятельность швов билиодигестивного анастомоза в данной подгруппе не наблюдалась.
Непосредственные результаты лечения отмечены следующие: у всех больных (n=31) после операции отмечалась лихорадка. Продолжительность лихорадки до 5 суток имела место у 19 61,3%, до 10 суток - у 10 32,2% и более 10 суток - у 2 6,5% пациентов. Подпеченочный дренаж в послеоперационном периоде имелся у всех больных. В срок до 3 суток дренаж удален у 3 больных, до 5 суток – у 22, до 10суток – у 6 больных. Частота послеоперационных осложнений составила 16,1%, в том числе специфических – 3,2% и неспецифических - 12,9%, летальности в данной группе не было. Средний послеоперационный койко-день при лечении рубцовых стриктур желчных протоков составил 17,3 ± 2,8.
В срок от 1 года до 8 лет после оперативного лечения сделан анализ состояния здоровья у 31 больного путем опроса, анкетирования и проведением у части пациентов общеклинического и специальных методов обследования. Хороший результат отмечен у 80,6%, удовлетворительный – у 19,4%, неудовлетворительных результатов в данной группе не отмечалось.
Анализ результатов лечения больных с рубцовыми стриктурами, оперированных по традиционной методике (вторая группа контрольная подгруппа)
| Виды послеоперационных осложнений | Количество осложнений |
|---|---|
| Специфические | |
| Несостоятельность швов анастомоза | 4 |
| Поддиафрагмальный абсцесс | 2 |
| Холемическое кровотечение | 1 |
| Гнойный холангит и абсцесс печени | 1 |
| Кровотечение из швов межкишечного анастомоза | 1 |
| Неспецифические | |
| Застойная пневмония | 2 |
| Спаечная непроходимость кишечника | 1 |
| Нагноение послеоперационной раны | 7 |
| Инфаркт миокарда | 1 |
| Острый пиелонефрит | |
| Тромбоэмболия брыжеечных сосудов | 1 |
| Тромбофлебит вен голени | 2 |
| Тромбоэмболия легочной артерии | 1 |
| Эвентрация | 2 |
| Всего: | 27 |
Таким образом, при лечении повреждений и рубцовых стриктур желчных протоков осложнения составили 56,25%, из них специфические были в 18,75% случаев, неспецифические – в 37,5%.
Непосредственные результаты лечения отмечены следующие: у всех больных (n=48) после операции отмечалась лихорадка. Продолжительностью до 5 суток - в 2 случаях, до 10 суток - у 30 62,5%, свыше 10 суток - у 10 20,8% пациентов. Во всех случаях наблюдалось подтекание желчи по «страховочному» дренажу: до 5 суток - у 17 35,4% пациентов, до 10 суток - у 29 60,4%, свыше 10 суток - у 2 4,2%. Частота послеоперационных осложнений составила 56,25%, из них специфические были в 18,75% случаев, неспецифические – в 37,5%. Средний послеоперационный койко–день составил 32,2 (при n-42, не учитывались 6 больных с летальным исходом).
В срок от 1 года до 8 лет после оперативного лечения сделан анализ состояния здоровья у 42 из 48 больных, выписанных из отделения, путем опроса, анкетирования и проведения общеклинических и специальных методов исследования у части пациентов с удовлетворительными и неудовлетворительными результатами лечения. Хороший результат отмечен у 18 пациентов (42,8%), удовлетворительный – у 21 пациента (50%) и неудовлетворительный – у 3 (7,2%) пациентов. 13 пациентам из контрольной подгруппы потребовались повторные операции в связи с рестриктурой анастомоза и развитием внутрипеченочного холелитиаза. Рестриктура развилась в сроки от 1 года до 4 лет, после удаления каркасных дренажей. У двух больных возник синдром «недренируемой левой доли печени» при проведении дренажа только через правый печеночный проток при первичной операции, что явилось показанием для бигепатического дренирования. Данное осложнение развилось через 1–1,5 года после операции при наличии СТД. У двух больных развился билиарный цирроз печени с периодическими обострениями, которые купируются консервативными мероприятиями, у одной пациентки периодически рецидивирует холангит.
Анализ результатов лечения больных с повреждениями и рубцовыми стриктурами желчных протоков с применением аллогенного мембранного биоматериала (вторая группа основная подгруппа)
В данной подгруппе оперативные вмешательства выполнялись с использованием указанного выше аллогенного мембранного биоматериала Аллоплант.
| Виды послеоперационных осложнений | Количество осложнений |
|---|---|
| Специфические | |
| Несостоятельность швов гепатикоеюноанастомоза | 1 |
| Подпеченочный абсцесс | 1 |
| Неспецифические | |
| Застойная пневмония | 2 |
| Ранняя спаечная непроходимость кишечника | 1 |
| Нагноение послеоперационной раны | 2 |
| Гематома послеоперационной раны | 1 |
| Всего: | 8 |
В послеоперационном периоде выполнены две релапаротомии: по поводу ранней спаечной кишечной непроходимости и подпеченочного абсцесса справа. Несостоятельность швов гепатикоеюноанастомоза закончилась выздоровлением путем консервативной терапии.
Непосредственные результаты лечения отмечены следующие: у всех больных (n=40) после операции отмечалась лихорадка. Продолжительность лихорадки до 4 суток имела место у 28 70%, до 10 суток - у 11 27,5% и более 10 суток - у 1 2,5% пациентов. Подпеченочный дренаж в послеоперационном периоде имелся у всех больных. В срок до 3 суток дренаж удален у 8 больных, до 5 суток – у 26, до 10 суток – 6 больных. Частота послеоперационных осложнений составила 20%, в том числе специфических 5% и неспецифических 15%. Летальность в данной группе: умер один больной от острого инфаркта миокарда в раннем послеоперационном периоде. Средний послеоперационный койко-день при лечении рубцовых стриктур желчных протоков составила 18,4 ± 2,8
В срок от 1 года до 8 лет после оперативного лечения сделан анализ состояния здоровья у 39 больных путем опроса, анкетирования и проведения у части пациентов общеклинического и специальных методов обследования. Хороший результат отмечен у 67,5%, удовлетворительный – у 32,5%, неудовлетворительные результаты в данной группе не отмечались.
Таким образом, сравнительный анализ результатов лечения больных с повреждениями и рубцовыми стриктурами желчевыводящих протоков в основной и контрольной подгруппах позволил прийти к следующему решению: в основной подгруппе пациентов, у которых операции выполнялись с использованием аллогенного мембранного биоматериала, отмечаются более благоприятное течение послеоперационного периода и достоверно меньшее количество осложнений. Данный факт мы связываем с тем, что аллогенный мембранный биоматериал позволяет произвести более надежную герметизацию зоны анастомоза и в последующем стимулирует регенерацию рыхлой волокнистой соединительной ткани без признаков рубцевания. В контрольных подгруппах одним из частых осложнений являлось рубцевание в области созданного билиодигестивного анастомоза с образованием стойких стриктур.
Исследования показали, что использование аллогенного мембранного биоматериала способствует герметизации зоны анастомоза, что позволяет в клинике снизить частоту несостоятельности анастомозов, создает благоприятные условия для развития процессов репаративной регенерации в области сформированного анастомоза и предупреждает процессы рубцевания в данной области.
Заключение
Основными причинами рубцевания желчевыводящих путей после хирургического вмешательства на них являются повреждения желчных протоков. Формирование билиодигестивного анастомоза с использованием аллогенного мембранного биоматериала является достаточно эффективным способом профилактики и лечения рубцовых стриктур внепеченочных желчных протоков.
В области пересадки аллогенного мембранного биоматериала Аллоплант при формировании билиодигестивного анастомоза активируется макрофагальная инфильтрация, что препятствует образованию рубцовых изменений и приводит к регенерации рыхлой волокнистой соединительной ткани на месте трансплантации.
Пластично моделируемый мембранный аллотрансплантат размером 20х50х2мм позволяет независимо от индивидуальных анатомических особенностей и характера течения патологического процесса надежно герметизировать область сформированного билиодигестивного анастомоза и создает условия для благоприятного течения репаративной регенерации.
При формировании билиодигестивного анастомоза независимо от вида патологии целесообразно применение аллогенного мембранного биоматериала для формирования билиодигестивного анастомоза с целью профилактики рубцового процесса.
Внедрение разработанных методов профилактики и лечения рубцовых стриктур позволило уменьшить частоту рубцевания после первичных операций на желчных путях с 4,6 до 0,4%, а при повторных реконструктивных операциях с 14,5 до 1,5 %.
Практические рекомендации
- При первичных вмешательствах на желчных путях по поводу различных заболеваний желчных путей и необходимости наложения билиодигестивного анастомоза рекомендуется применение аллогенного мембранного биоматериала Аллоплант для формирования билиодигестивного анастомоза.
- При низких рубцовых стриктурах холедоха наиболее физиологично наложение холедоходуоденоанастомоза. При отсутствии условий для его выполнения необходимо применение билиодигестивного соустья с петлей тощей кишки, выключенной по Ру с использованием аллогенного мембранного биоматериала Аллоплант.
- При высоких повреждениях и рубцовых стриктурах желчных протоков выполняется гепатикоеюностомия, которую следует сочетать со СТД при ширине создаваемого соустья менее 15мм с применением аллогенного мембранного биоматериала Аллоплант.
Литература
- Палтусов А.И., Абдеев Р.Р. Хирургическое лечение свежих повреждений холедоха и их последствий.// Вопросы теоретической и практической медицины.- Уфа,2001. С.25-26.
- Палтусов А.И. Хирургическое лечение повреждений холедоха и их последствий рубцовых стриктур// Материалы Республиканской конференции молодых ученых Республики Башкортостан.- Уфа, 2002. С.64-65.
- Пешков Н.В., Палтусов А.И. Хирургическое лечение травм и рубцовых стриктур внепеченочных желчевыводящих путей// Актуальные проблемы гепатологии. -Уфа 2002. С.152-155.
- Нартайлаков М.А., ПешковН.В., Палтусов А.И., Мингазов Р.С и др. Профилактика и хирургическое лечение травм и рубцовых стриктур внепеченочных желчных протоков: Метод.реком.- Уфа,2002г. – 16с.
- Палтусов А.И. Способ формирования холедоходуоденоанастомоза в эксперименте.// Научный прорыв – 2002.- Уфа,2002. – С.63-64.
- Палтусов А.И, Андреев П.П. Диагностика повреждений и рубцовых стриктур гепатикохоледоха// Научный прорыв – 2003. –Уфа, 2003.- С.66-67.
к содержанию | опубликовать статью
СЛУЧАЙ ИЗ КЛИНИЧЕСКОЙ ПРАКТИКИ
СЛУЧАЙ УСПЕШНОГО ПРИМЕНЕНИЯ МЕТОДА ФАРМАКОПУНКТУРЫ БИОМАТЕРИАЛА АЛЛОПЛАНТ В КОМПЛЕКСНОМ ЛЕЧЕНИИ АХОНДРОПЛАЗИИ
Валиева Н. И., рефлексотерапевт ФГБУ ВЦГПХ Минздравсоцразвития России
Автор на клиническом примере обосновывает принципиальную возможность использования фармакопунктуры диспергированным биоматериалом Аллоплант в комплексном лечении больных с ахондроплазией.
Больной С. 2002 г.р., проходил амбулаторное лечение во Всероссийском центре глазной и пластической хирургии с марта 2008 года по поводу ахондроплазии (Ахондроплазия — системное поражение скелета — врождённая болезнь, характеризующаяся нарушением энхондрального остеогенеза; проявляется карликовостью, короткими конечностями при обычной длине туловища, деформацией нижних конечностей и позвоночника и относительной макроцефалией).
Из анамнеза: Родился доношенным ребенком от здоровой матери. Беременность проходила нормально. Диагноз был установлен сразу после рождения. Рост при рождении 49 см.
Status localis на 2005 год: ходит самостоятельно. Походка не изменена. Непропорциональность головы, туловища и сегментов конечностей. Имеется варусная деформация нижних конечностей, умеренная вальгусная деформация стоп.
Традиционная тактика лечения при этом заболевании следующая.
- Консервативное лечение в раннем возрасте направлено на профилактику деформаций нижних конечностей, укрепление мышц конечностей, спины, живота
- Хирургическое лечение проводят при развившихся деформациях нижних конечностей, а также с целью увеличения роста.
Anamnesis morbi:
До 2005 года лечения не принимал. Рост на этот период 72,5 см.
В апреле 2005 года была проведена ортопедическая операция – Биозагвоздка зон роста обоих коленных суставов. После чего рост увеличился на 12 см. Но за весь период с 2007 по 2008 год прирост составил только 0,5 см.
В марте 2008 г. в отделе рефлексотерапии Всероссийского центра глазной и пластической хирургии был проведен первый курс акупунктурного введения диспергированного биоматериала Аллоплант в биологически активные точки (БАТ) по специально разработанной методике. Проводилось три сеанса обкалывания Аллоплантом, разведенном в соотношении 100 мг. на 15 мл. физ. р-ра, с интервалом через день. Инъекции делались внутрикожно и подкожно. Количество используемых БАТ - до 40. Объем вводимого препарата от 0,3 до 0,5 мл/БАТ.
Рост ребенка на начало курса обкалывания составлял 85 см. После этого в течение 9 месяцев ребенок подрос на 5 см. Первые 3 месяца - 3 см; следующие 3 месяца- 1,5 см; следующие 3 месяца- 0,5 см.
В мае-октябре 2009 г. (через год) был проведен второй курс акупунктурного введения Аллопланта по той же схеме. После чего за 6 месяцев ребенок прибавил вросте еще 5 см. При этом рост костей туловища и конечностей происходил согласно возрастным пропорциям.
После этого в декабре этого же 2009г. была проведена вторая операция на коленных суставах, подобная операции в 2005г. при росте 96 см., после которой сразу рост был увеличен на 11 см.
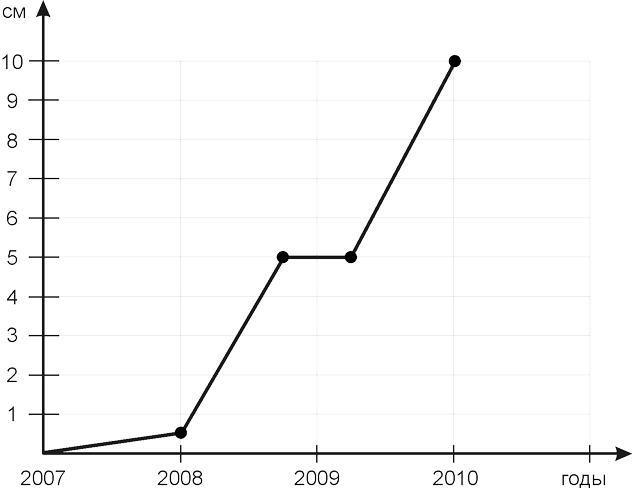
Рис. 1 Динамика роста на фоне акупунктурного введения диспергированного аллогенного биоматериала Аллоплант.
В июле 2010 г. мы провели третий курс акупунктурного введения Аллопланта. На момент последнего визита рост пациента - 105 см. В ноябре 2010 г. - 107 см. За 4 месяца прибавил рост на 2 см.
Заключение
После каждого проведенного курса акупунктурного введения Аллопланта во временном интервале от 6 до 9 месяцев пациент прибавлял в росте на 5 см. За период с марта 2008 г. по декабрь 2009 г. только на фоне акупунктурного введения диспергированного аллогенного биоматериала Аллоплант, пациент увеличил рост на 10 см.
Ранее такая динамика была возможной только после оперативного вмешательства.
Приведенный клинический пример указывает на принципиальную возможность использования фармакопунктуры биоматериалом Аллоплант в комплексном лечении больных с ахондроплазией.
к содержанию | опубликовать статью
ОПЕРАЦИЯ ЛЕЧЕБНОГО РЕТРОСКЛЕРОПЛОМБИРОВАНИЯ ДИСПЕРГИРОВАННЫМ БИОМАТЕРИАЛОМ АЛЛОПЛАНТ В ЛЕЧЕНИИ ДИАБЕТИЧЕСКОЙ РЕТИНОПАТИИ
Султанов Р.З.
"ФГБУ Всероссийский центр глазной и пластической хирургии" Минздравсоцразвития России
Экспериментально-морфологическими методами установлено, что операция лечебного ретросклеропломбирования с применением диспергированного биоматериала Аллоплант способствует рассасыванию внутриглазного кровоизлияния и нормализации гистологической картины сетчатки. Данная операция применена при лечении диабетической ретинопатии и установлены показания для ее выполнения у больных диабетической ретинопатией с отечно-геморрагическим синдромом.
Актуальность Количество больных сахарным диабетом составляет 4-5% населения развитых стран, ежегодно увеличиваясь на 5-7% (А.П. Калинин, 1998; S.E. Skorman, 1987). Успешная заместительная терапия инсулиновой недостаточности позволила приблизить продолжительность жизни больных сахарным диабетом к среднестатистической, что привело к увеличению продолжительности заболевания и к росту количества больных с сосудистыми осложнениями. Наиболее часто встречающимся сосудистым осложнением диабетического процесса является диабетическая ретинопатия, которая определяется у 10-100% больных в зависимости от давности и тяжести течения основного заболевания (Э.П. Касаткина, 1990; Л.А. Кацнельсон, 1990; М. Кохен, 1998; Л.К. Дудникова, 1999).
Патогенез диабетической ретинопатии определяется нарушением углеводного обмена при сахарном диабете. На местном уровне формируется порочный круг, включающий диффузную ретинальную гипоксию, усиление анаэробного метаболизма сетчатки, развитие местного ацидоза, микроангиопатию, венозный застой, с последующим формированием участков глубокой гипоксии сетчатки и развитием пролиферативных процессов (А.П. Нестеров, 1996).
Существует большое количество методов лечения диабетической ретинопатии: комплексная медикаментозная терапия (С.В. Гольцева, 1983; В.И. Белоус, 1987, 1990; А.И. Муха, 1990; М. Косанович, 1992), лазеркоагуляция сетчатки (Л.А. Кацнельсон, 1991; P.K. Khosla, 1993; А.П. Калинин, 1998), трансцилиарная витрэктомия (А.К. Кривицкий, 1990; Я.И. Глинчук, 1993, 1995; A.E. Kreiger, 1993; N.A. Chaudhry, 1995), периферическая криокоагуляции сетчатки (Л.А. Кацнельсон, 1995; R. De Bara, 1989; N. Ando, 1991), реваскуляризация хориоидеи эписклеральным лоскутом (О.В.Родионов, 1997, 1999). Однако, несмотря на многообразие методов лечения, диабетическая ретинопатия по-прежнему остается ведущей причиной слепоты больных сахарным диабетом (Л.К. Дудникова, 1999; Moss S.E. et al., 1994).
Отсутствие безопасного, эффективного, несложного по технике выполнения хирургического способа лечения диабетической ретинопатии заставило нас обратить внимание на экстрасклеральные способы улучшения кровообращения заднего отдела глазного яблока с использованием ауто-, алло-, ксенотрансплантатов и эксплантатов. Эти операции применяли для лечения миопической болезни и центральной хориоретинальной дистрофии (М.С. Ремизов, 1981; М.В. Зайкова, 1984, 1993; Т.В. Баталова, 1987; Н.В. Ковыль, 1990; С.В. Уварова, 1991; Ю.А. Чеглаков, 1995, 1996, 1997).
Учитывая патогенез диабетической ретинопатии, представляет интерес изучение возможности применения и определение эффективности экстрасклеральной пластики диспергированным биоматериалом Аллоплант со сниженными антигенными свойствами при лечении диабетической ретинопатии. Данный вид биоматериала серийно выпускается в лаборатории по производству трансплантатов Всероссийского центра глазной и пластической хирургии (ТУ 42-2-537-99, Аллотрансплантат для офтальмологии и пластической хирургии) и обладает высокой биологической активностью в регуляции регенераторных процессов, высокой иммунотропной активностью, оказывает выраженное активирующее влияние на клетки макрофагального ряда (Р.С. Мингазов, 1994; И.А. Сафин, 1994; В.У. Галимова, 1998; Ш.А. Зарипов, 1998; А.Х. Мустафин, 1998; Р.А. Хасанов, 1999).
Исходя из всего вышеизложенного цель исследования: установить возможность применения и определить эффективность лечебного ретросклеропломбирования диспергированным биоматериалом Аллоплант при отечно-геморрагической форме диабетической ретинопатии.
Материалы и методы исследования
Экспериментальные исследования были проведены на 24 кроликах, которым был смоделирован гемофтальм путем введения в стекловидное тело 0,3мл аутологичной крови. Опытной группе кроликов (16 кроликов) непосредственно после моделирования гемофтальма была проведена операция лечебного ретросклеропломбирования диспергированным аллогенным биоматериалом. Животных выводили из эксперимента на 6, 14, 30, 60 сутки путем передозировки тиопентала натрия.
Методы экспериментального исследования:
- витальная биомикро- и офтальмоскопия с оценкой выраженности внутриглазного кровоизлияния по экспертной балльной системе;
- микроскопическое исследование с окраской пикрофуксином, гематоксилином и эозином.
Анализ результатов хирургического лечения был проведен у 124 пациентов (160 глаз) с отечно-геморрагической формой диабетической ретинопатии. Пред- и послеоперационные исследования больных включали: визометрию, кинетическую периметрию по Гольдману, компьютерную периметрию, электротонографию, электрофизиологические исследования, биомикро- и офтальмоскопию с экспертной балльной оценкой состояния оптических сред глаза, выраженности внутриглазного кровоизлияния (по Kokutei K., 1993) и состояния глазного дна (по классификации В.И.Ивериели и Э.А.Чкония, 1981), фотосъемку глазного дна, флюоресцентную ангиографию. Все пациенты прошли послеоперационное обследование в сроки 14 суток, 1, 3, 6, 12, 24, 36 месяцев.
Изначально пациенты были разделены на три группы по стадии заболевания: 1) имеющие непролиферативную ретинопатию – 36 человек, 46 глаз; 2) имеющие препролиферативную ретинопатию – 32 человека, 46 глаз, 3) имеющие пролиферативную ретинопатию – 56 человек, 68 глаз. Пациенты этих групп имели приблизительно равное распределение по полу, среднему возрасту (48,87±3,03 лет, 56,3±3,8 лет, 48,03±2,7 лет, соответственно) средней давности заболеваемости сахарным диабетом (15,91±1,28 лет, 15,39±1,65 лет, 15,0±1,45 лет, соответственно). В группе с непролиферативной ретинопатией количество пациентов первого и второго типов сахарного диабета было одинаковым. В группах с препролиферативной и пролиферативной ретинопатией преобладали пациенты с первым типом сахарного диабета с тяжелым, нестабильным течением диабета в стадии субкомпенсации. Ранее медикаментозное лечение диабетической ретинопатии было проведено в 56,5% случаев в непролиферативной группе, в 52,18% - в препролиферативной группе и в 97% - в пролиферативной. Лазеркоагуляция ранее была проведена в 13% случаев в непролиферативной группе, в 13,04% - в препролиферативной группе, в 53% - в пролиферативной. Витрэктомия ранее была проведена в 13,75% случаев в группе пролиферативной ретинопатии. У всех больных до операции наблюдали отечно-геморрагические проявления диабетической ретинопатии. У большинства пациентов отмечали снижение остроты зрения за последний год перед операцией (100%, 91,3%, 82,35%, соответственно) с градиентом снижения 0,21±0,03 (1 группа), 0,25±0,04 (2 группа), 0,28±0,04 (3 группа). Из приведенных данных видно, что хирургическое лечение проводили пациентам с большим сроком от начала заболевания сахарным диабетом и прогрессивной потерей зрительных функций.
Все пациенты в до- и в послеоперационный период находились под наблюдением эндокринолога городского эндокринологического центра. При необходимости им проводили коррекцию общего соматического состояния.
Полученные данные обрабатывали методом сравнения попарно-связанных выборок с использованием t-критерия Стьюдента для зависимых выборочных совокупностей. Значимыми считали различия при p<0,05. Для наглядности наиболее информативные состояния зрительного анализатора представлены в относительных единицах - процент, где дооперационный уровень принят за 100%. Качественные изменения в группах наблюдения по различным признакам оценивали также и по критерию “лучше / без изменений / хуже” относительно дооперационного уровня. Кроме того, проводили группирование больных, характеризующихся сходным предоперационным статусом и их автоматическую классификацию. Все расчеты производили с помощью пакетов прикладных программ Statistica for Windows v.5.0 и ГРАНД.
Всем указанным пациентам была проведена операция лечебного ретросклеропломбирования диспергированным биоматериалом Аллоплант. Суть данного хирургического вмешательства заключалась в том, что через изогнутую по кривизне глазного яблока тупоконечную иглу, введенную к заднему полюсу глазного яблока между теноновой капсулой и склерой, иньецировали суспензию биоматериала Аллоплант (рис. 1). Последнюю готовили непосредственно перед операцией следующим образом: содержимое ампулы (200мг порошка) разводили в 2мл 0,9% раствора NaCl и набирали в шприц толстой иглой.
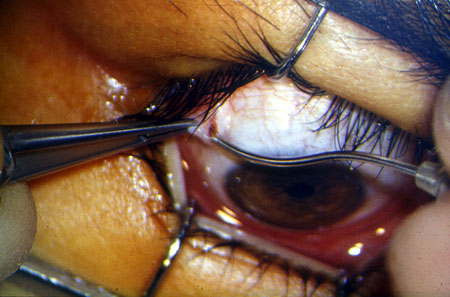 |
|---|
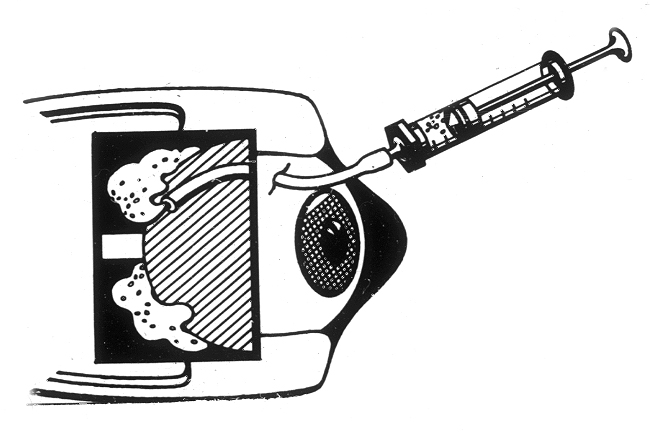 |
| Рис. 1 Введение иглы в субтеноново пространство к заднему полюсу глазного яблока и схема операции. |
Экспериментально-морфологические исследования
На модели гемофтальма было показано, что операция лечебного ретросклеропломбирования диспергированным биоматериалом Аллоплант не приводит к каким-либо отрицательным последствиям.
В опытной группе происходила стимуляция фагоцитарной активности клеток, результатом чего явилось полное рассасывание гемофтальма и восстановление гистологической картины сетчатки к конечному сроку наблюдения.
В контрольной группе (без введения биоматериала) к конечному сроку происходила дегенерация нейронов сетчатки с замещением их клетками нейроглии. В опытной группе происходила пролиферация прекапилляров и капилляров сетчатки. Данный феномен отсутствовал в контрольной группе. Следовательно неоваскуляризация в данном случае не связана с патологическим процессом.
Можно предположить, что описанное биологическое влияние диспергированного биоматериала Аллоплант обусловлено короткодистантным моделируюшим действием протеогликанов Аллопланта, а также монокинами, которые выделяются активированными макрофагами и фибробластами в зоне введения диспергированного биоматериала. Поэтому применение этой операции при диабетической ретинопатии мы посчитали обоснованным и достаточно безопасным.
Клиническая оценка результатов операции лечебного ретросклеро-пломбирования диспергированным биоматериалом Аллоплант
Установлено, что этот способ введения биологического материала в субтеноновое простраство не приводил к интра- и послеоперационным осложнениям. У пациентов с отечно-геморрагической формой диабетической ретинопатии повышение остроты зрения (рис. 2) начиналось с ближайших сроков наблюдения и достигало максимума к 3-6 месяцам после операции (1 группа – в 1,28 раза, 2 группа – в 1,56 раза, 3 группа – 1,59 раза).
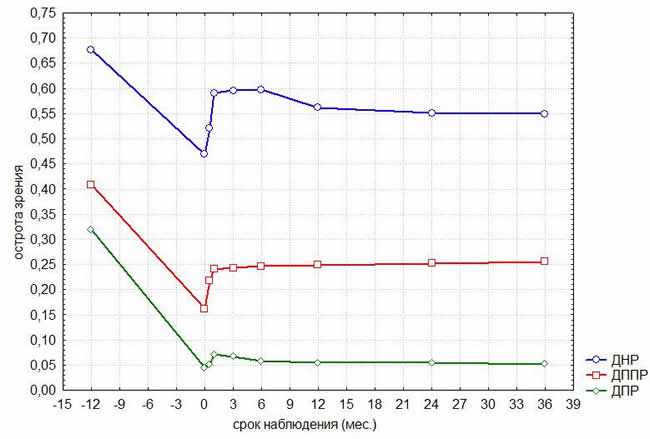 |
|---|
| Рис. 2 Динамика остроты зрения после операции лечебного ретросклеропломбирования у пациентов с диабетической непролиферативной, препролиферативной и пролиферативной ретинопатией. |
В эти сроки наблюдения прирост остроты зрения наблюдался в 82,6% случаев (1 группа), в 65,22% случаев (2 группа), 41,2% (3 группа), стабилизация остроты зрения на дооперационном уровне в 8,7% случаев (1 группа), в 13,04% (2 группа), в 29,4% (3 группа).
В последующий период наблюдений острота зрения стабилизировалась на достигнутом уровне в группах с диабетической непролиферативной и препролиферативной ретинопатией.
В группе с пролиферативной ретинопатией острота зрения снижалась, однако, оставалась выше дооперационного уровня. Такие же изменения, во всех трех группах, отмечались в отношении светочувствительности центрального поля зрения.
Повышение остроты зрения обуславливалось повышением прозрачности стекловидного тела и рассасыванием внутриглазных кровоизлияний (рис. 3), минимальный уровень которых приходился также на 3-6 месяц послеоперационного наблюдения (0,079±0,039 баллов и 0,129±0,045 баллов – 1 группа, 1,00±0,077 баллов и 0,588±0,085 баллов – 2 группа, 1,478±0,112 баллов и 0,679±0,081 баллов – 3 группа, соответственно). В третьей группе снижение уровня внутриглазных геморрагий не приводит к полному просветлению стекловидного тела, поскольку помутнения представлены не элементами крови, а его фиброзом.
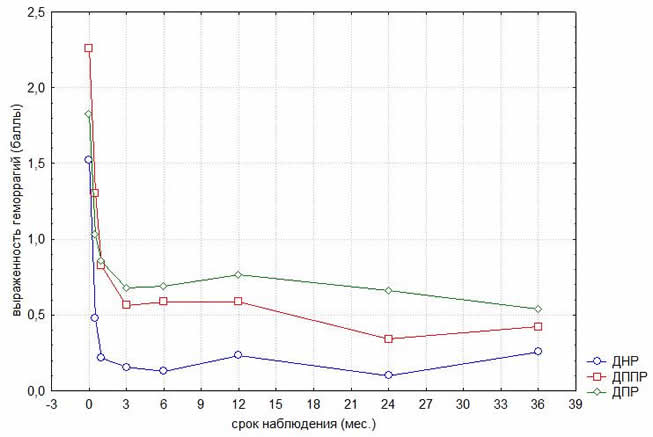 |
|---|
| Рис. 3 Изменения состояния внутриглазных геморрагий после операции лечебного ретросклеропломбирования у пациентов с диабетической непролиферативной, препролиферативной и пролиферативной ретинопатией. |
В группах с непролиферативной и препролиферативной ретинопатией наблюдали стабилизацию состояния хрусталика на дооперационном уровне. В группе с пролиферативной ретинопатией отмечали достоверное помутнение хрусталика, вызванное изначальным нарушенным состоянием обмена в тканях глазного яблока.
Достоверное сужение площади среднего суммарного поля зрения ко 2-3 году послеоперационного наблюдения можно объяснить нарастанием дистрофических процессов на глазном дне. В первой и второй группах эти изменения были незначительными, и проявлялись только к конечному сроку наблюдения. В третьей группе, изначально имевшей пролиферативные изменения на глазном дне, продолжающийся фиброз привел к достоверному сужению суммарного поля зрения уже к первому году после операции, с последующим ухудшением к конечным срокам наблюдения. Эти выводы подтверждаются изменениями пороговой электрочувствительности в послеоперационном периоде. Если в первых двух группах изменения указывали на стабилизацию процесса, то в группе с пролиферативной ретинопатией определяли явную тенденцию к повышению порога электрочувствительности, имевшего начально высокий уровень. Изменения показателей критической частоты слияния электрофосфена также указывали на стабилизацию процесса в группах непролиферативной, препролиферативной ретинопатии и ухудшение состояния в группе пролиферативной ретинопатии.
Снижение истинного внутриглазного давления в ближайшие послеоперационные сроки наблюдения (в пределах нормы) происходило за счет уменьшения продукции камерной влаги (F) и протекало параллельно с рассасыванием внутриглазных кровоизлияний. Это связано с угнетающим действием продуктов перекисного окисления липидов, возникающих вследствие распада элементов крови, на функцию цилиарного тела (Р.Б. Агаева 1991; Р.В. Гаджиев 1985; Я.И. Глинчук 1995).
Первоначальная автоматическая факторизация признаков подтвердила, что изначально острота зрения при диабетической ретинопатии зависит от: 1) состояния прозрачности стекловидного тела и выраженности отечно-геморрагического синдрома (фактор геморрагий) и 2) состояния глазного дна и, связанного с этим, показателей пороговой электрочувствительности, электролабильности и полей зрения (фактор пролиферации). В результате классификации пациентов с диабетической ретинопатией по этим двум факторам, автоматически были выделены группы пациентов, условно соответствующие стадийности патологического процесса: диабетическая непролиферативная ретинопатия – кластер A, диабетическая препролиферативная ретинопатия – кластер B, диабетическая пролиферативная ретинопатия – кластер C. Кроме того, в отдельную группу автоматически были выделены пациенты с высокой степенью выраженности отечно-геморрагического синдрома – кластер D (. 4).
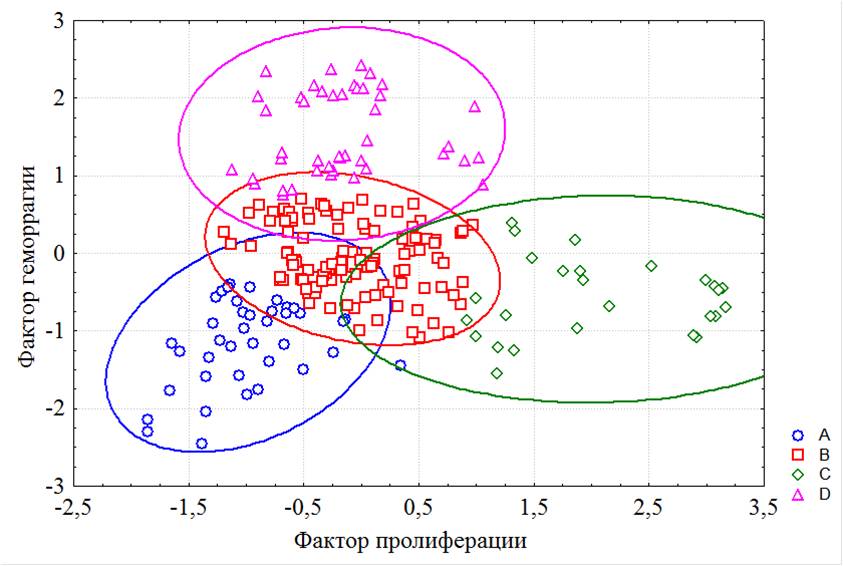 |
|---|
| Рис. 4 Расположение кластер-групп на плоскости факторов. |
Выявленные кластеры отличались друг от друга начальными функциональными показателями зрительной системы (таб.1). Кроме того, пациенты кластера С были представлены, в основном, объектами, имевшими тяжелое нестабильное течение сахарного диабета.
| Кластер А | Кластер B | Кластер C | Кластер D | |
|---|---|---|---|---|
| Острота зрения | 0,47±0,04 | 0,08±0,01 | 0,01±0,005 | 0,06±0,02 |
| Поля зрения | 459,9±11,0 | 371,6±11,3 | 124,4±38,4 | 373,6±24,5 |
| ПЭЧ | 113,8±10,0 | 190,4±15,3 | 702,1±61,6 | 132,7±50,5 |
| ЭЛ | 41,34±1,13 | 36,29±1,41 | 7,1±1,7 | 45,86±3,47 |
| Po | 15,45±0,46 | 14,65±0,46 | 16,40±0,77 | 13,97±0,84 |
| Стекловидное тело | 0,67±0,07 | 1,44±0,09 | 2,30±0,21 | 3,29±0,20 |
| Выраженность геморрагий | 1,44±0,07 | 1,97±0,08 | 1,30±0,11 | 3,71±0,13 |
| Состояние глазного дна | 2,37±0,11 | 3,56±0,11 | 5,40±0,16 | 3,43±0,14 |
Кластеры имели различную динамику зрительных функций в послеоперационном периоде. У пациентов кластера A уже в первые сроки наблюдения после операции определяли достоверное повышение остроты зрения с последующей стабилизацией на уровне выше дооперационного (рис. 5). Повышение остроты зрения было, несомненно, связано с повышением прозрачности стекловидного тела и уменьшением выраженности отечно-геморрагического синдрома.
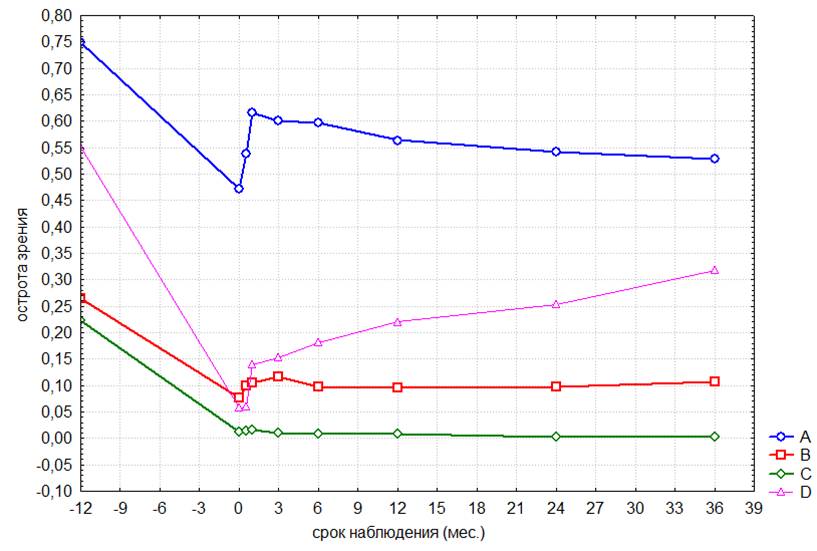 |
|---|
| Рис. 5 Динамика остроты зрения после операции лечебного ретросклеропломбирования у пациентов кластеров A, B, C и D (метод попарно-связанных средних). |
Незначительное сужение среднего суммарного поля зрения к конечным срокам наблюдения было обусловлено нарастанием дистрофических изменений на глазном дне в пределах балльной оценки непролиферативной ретинопатии. Незначительность изменений состояния глазного дна подтверждается стабилизацией площади суммарного поля зрения, показателей порога электрочувствительности и электролабильности.
Острота зрения пациентов кластера B достоверно улучшалась в ближайшие 3 месяца после операции, в последующем несколько снижалась и стабилизировалась на уровне, выше дооперационного. Также как и в первой группе, повышение остроты зрения тесно связано с рассасыванием внутриглазных геморрагий и повышением прозрачности стекловидного тела. Однако, в этой группе мы наблюдали достоверное ухудшение состояния глазного дна в сторону пролиферативной ретинопатии. Это обусловило достоверное сужение среднего суммарного поля зрения, повышение порога электрочувствительности к конечным срокам наблюдения.
Изменения остроты зрения пациентов кластера C характеризуются стабилизацией в ближайшие сроки наблюдения (до 3 месяцев после операции) с последующим снижением до уровня, ниже дооперационного. В эти же сроки наблюдения (до 3 месяцев после операции) происходит расширение полей зрения, снижение порога электрочувствительности и повышение электролабильности. Однако, ввиду дальнейшего прогрессирования фиброзных изменений на глазном дне, мы наблюдали сужение полей зрения, повышение пороговой электрочувствительности выше исходного уровня, снижение уровня электролабильности. В кластерах B и C не происходило полного просветления стекловидного тела, поскольку помутнения его были представлены элементами фиброза.
В кластере D мы наблюдали наибольший прирост остроты зрения с максимальным уровнем к конечному сроку наблюдения. Это было связано с рассасыванием обширных геморрагий и повышением прозрачности стекловидного тела на протяжении всего периода наблюдения и незначительными изменениями со стороны глазного дна. Состояние глазного дна, полей зрения, порога электрочувствительности и электролабильности оставались стабильными в течение 3 лет наблюдения.
Если в первых трех кластерах изменения истинного внутриглазного давления были незначительными и сводились к уменьшению в ближайший послеоперационный период с последующим ростом до предоперационного уровня, то в кластере D мы наблюдали резкое снижение истинного внутриглазного давления в ближайший год после операции до уровня нижней границы нормы, с последующим восстановлением ко 2 году после операции. Снижение истинного внутриглазного давления во всех четырех кластерах определялось снижением продукции внутриглазной жидкости. Прослеживали четкую параллель между степенью выраженности внутриглазных геморрагий до операции и степенью уменьшения продукции камерной влаги (F), а, значит, и снижением внутриглазного давления после оперативного вмешательства. Рассасывание внутриглазных геморрагий в ближайшие 6 месяцев после введения биоматериала Аллоплант и достижение определенной степени прозрачности стекловидного тела определяли фазу восстановления продукции камерной влаги и внутриглазного давления.
Изменения степени прозрачности хрусталика после операции также были тесно связаны с выраженностью внутриглазного кровоизлияния до операции – чем выше степень геморрагий, тем быстрее нарастают изменения в хрусталике.
Сопоставляя полученные результаты с данными литературы по применению лазеркоагуляции, криокоагуляции, витрэктомии, операции реваскуляризации хориоидеи, медикаментозного лечения, можно констатировать, что лечебное ретросклеропломбирование биоматериалом Аллоплант не менее эффективно в лечении диабетической ретинопатии. Кроме того, у части пациентов данная операция была проведена при состоянии прозрачности оптических сред, не позволяющих использовать лазеркоагуляцию сетчатки. Анализируя результаты витрэктомии и реваскуляризации хориоидеи, можно отметить, что предложенный хирургический метод имеет эффективность, сходную с вышеуказанными методиками при неосложненных пролиферацией формах диабетической ретинопатии. Однако, отсутствие интра- и послеоперационных осложнений лечебного ретросклеропломбирования биоматериалом Аллоплант делает эту операцию более предпочтительной при выборе методик лечения неосложненных пролиферацией форм диабетической ретинопатии. Вместе с тем, предложенный нами метод не исключает применение витрэктомии и реваскуляризации хориоидеи, не усложняет их выполнение и может быть использован в сочетании с ними.
Таким образом, лечебное ретросклеропломбирование биоматериалом Аллоплант является малотравматичным, безопасным и эффективным хирургическим вмешательством при неосложненных обширной пролиферацией формах диабетической ретинопатии и может быть применено на этапах медико-социальной реабилитации этой тяжелой группы пациентов.
ЗАКЛЮЧЕНИЕ
Операция лечебного ретросклеропломбирования биоматериалом Аллоплант является эффективным, малотравматичным и безопасным методом лечения больных с отечно-геморрагической формой диабетической ретинопатии.
В эксперименте установлено, что диспергированный аллогенный биоматериал, введенный в субтеноново пространство при операции лечебного ретросклеропломбирования, подвергается полной резорбции, без признаков рубцевания окружающих тканей, способствует полному рассасыванию внутриглазного кровоизлияния и нормализации гистологической картины сетчатки.
Операция лечебного ретросклеропломбирования диспергированным биоматериалом Аллоплант у больных с отечно-геморагической формой непролиферативной диабетической ретинопатии, достоверно улучшает остроту зрения в 1,28 раза и стабилизирует ее у 82,6% пациентов в течение 3 лет наблюдения.
У больных с отечно-геморагической формой препролиферативной диабетической ретинопатии эта операция достоверно улучшает остроту зрения в 1,56 раза и стабилизирует ее у 73,9% пациентов в течение 3 лет наблюдения.
При отечно-геморагической форме пролиферативной диабетической ретинопатии эта операция только стабилизирует остроту зрения у 55,9% больных.
Операция лечебного ретросклеропломбирования диспергированным биоматериалом Аллоплант показана при всех стадиях диабетической ретинопатии, сопровождающихся отечно-геморрагическим синдромом; она оказывает стабилизирующее действие при далекозашедших нейродистрофических изменениях глазного дна и неэффективна при выраженной витреоретинальной пролиферации и тракционной отслойке сетчатки.
ПРАКТИЧЕСКИЕ РЕКОМЕНДАЦИИ
Для лечения и реабилитации больных с отечно-геморрагической формой диабетической ретинопатии рекомендуется операция лечебного ретросклеропломбирования диспергированным биоматериалом Аллоплант, которая не требует дорогостоящего оборудования, проста по технике выполнения и может быть применена в условиях обычного офтальмологического отделения как в стационарных, так и в амбулаторных условиях.
Предлагаемая операция, при наличии соответствующих показаний, может быть применена в сочетании с другими видами лечения диабетической ретинопатии (медикаментозная терапия, лазеркоагуляция сетчатки, витрэктомия, операция реваскуляризации хориоидеи).
ЛИТЕРАТУРА
- Хирургическое лечение внутриглазных кровоизлияний при диабетической ретинопатии: Тез. докл. IV науч.-практ. конф. «Новые технологии микрохирургии глаза». – Оренбург, 1995. – С. 93-94. (Соавторы: Родионов О.В.).
- Иммунологические аспекты применения порошкообразных трансплантатов для инъекций серии аллоплант при диабетической ретинопатии: Тез. докл. IV науч. конф. «Нейроиммунология, нейроинфекции, нейроимидж». - Санкт-Петербург, 1995. – С. 106. (Соавторы: Сибиряк С.В., Мулдашев Э.Р., Курчатова Н.Н., Евстифеева Т.А., Киреев В.Л.).
- Операция лечебного ретросклеропломбирования диспергированным биоматериалом Аллоплант в лечении диабетической ретинопатии//Bulg. J. Ophthalmol.- Кн.1, - София, 1996. – С. 9-11.
- Опыт организации офтальмоэндокринологической помощи: Тез. докл. V науч.-практ. конф. офтальмологов «Новые технологии микрохирургии глаза». – Оренбург, 1996. – С. 15-16. (Соавторы: Мулдашев Э.Р., Родионов О.В., Галимова В.У.).
- Состояние гемогидродинамики глаза у больных с диабетической ретинопатией после вазолимфореконструктивных операций: Тез. докл. V науч.-практ. конф. офтальмологов «Новые технологии микрохирургии глаза». – Оренбург, 1996. – С. 148-149. (Соавторы: Родионов О.В, Галимова В.У., Мустафин М.М.).
- Отдаленные результаты после вазолимфореконструктивных операций в лечении отечно-геморрагических форм диабетической ретинопатии: Тез. докл. V науч.-практ. конф. офтальмологов «Новые технологии микрохирургии глаза». – Оренбург, 1996. – С. 150-151. (Соавторы: Родионов О.В., Галимова В.У, Киреев В.Л.).
- Компьютерная периметрия в оценке зрительного анализатора у пациентов с диабетической ретинопатией: Тез. докл. Всерос. науч.-практ. конф., посвященной 95-летию со дня рождения Т.И.Ерошевского. – Самара, 1997. – С. 148-149. (Соавторы: Родионов О.В., Мухамадеев Р.А., Галимова В.У.).
- Лечебное ретросклеропломбирование в лечении диабетической ретинопатии: Тез. докл. Всерос. науч.-практ. конф., посвященной 95-летию со дня рождения Т.И.Ерошевского. – Самара, 1997. – С. 284-287. (Соавторы: Родионов О.В., Булатов Р.Т., Галимова В.У.).
- Реваскуляризирующая хирургия диабетической ретинопатии: Тез. докл. первой Евро-азиатской конф. по офтальмологии. – Екатеринбург, 1998. – С. 85. (Соавторы: Мулдашев Э.Р., Родионов О.В., Ларин А.И.).
- Состояние центрального поля зрения у больных с диабетической ретинопатией: Тез. докл. первой Евро-азиатской конф. по офтальмологии. – Екатеринбург, 1998. – С. 86. (Соавторы: Родионов О.В., Мухамадеев Р.А., Ларин А.И.).
- Диспергированный биоматериал аллоплант в лечении диабетической ретинопатии: Тез. докл. первой Евро-азиатской конф. по офтальмологии. – Екатеринбург, 1998. – С. 87. (Соавторы: Родионов О.В., Ларин А.И., Булатов Р.Т.).
- Поляризационно-оптический анализ репаративной регенерации при аллотрансплантации: Тез. докл. VI науч.-практ. конф. по вопросам хирургического лечения заболеваний органа зрения. – Екатеринбург, 1998. – С. 28. (Соавторы: Родионов О.В., Булатов Р.Т., Скалдина О.А., Муслимов С.А., Ларин А.И.).
- Иммунологические аспекты операции ретросклеропломбрования биоматериалом Аллоплант: Тез. докл. VI науч.-практ. конф. по вопросам хирургического лечения заболеваний органа зрения. – Екатеринбург, 1998. – С. 29-32. (Соавторы: Булатов Р.Т., Сибиряк С.В., Родионов О.В., Яковлева В.Г.).
- Отдаленные результаты реваскуляризирующих операций у больных с диабетической ретинопатией: Тез. докл. науч.-практ. конф. офтальмологов «Диабет глаза». – Оренбург, 1999. – С. 32-33. (Соавторы: Родионов О.В., Мулдашев Э.Р., Ларин А.И., Булатов Р.Т.).
- Применение диспергированного биоматериала Аллоплант для коррекции внутриглазной патологии: Тез. докл. VII науч.-практ. конф. по вопросам хирургического лечения заболеваний органа зрения. – Екатеринбург, 1999. – С. 133-135. (Соавторы: Муслимов С.А., Шумкин А.М.).