СОДЕРЖАНИЕ НОМЕРА
МОРФОЛОГИЯ КРЫЛОВИДНО-ВЕРХНЕЧЕЛЮСТНОЙ ЩЕЛИ ПРИ РАЗЛИЧНОЙ ФОРМЕ ЧЕРЕПА У ВЗРОСЛЫХ ЛЮДЕЙ ГОУ ВПО Полковова И.А., Алешкина О.Ю.
ОБЗОР РОССИЙСКОЙ НАУЧНО-ПРАКТИЧЕСКОЙ КОНФЕРЕНЦИИ С МЕЖДУНАРОДНЫМ УЧАСТИЕМ «НОВЫЕ ТЕХНОЛОГИИ МИКРОХИРУРГИИ ГЛАЗА (ОФТАЛЬМОПАТОЛОГИЯ ДЕТСКОГО ВОЗРАСТА)», 17-19 ДЕКАБРЯ 2008 Г., Г. ОРЕНБУРГ Нигматуллин Р.Т.
ПЕРВИЧНАЯ ЭСТЕТИЧЕСКАЯ РЕАБИЛИТАЦИЯ ПАЦИЕНТОВ ПОСЛЕ СУБТОТАЛЬНОЙ РЕЗЕКЦИИИ ОКОЛОУШНОЙ СЛЮННОЙ ЖЕЛЕЗЫ
Мулдашев Э.Р., Вырупаев С.В., Гайфуллин С.Н., Щербаков Д.А.
АНАТОМОМЕТРИЧЕСКАЯ ХАРАКТЕРИСТИКА ПИЩЕВОДА В ГРУДНОМ ВОЗРАСТЕ Баландина И.А., Еремченко Н.В.
КЛИНИЧЕСКИЙ СЛУЧАЙ ПРИМЕНЕНИЯ БИОМАТЕРИАЛОВ СЕРИИ АЛЛОПЛАНТ ПРИ ЛЕЧЕНИИ ПРОБОДНОЙ ЯЗВЫ РОГОВИЦЫ
А. Г. Ямлиханов
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ВРОЖДЕННОЙ ГЛАУКОМЫ С ИСПОЛЬЗОВАНИЕМ БИОМАТЕРИАЛА АЛЛОПЛАНТ Галимова В.У., Полякова Е.Ю.
ПРИМЕНЕНИЕ ДИСПЕРГИРОВАННОГО БИОМАТЕРИАЛА АЛЛОПЛАНТ ДЛЯ ЛЕЧЕНИЯ ПОРАЖЕНИЙ ПЕРЕДНЕГО СЕГМЕНТА ГЛАЗНОГО ЯБЛОКА
Булатов Р.Т., Белова Е.А.
Публикации 2009г.
МОРФОЛОГИЯ КРЫЛОВИДНО-ВЕРХНЕЧЕЛЮСТНОЙ ЩЕЛИ ПРИ РАЗЛИЧНОЙ ФОРМЕ ЧЕРЕПА У ВЗРОСЛЫХ ЛЮДЕЙ
Полковова И.А., Алешкина О.Ю.
ГОУ ВПО «Саратовский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию» Полковова И.А., Алешкина О.Ю.
Современные методы диагностики и технологии оперативных вмешательств при заболеваниях и повреждениях труднодоступных областей черепа и их содержимого невозможны без знания закономерностей строения и вариантов формы черепа как целостной системы и точных размеров его локальных структур. Однако при множестве описательных и экспериментальных данных ощущается недостаток теоретических и обобщающих работ по морфологии труднодоступных структур черепа. Это целиком относится к морфологии крыловидно-верхнечелюстной щели, являющейся «входными воротами» в крыловидно-нёбную ямку с её важными сосудисто-нервными образованиями и коммуникациями. Многие авторы указывают на то, что эффективность диагностики и оперативного лечения, связанных с патологией сосудисто-нервного пучка в крыловидно-нёбной ямке, невозможна без знания анатомической изменчивости крыловидно-верхнечелюстной щели, ее морфофункциональных связей с прилежащими структурами мозгового и лицевого черепа. Несмотря на то, что достаточно подробно изучены морфология крыловидно-нёбной ямки, морфометрические характеристики крыловидного узла, верхнечелюстного нерва и артерии, лишь в единичных работах встречаются некоторые краниометрические данные о крыловидно-верхнечелюстной щели. В связи с этим актуально комплексное морфо-топометрическое исследование полового диморфизма, типовой и возрастной изменчивости крыловидно-верхнечелюстной щели в системе черепа в целом для последующего использования в диагностической и оперативной видеоэндоскопической нейрохирургии; рентгеновской, компьютерной и магнитно-резонансной томографиях, в выборе тактики нейро- и ортодонтических вмешательств.
Обзор российской научно-практической конференции с международным участием «Новые технологии микрохирургии глаза (офтальмопатология детского возраста)», 17-19 декабря 2008 г., г. Оренбург
Р.Т. Нигматуллин
ФГУ «Всероссийский центр глазной и пластической хирургии», г.Уфа
На базе Оренбургского филиала ФГУ МНТК «Микрохирургия глаза» состоялась традиционная ежегодная конференция, посвященная новым технологиям микрохирургии глаза. Приоритетами в данной конференции были выбраны методы лечения офтальмологической патологии в детском возрасте.
На I пленарном заседании интерес вызвали выступления следующих докладчиков:
- Метаев С.А. «Хирургическое лечение отслоек сетчатки с применением технологии 25G», (г. Москва);
- Шацких А.В. «Хирургическое лечение врожденной катаракты у пациента с первичным гиперпластическим персистирующим стекловидным телом. Клинический случай», (г.Москва);
- Кононов Л.Б. «Показания к первичной имплантации ИОЛ и особенности хирургической техники у детей с врожденными катарактами первого года жизни», (г.Москва).
На II пленарном заседании был представлен доклад Кашура О.И. с соавт. «Распространенность, структура и результаты лечения ретинопатии недоношенных в Хабаровском крае», который был посвящен анализу распространенности и результатам реабилитации больных с врожденной патологией в регионе.
На III пленарном заседании выступили докладчики из различных офтальмологических клиник городов Москвы, Самары, Оренбурга, Краснодара:
- Агафонова В.В. «Возможности метода оптической когерентной томографии для определения анатомо-топографического состояния экстраокулярных мышц» (г.Москва);
- Кадникова О.В. «ИАГ – лазерная дисцизия вторичной катаракты у детей» (г.Оренбург);
- Стебнев В.С. «Первичная витректомия в хирургии регматогенной отслойки сетчатки» (г.Самара).
Также в конференции приняли активное участие сотрудники ФГУ «Всероссийский центр глазной и пластической хирургии», г.Уфа:
- Карушин О.И. «Комплексное лечение первичной глаукомы с нормализованным офтальмотонусом»;
- Кадыров Р.З. «Результаты хирургического лечения воспалительных заболеваний роговицы биоматериалов Аллоплант»;
- Кульбаев Н.Д. «Использование офтальмологического тренажера для обучения врачей – офтальмохирургов».
На заседании круглого стола «Высокие технологии в офтальмопатологии детского возраста» приняли участие:
- Канюков В.Н. – профессор, директор Оренбургского филиала ФГУ МНТК «Микрохирургия глаза»;
- Агафонова В.В. – д.м.н., ученый секретарь Ученого совета ФГУ МНТК «Микрохирургия глаза»;
- Каган И.И. – профессор, заведующий кафедрой Оперативной хирургии и клинической анатомии им. С.С. Михайлова ГОУ ОрГМА;
- Фролов Б.А. – д.м.н. профессор, заведующий кафедрой патологической физиологии, проректор по научной работе ОрГМА;
- Нигматуллин Р.Т. – д.м.н., профессор, зам. генерального директора по науке ФГУ «Всероссийский центр глазной и пластической хирургии»
- Курочкин В.Н. – к.м.н., заведующий детским хирургическим отделением Краснодарского филиала ФГУ МНТК «Микрохирургия глаза»
В ходе дискуссии было отмечено, что основу развития высоких технологий в лечении патологий детского возраста составляет клиническая анатомия и патофизиология. В частности, было указано на необходимость дальнейшей разработки вопросов возрастной и вариантной морфологии зрительной системы. Именно поэтому высокую оценку получили доклады, которые базировались на данных экспериментальной и клинической морфологии. Участники также обсудили проблемы медицинского образования и повышения квалификации специалистов, работающих в области детской офтальмологии.
к содержанию | опубликовать статью
Первичная эстетическая реабилитация пациентов после субтотальной резекциии околоушной слюнной железы
Мулдашев Э.Р., Вырупаев С.В., Гайфуллин С.Н., Щербаков Д.А.
ФГУ «Всероссийский центр глазной и пластической хирургии», г.Уфа
Опухолевые поражения околоушной слюнной железы (ОСЖ), как правило, требуют хирургического лечения (Щипский А.В., 2001). При этом целью оперативных вмешательств на ОСЖ является не только резекция опухоли и профилактика Фрей синдрома, но и органосохранность железы, а также стимуляция её репаративного потенциала (Kagami H. et al., 2000).
В настоящее время для профилактики осложнений после резекции ОСЖ предложены различные модификации местно-пластических операций (Anjum K. Et al., 2008), а также применение различных биосинтетических и силиконовых пленок (Aframian D.J., 2000; Афанасьев В.В., 2005). Однако последние не нашли широкого клинического применения, а выполнение местно-пластических операций не всегда возможно ввиду отсутствия материала для формирования лоскута. Известно использование биоматериалов Аллоплант в челюстно-лицевой хирургии (Мулдашев Э.Р., 1976-1993).
По нашим данным выбранные трансплантаты являются аттрактантами мезенхимальных стволовых клеток и стимулируют репаративные процессы в области трансплантации. Целью настоящего исследования явилось клиническое обоснование использования биоматериала для каркасной пластики (БКП) при закрытии дефекта ОСЖ. На первом этапе исследования проведен ретроспективный анализ работы отделения челюстно-лицевой хирургии Республиканского онкологического диспансера (г. Уфа) в период с 2005 по 2009 годы. Отобраны пациенты с доброкачественными опухолями ОСЖ. При этом в контрольную группу вошли лишь пациенты с локализацией опухолевого процесса в наружной части ОСЖ и без прорастания лицевого нерва опухолью. Данной группе больных выполнялся классический разрез кожи по Ковтуновичу, резекция опухоли и ушивание кожных покровов. Второй этап исследования выполнен на базе отделения пластической хирургии и регенеративной стоматологии ФГУ «Всероссийский центр глазной и пластической хирургии» с 2000 по 2009 годы.
В основную группу (n=30) вошли пациенты с доброкачественными опухолями ОСЖ, которым выполнялся разрез, соответствующий таковому при фейслифтинге, резекция опухоли с последующим закрытием дефекта железы биоматериалом для каркасной пластики (БКП) серии Аллоплант (ТУ 42-2-537-2006). Для динамического наблюдения за трансплантатом и состоянием ОСЖ использовался способ МР-сканирования околоушной слюнной железы, разработанный Г.А. Кантюковой с соавт. (2008). Послеоперационные осложнения у пациентов обеих групп разделены на ранние и поздние. К ранним осложнениям мы отнесли отек в области операционной раны, нагноение операционной раны, формирование свища, а также парез лицевого нерва.
В контрольной группе 37% пациентов не имели ранних осложнений, у 37% наблюдалось нагноение операционной раны, у 13% формировался свищ, 10% - сильный отек в области проведенной операции, 3% пациентов имели парез лицевого нерва. Среди поздних послеоперационных осложнений наиболее частым явилось развитие аурикулотемпорального синдрома Люси Фрей, который наблюдался в 72% случаев.
При этом варьировала выраженность данного синдрома среди пациентов, которая, по-видимому, определяется площадью контакта культи ОСЖ с подкожной клетчаткой и кожей.
У пациентов основной группы применение БКП для закрытия дефекта железы не вызывает развитие местного иммунодефицита и не сопровождается герпетической или бактериальной инфекцией.Отдаленные результаты проведенного хирургического лечения показали, что достигнутый косметический эффект полностью скрывает дефицит ткани ОСЖ (Рис. 1), полученный после субтотальной резекции железы.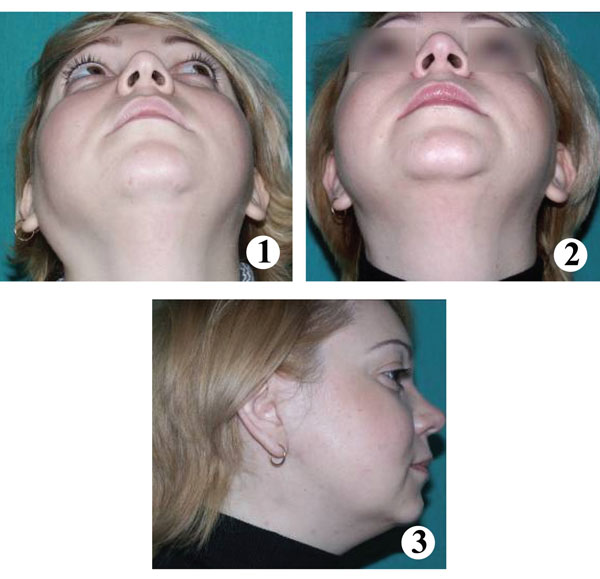
Рис. 1 Внешний вид больной. (1) – до операции, (2), (3) – после операции.
МР-исследование ОСЖ выполненное в отделенные сроки (1 год и 5 лет) после хирургического лечения смешанной опухоли органа подтвердило отсутствие рецидивов заболевания. При этом ткань оперированной железы не подвергалась атрофии после субтотальной резекции, как это отмечено в работах А.Б. Денисова (2003, 2006). Напротив, структура ОСЖ отражала её активное функциональное состояние. БКП также определялся при МР-исследовании в области трансплантации, т.е. не происходило смещения биоматериала в отдаленные сроки. 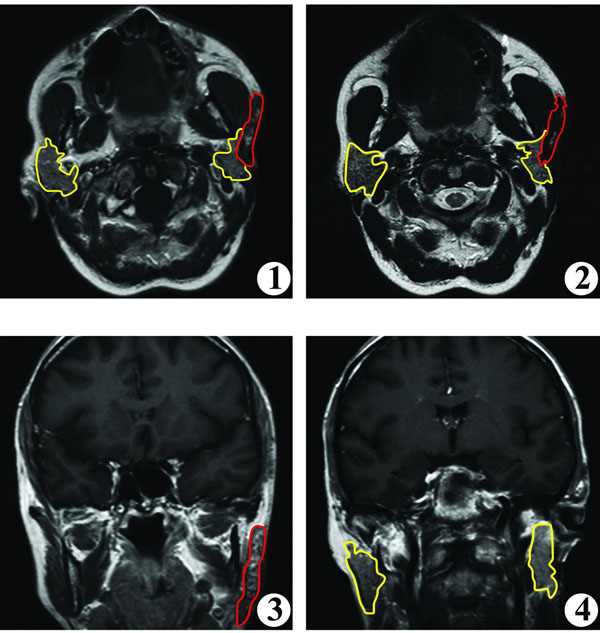
Рис. 2 МРТ околоушной слюнной железы через год после удаления смешанной опухоли и первичной эстетической реабилитации. (1) – аксиальная проекция, режим Т1, (2) – аксиальная проекция, режим Т21, (3) – коронарная проекция, режим Т1, (4) – коронарная проекция, режим Т1. Желтым отмечена ОСЖ,
красным – БКП.
Таким образом, использование БКП позволяет избежать развития Фрей синдрома.
к содержанию | опубликовать статью
АНАТОМОМЕТРИЧЕСКАЯ ХАРАКТЕРИСТИКА ПИЩЕВОДА В ГРУДНОМ ВОЗРАСТЕ
Баландина И.А., Еремченко Н.В.
ГОУ ВПО «Пермская
государственная медицинская академия имени академика Е.А. Вагнера Федерального
агентства по здравоохранению и социальному развитию
Актуальность проблемы. Изучение морфологических особенностей пищевода новорожденных и детей младенческого возраста имеет важное значение не только в связи с его важной функцией, но и большой ролью данного органа в терапевтической и хирургической практике (Ф. Ф. Сакс с соавт, 1984; H. Zhang, 2004; С. В. Бельмер с соавт, 2005; Л. М. Беляева, 2006). У детей первых недель и месяцев жизни встречаются как пороки развития пищевода, так и преходящие нарушения его моторики. Практические наблюдения показывают, что у 38% новорожденных и детей грудного возраста наблюдается синдром срыгивания, который, как правило, прекращается на втором-третьем месяце жизни. Организм ребенка и организм взрослого имеют качественные и количественные различия. Эти различия заключаются в морфологической незрелости организма ребенка первого года жизни, которая является основной причиной недостаточного развития его функций. Правильное решение диагностических и лечебных вопросов невозможно без комплексного изучения строения и особенностей всех структурных элементов пищевода в различные возрастные периоды. В доступной нам литературе мы не встретили работ, посвященных исследованию зависимости макроскопических характеристик пищевода от анатомометрических параметров грудной клетки у детей грудного возраста. До настоящего времени не определены изменения пространственного расположения пищевода у младенцев, детально не изучена возрастная динамика микроскопической анатомии пищевода с момента рождения до конца первого года жизни. Цель исследования. Установить взаимосвязь морфологических и морфометрических характеристик пищевода с параметрами грудной клетки и туловища у детей первого года жизни.
Задачи исследования:
1. Изучить анатомометрические параметры грудной клетки и туловища у детей первого года жизни.
2. Исследовать особенности анатомического развития пищевода и выявить зависимость его макроскопических характеристик от анатомометрических параметров грудной клетки и туловища у детей первого года жизни.
3. Определить топографические изменения пищевода в течение первого года жизни.
4. Изучить возрастную динамику микроскопической анатомии пищевода детей грудного возраста.
5. Провести сравнительный анализ анатомометрических, макроскопических и микроскопических особенностей пищевода в течение грудного возраста и обосновать клиническое значение выявленной закономерности.
Материал и методы исследования. Работа выполнена на кафедре нормальной, топографической и клинической анатомии, оперативной хирургии Государственного образовательного учреждения высшего профессионального образования «Пермская государственная медицинская академия имени академика Е.А. Вагнера Федерального агентства по здравоохранению и социальному развитию». Анатомометрические исследования секционного материала проведены в патоморфологическом отделении Пермская краевая детская клиническая больница. Гистологические, гистохимические, иммуногистохимические, микроморфометрические исследования выполнены в отделе патоморфологических исследований Центральной научно-исследовательской лаборатории ГОУ ВПО «ПГМА им. ак. Е.А. Вагнера Росздрава». Работа основана на анализе результатов исследований трупов 108 детей, поступивших в патоморфологическое отделение Пермской краевой детской клинической больницы в период с 2002 по 2008 год, погибших от заболеваний, не связанных с патологией желудочно-кишечного тракта. Возраст детей составлял от момента рождения до 1 года: 57 мальчиков и 51 девочка.
С целью выявления закономерностей анатомического развития и анатомометрических особенностей пищевода у детей грудного возраста объекты исследования распределяли по следующим возрастным группам: в I группу включили 12 новорожденных, возраст которых составил от момента рождения до 10 суток, во II группу вошли 15 детей в возрасте от 10 суток до 1 месяца, в III группу – 13 детей в возрасте от 1 до 3 месяцев, в IV группу – 14 детей в возрасте от 3 до 6 месяцев, в V группу – 11 детей в возрасте от 6 до 8 месяцев, в VI группу – 13 детей в возрасте от 8 до 10 месяцев, в VII группу – 16 детей в возрасте от 10 до 11 месяцев и VIII группу составили 14 детей в возрасте от 11 до 12 месяцев включительно. Все дети являлись доношенными, со средней массой тела при рождении 3036±0,5 г, оценка по шкале Апгар при рождении соответствовала 4±0,4 балла. Материал распределили по возрастно-росто-весовым группам и анализ морфометрических показателей провели в каждой из групп и между группами при различиях в росте 25 см, так как при этом разница длины пищевода в каждой рассматриваемой группе не превышала допустимых норм развития органа у детей грудного возраста, что не являлось препятствием для проведения математической обработки цифровых данных.
Были проведены следующие методы исследования: антропометрический, включая торакометрию, органометрический пищевода, гистологический, гистохимический, иммуногистохимический, микроморфометрический.
Антропометрическое исследование с выполнением торакометрии провели у всех 108 трупов детей первого года жизни, при этом использовали следующий инструментарий: весы медицинские детские, скользящий циркуль, измерительную ленту, линейку. Измеряли вес трупа ребенка, рост, длину туловища (от яремной вырезки до лонного сочленения). С целью подтверждения объективности произведенной выборки у исследуемых объектов вычисляли росто-весовой показатель (РВП=М×100/Р, М – масса тела; Р – рост) и индекс Пинье (IP=Р-(ОГК+М).; ОГК – окружность грудной клетки). При выполнении торакометрии измеряли окружность грудной клетки (ее горизонтальный периметр) сантиметровой лентой на уровне сосков, подмышечных впадин, мечевидного отростка грудины и XI ребра. Для определения соответствия роста органов грудной полости вычисляли индекс пропорциональности между ростом и окружностью грудной клетки по следующей формуле: ИП =Р×100/ОГК,
Площадь передней грудной стенки определяли по методу Г.Д. Вилявина (1940) с использованием рентгеновских снимков. Сущность метода заключается в том, что на изучаемую поверхность наносится карта, разлинованная на квадраты заданной площади, с помощью которых оценивается площадь изучаемой поверхности.
Макрометрическое исследование пищевода включало изучение топографии пищевода и определение линейных размеров органа и его отделов: исследование длины пищевода, длин его отделов (шейного, грудного, брюшного), полуокружности пищевода на уровнях сужений (фарингеального, бронхиальное, диафрагмального) и расширений (верхнего, нижнего). Определив размер полуокружности, вычисляли диаметр исследуемого органа на уровнях сужений и расширений по формуле: l=2πR, откуда D=2R=l/π, где D – диаметр окружности; R – радиус окружности; l– длина окружности; π=3,14. Высчитывали процентные показатели А.Н. Шкарины (отношение длины пищевода к длине туловища) и М.Н. Умовиста (отношение длины пищевода к длине тела). Для измерений диаметров фарингеального, бронхиального, диафрагмального сужений, верхнего и нижнего расширений был использован измерительный циркуль, линейка и предложенный нами инструмент для измерения диаметра полых органов (патент на полезную модель № 78055 от 20.11.2008). Изучали скелетотопию изгибов пищевода и их проекции относительно срединной линии, скелетотопию сужений пищевода; исследовали синтопию отделов пищевода; исследовали пространственные координаты пищевода в грудной и брюшной полостях; определяли площадь пищевода и его объемные параметры (вес, длина, объем пищевода и его отделов) в проекции на переднюю грудную стенку. Методика получения данных для расчета пространственного расположения пищевода заключалась в измерении расстояния от срединной линии, которая условно проходит по позвоночнику и прилежит к центру тел позвонков, до ближайшего края пищевода (при измерении расстояния во фронтальной плоскости) и до заднего края пищевода (при измерении расстояния в сагиттальной плоскости). Замеры проводили измерительным микрометрическим циркулем, с помощью которого полученное расстояние переносили на измерительную линейку, данные заверяли микрометром. Путем сложения полученных данных о длине и диаметре пищевода с проекционными линиями, проведенными на основании полученных координат, вычисляли пространственное расположение пищевода в грудной полости относительно позвоночника. Для расчета пространственных координат использовали показатели вариационной статистики: М – среднее значение ширины проекции пищевода в той или иной плоскости; m – значение, в пределах которого при измерении допускается ошибка; max – максимальное значение показателя; min – минимальное значение показателя; δ – среднее квадратичное отклонение среднего значения, V – коэффициент вариации.
Материалом для гистологического и гистохимического исследований служили участки передней стенки верхне-грудного отдела пищевода, взятые на уровне II грудного позвонка. Изготавливали серийные поперечные срезы толщиной в 5 микрон. При визуальной оценке изучали не менее 3 срезов у каждого человека. Препараты окрашивали гематоксилином и эозином, по ван Гизону. Для выявления нейтральных мукополисахаридов проводили ШИК-реакцию, с контролем амилазой. Для проведения иммуногистохимического исследования материал фиксировали в 10%-ном забуференномпо Лилли формалине (pH-7,2), гистологические препараты готовили по стандартным методикам с заливкой в гистамикс. Для выявления в исследуемых образцах пищеводов фактора пролиферации Ki-67, десмина и цитокератинов 5 и 14 (ЦКР5, ЦКР14) использовали антитела и полный диагностический набор компании Diagnostic BioSystems (DAB) (США). При проведении иммуногистохимического исследования использовали позитивные контроли. Далее срезы трехкратно промывали в трис-буфере, после чего подвергали экспозиции с вторичными антителами (мышиные и кроличьи биотинилированные антитела) DAB в течение 10 минут. При определении экспрессии Ki-67 ядерная реакция любой интенсивности фиксировалась как позитивная. Оценка интенсивности пероксидазной метки и определение индекса пролиферации Ki-67 проводились полуколичественным методом – учитывалось число позитивных на 100 учтенных ядер (при учете 500–1000 клеток), а также при помощи специализированного программного обеспечения для медицины и биологии BioVision, version 4,0.
Микроморфометрию препаратов поперечных срезов пищеводов выполняли при 50- и 100-кратном увеличении микроскопа с использованием цифровой камеры для микроскопа САМ V200. Результаты обрабатывали при помощи специализированного программного обеспечения BioVision, версия 4,0. Для статистического исследования использовали программы Microsoft Excel «Biostat». Морфометрические исследования слизистой оболочки включали определение толщины эпителиального пласта, собственной и мышечной пластинок. В эпителии подсчитывали число слоев эпителиальных клеток. В мышечной пластинке слизистой оболочки определяли диаметр пучков мышечных волокон. В соединительнотканном компоненте исследовали плотность расположения фибробластов, фиброцитов, агранулоцитов, гранулоцитов и тучных клеток. Подсчёт производили при увеличении ×630 в пределах тест-сетки площадью 25600 мкм2 с последующим перерасчётом на условный 1 мм2 площади соединительной ткани. Измеряли толщину мышечной оболочки, дифференцируя ее составляющие: внутренний слой, прослойка, наружный слой. Изучали толщину адвентициальной оболочки.
Результаты исследований подвергали статистической обработке на персональном компьютере в программе Microsoft Excel-2007. Для оценки силы связи между исследуемыми параметрами определяли коэффициент корреляции. Для характеристики некоторых показателей применяли методику вариационной статистики.
Результаты исследования
У 86 (79,63%) исследуемых трупов детей в возрасте от 0 до 10 месяцев росто-весовой показатель имел нормальные значения от 6 до 15. У 22 (20,37%) детей в возрасте от 10 до 12 месяцев отмечали допустимые увеличения значения росто-весового показателя (от 16 до 17), входящие в диапазон индивидуальных колебаний данного анатомического признака.
Окружность грудной клетки на первом году жизни увеличивалась с 31 до 55 см. При определении средних показателей изменения окружности грудной клетки в течение первого года жизни отметили их равномерное увеличение на протяжении первых 6 месяцев. Далее выявились 2 срока замедления темпов увеличения окружности, которые приходились на возрастной период от 6 до 8 месяцев и период от 10 до 11 месяцев. В результате проведенного исследования нами выделены следующие периоды формирования грудной клетки и туловища: а) период интенсивного увеличения окружности грудной клетки и длины туловища (от 3 до 6 месяцев); б) период замедления темпов увеличения окружности грудной клетки на фоне продолжающего интенсивного роста туловища (от 6 до 8 месяцев); в) период замедления темпов увеличения окружности грудной клетки на фоне умеренного роста туловища (от 10 до 11 месяцев).
При макрометрическом исследовании пищевода у трупов детей грудного возраста его длина составила от 10,5 до 19,1 см. Определялись два периода интенсивного увеличения длины пищевода: от 1 до 3 месяцев жизни (длина пищевода увеличилась в среднем с 10,5 до 13,4 см) и от 6 до 8 месяцев после рождения (длина пищевода увеличилась в среднем с 13,5 до 16,9 см). У 38 (35,19%) детей различных возрастных групп показатель А.Н. Шкарины находился в пределах нормы и выражался отношением 0,54–0,53:1. У 2 (1,85%) новорожденных наблюдалась физиологическая диспропорция грудной клетки, что обусловило увеличение данного показателя в сравнении с нормальными значениями до 0,58–0,57:1. У 9 (8,33%) детей отмечали допустимое увеличение показателя А.Н. Шкарины, который составил 0,58-0,57:1. У 50 (46,30%) детей, в состав которых входили представители всех возрастных групп, кроме новорожденных, имелось допустимое уменьшение показателя А.Н. Шкарины в интервале 0,52–0,51:1. У 9 (8,33%) детей в возрасте старше 11 месяцев данный показатель был ниже нормальных значений и составлял 0,5:1. Мы полагаем, что интенсивность роста пищевода у этих младенцев превышала интенсивность роста туловища. У 13 (12,04%) детей в возрасте от 0 до 3 месяцев показатель М.Н. Умовиста находился в пределах нормальных значений, при этом отношение длины пищевода составляло 19,00 – 19,99% от длины тела. У 8 (7,41%) детей также в возрасте от 0 до 3 месяцев отмечалось допустимое уменьшение значений показателя М.Н. Умовиста, при котором отношение длины пищевода составляло 17,00–18,99% от длины тела. У 81 (75%) исследуемых, относящихся к различным возрастным группам, выявили допустимое увеличение значений показателя М.Н. Умовиста, при котором отношение длины пищевода составляло 20,00–25,99% от длины тела. У 6 (5,56%) детей (возраст 1 (0,93%) принадлежит к возрастному периоду от 10 до 11 месяцев и 5 (4,63%) – к периоду от 11 до 12 месяцев) значения показателя М.Н. Умовиста превышали допустимые границы. При этом отношение длины пищевода составляло 26,00–27,99% от длины тела.
Обращает внимание то, что шейный отдел пищевода у новорожденных в сравнении со всей длиной органа был достаточно протяженным и достигал 2,7±0,06 см при общей длине пищевода, равной 10,6±0,1 см. Наиболее интенсивный рост грудного отдела наблюдался в возрасте от 1 до 8 месяцев (от 8,3±0,1 см до 11,3±0,1 см). В течение первого месяца жизни брюшной отдел пищевода не визуализировался. Далее длина данного отдела также равномерно увеличивалась с возрастом до 10 месяцев. После 10-и месяцев этот показатель оставался стабильным и составлял 0,6±0,05. Среднюю величину диаметра пищевода вычисляли путем сложения следующих значений: диаметров 3 сужений и 2 расширений. Получив средний показатель величины диаметра пищевода, выделили два периода интенсивного увеличения данного показателя. Первый период приходился на временной промежуток от 3 до 6 месяцев, второй период – от 10 до 11 месяцев жизни. В периоде новорожденности у ребенка наблюдали наличие только диафрагмального сужения (диаметром 4,0±0,05 мм). В возрастном периоде от 10 суток до 1 месяца наблюдалось формирование бронхиального сужения (диаметр 4,5±0,07 мм). В периоде от 1 до 3 месяцев были сформированы все сужения. Самыми узкими были диафрагмальное (диаметр 5,2±0,03 мм) и бронхиальное (диаметр 5,2±0,08 мм) сужения, самым широким – фарингеальное (диаметр 6,1±0,07 мм). К концу грудного возраста самым узким оставалось диафрагмальное сужение, диаметр которого составлял 8,5±0,07 мм против средней величины диаметра пищевода, равной 13,2±0,09 мм. Самым широким было фарингеальное сужение (диаметр 10,0±0,04 мм). В возрасте от 0 до 10 суток диаметры верхнего и нижнего расширений были одинаковыми. При исследовании изменений диаметра верхнего расширения отмечали тенденцию к его постоянному увеличению в течение всего первого года жизни, исключение составил период от 8 до 11 месяцев, когда диаметр верхнего расширения возрос с 12,0±0,03 мм до 12,8±0,07 мм. Нижнее расширение наиболее интенсивно увеличивалось в возрастном периоде от 1 до 6 месяцев, когда диаметр его возрос с 9,5±0,02 мм до 11,5±0,04 мм.
Нами было выявлено, что на протяжении первого года жизни наиболее интенсивный прирост анатомометрических параметров пищевода приходится на возрастные периоды от 1 до 3 и от 6 до 8 месяцев.
Скелетотопически начало пищевода проецировалось на диск между III и IV шейными позвонками, а конец – на XI грудной позвонок. Шейный его отдел заканчивался на уровне нижнего края VII шейного позвонка. Граница между верхним и средним грудными отделами располагалась между III и IV позвонками, граница между средним и нижним грудными отделами проецировалась между VI и VII позвонками, а граница между грудным и брюшным отделами скелетотопически была на уровне между IX и X позвонками. В начале шейного отдела пищевод, как правило, располагался симметрично позвоночному столбу. Первый левый фронтальный изгиб в течение всего первого года жизни определялся на уровне VII шейного позвонка. Максимальная амплитуда отклонений измерялась от срединной линии до левого края пищевода. В возрастном периоде от 1 до 3 месяцев с момента рождения наблюдалось отклонение пищевода влево от срединной линии на 2,5±0,015 мм, а к концу грудного возраста оно достигало 4,0±0,01 мм. Правый фронтальный изгиб в течение первого года жизни имел минимальную амплитуду отклонений, которая была нами зафиксирована на уровне межпозвонкового диска III и IV грудных позвонков. В первые три месяца жизни пищевод отклонялся относительно срединной линии вправо на 3,0±0,015 мм, к концу первого года жизни – на 4,5±0,022 мм. Второй левый фронтальный изгиб в течение первого года жизни имел максимальные отклонения амплитуды от срединной линии (в сравнении с другими изгибами), которые зафиксированы на уровне X грудного позвонка. С периода новорожденности до двенадцатимесячного возраста отклонение влево менялось с 1,5±0,026 мм до 8,0±0,026 мм соответственно.
Сагиттальные изгибы пищевода в течение первых трех месяцев жизни визуально практически не выявлялись. Мы полагаем, что это связано с отсутствием шейного лордоза и практически не сформировавшегося грудного кифоза позвоночника. В периоде от 3 до 6 месяцев отклонение верхнего сагиттального изгиба, которое было зафиксировано на уровне IV грудного позвонка, относительно срединной линии составляло 1,5±0,026 мм; в возрасте от 11 до 12 месяцев данное отклонение уже составляло 5,0±0,022 мм. В периоде от 3 до 6 месяцев отклонение проекции среднего сагиттального изгиба, которое было зафиксировано на уровне VII грудного позвонка относительно срединной линии, составляло 2,5±0,019 мм, а концу грудного возраста данное отклонение составляло 7,0±0,026 мм. В периоде от 3 до 6 месяцев отклонение проекции нижнего сагиттального изгиба, которое было зафиксировано на уровне VII грудного позвонка, относительно срединной линии составляло 3,0±0,026 мм; к завершению первого года жизни данное отклонение достигало 8,0±0,022 мм.
Начало формирования фарингеального сужения пришлось на возрастной период от 1 до 3 месяцев. В этом возрасте оно располагалось на уровне VII шейного позвонка. В последующих возрастных периодах оно становилось более выраженным и проецировалось в периоде от 3 до 6 месяцев на уровне VI шейного позвонка; в периоде от 6 до 8 месяцев – V шейного позвонка; в периоде от 8 до 10 месяцев – между V и IV шейными позвонками; в периоде от 10 до 12 месяцев – на уровне IV шейного позвонка. Начало формирования бронхиального сужения пришлось на возрастной период от 10 суток до 1 месяца. До 6 месяцев включительно бронхиальное сужение проецировалось на уровень IV грудного позвонка. В периоде от 6 до 11 месяцев данное сужение располагалось между IV и V грудными позвонками. В возрастном периоде от 11 до 12 месяцев бронхиальное сужение проецировалось на уровне V грудного позвонка. Диафрагмальное сужение пищевода в течение первого месяца жизни проецировалось на уровне IX грудного позвонка. В возрасте от 1 до 8 месяцев данное сужение располагалось между IX и X грудными позвонками, а в возрасте от 8 до 12 месяцев – на уровне X грудного позвонка. С целью определения изменения пространственного расположения пищевода в течение первого года жизни исследовали расположение пищевода в грудной и брюшной полостях в трех взаимно-перпендикулярных плоскостях. Ось X проходит через основание X грудного позвонка; ось Y – это срединная линия грудной клетки, которая проходит по центру тел позвонков; ось Z – линия, проведенная перпендикулярно осям Х и Y в месте их пересечения. В шейном отделе выбрана одна контрольная точка фарингеальное сужение на уровне IV шейного позвонка. Ее координаты соответствуют расположению пищевода позади трахеи без отклонения от срединной линии. В грудном отделе было выбраны четыре контрольные точеки, которые соответствуют максимальным отклонениям пищевода от срединной линии в зависимости от его синтопии и скелетотопии. Так, например, точка верхнее расширение на уровне VII шейного позвонка отклонена влево на 0,2±0,002 см и на 0,2±0,007 см вперед в зависимости от синтопии с дугой аорты и бифуркацией трахеи, а также скелетотопически в соотношении с кифозом грудного отдела позвоночника. Точка бронхиальное сужение на уровне IV грудного позвонка отклоняется в левую сторону и еще больше кпереди: вправо на 0,25±0,004 см, а кпереди – на 0,4±0,007 см. Следующей точкой является нижнее расширение на уровне VIII грудного позвонка, имеет отклонение влево на 0,2±0,004 см и кпереди на 0,6±0,01 см в зависимости от синтопии с сердечной сумкой, а скелетотопически связана с переходом кифоза в лордоз. Точка диафрагмальное сужение на уровне X грудного позвонка имеет большее значение отклонений от осей в грудном отделе пищевода: влево отклоняется на 0,5±0,005 см, кпереди имеет наибольшее значение отклонений на протяжении всего пищевода 0,8±0,015 см. В брюшном отделе имеется одна контрольная точка кардиальное отверстие на уровне XI грудного позвонка. Она имеет отклонение влево на 0,6±0,005 см и кпереди – на 0,7±0,01 см. Средние показатели пространственных координат пищевода относительно трех плоскостей в грудной и брюшной полостях на первом году жизни приводятся в таблице 1.
Таблица 1
СРЕДНИЕ ПОКАЗАТЕЛИ ПРОСТРАНСТВЕННЫХ КООРДИНАТ ПИЩЕВОДА В ГРУДНОЙ И БРЮШНОЙ ПОЛОСТЯХ НА ПЕРВОМ ГОДУ ЖИЗНИ, см (n=108)
| Контрольные точки пищевода с проекцией на позвоночник | Оси |
М±m |
Max |
Min |
σ |
V |
| Фарингеальное сужение на уровне CIV | X |
0 |
0 |
0 |
0 |
0 |
Y |
13,5±0,188 |
15,3 |
11,4 |
1,95 |
0,2830 |
|
Z |
-0,2±0,007 |
-0,1 |
-0,2 |
0,07 |
0,0250 |
|
| Верхнее расширение на уровне CVII | X |
0,2±0,007 |
0,2 |
0,1 |
0,07 |
0,0250 |
Y |
10,4±0,183 |
12,4 |
8,6 |
1,90 |
0,3481 |
|
Z |
-0,2±0,007 |
-0,1 |
-0,2 |
0,07 |
0,0250 |
|
| Бронхиальное сужение на уровне TV | X |
-0,25±0,004 |
-0,22 |
-0,30 |
0,04 |
0,0068 |
Y |
6,3±0,121 |
7,7 |
5,2 |
1,26 |
0,2508 |
|
Z |
-0,4±0,007 |
-0,3 |
-0,4 |
0,07 |
0,0125 |
|
| Нижнее расширение на уровне TVIII | X |
0,2±0,004 |
0,25 |
0,18 |
0,04 |
0,0070 |
Y |
4,2±0,089 |
5,3 |
3,5 |
0,92 |
0,2024 |
|
Z |
-0,6±0,01 |
-0,5 |
-0,7 |
0,10 |
0,0167 |
|
| Диафрагмальное сужение на уровне TX | X |
0,5±0,005 |
0,56 |
0,45 |
0,05 |
0,0060 |
Y |
0 |
0 |
0 |
0 |
0 |
|
Z |
-0,8±0,015 |
-0,6 |
-0,9 |
0,16 |
0,0313 |
|
| Кардиальное отверстие на уровне TXI | X |
0,6±0,005 |
0,67 |
0,56 |
0,05 |
0,0043 |
Y |
-3,6±0,074 |
0,0 |
-2,5 |
0,77 |
0,1667 |
|
Z |
-0,7±0,01 |
-0,6 |
-0,8 |
0,10 |
0,0143 |
Достоверность различий p < 0,005. Отрицательное значение некоторых точек связано с тем, что они распложены в отрицательных плоскостях системы координат. Была определена площадь передней грудной стенки (ПГС) по методу Г.Д. Вилявина (1940), которая составила в среднем 213,0±0,28 см2. В таблице 2 представлены площадь пищевода, а также площади шейного, грудного и брюшного его отделов и их процентное соотношение к площади пищевода.
Таблица 2
СРЕДНИЕ ПОКАЗАТЕЛИ ПЛОЩАДИ ПИЩЕВОДА В ПРОЕКЦИИ НА ПЕРЕДНЮЮ ГРУДНУЮ СТЕНКУ НА ПЕРВОМ ГОДУ ЖИЗНИ (n=108)
Площадь отделов пищевода |
М±m |
Max |
Min |
σ |
V |
|
Общая |
см² |
9±0,009 |
16 |
3,1 |
0,089 |
0,0009 |
S ПГС |
213±0,28 |
285 |
139 |
2,9 |
0,0395 |
|
% от S ПГС |
2±0,0004 |
6 |
1 |
0,005 |
0,000013 |
|
Шейный отдел |
см² |
2±0,006 |
4 |
0,7 |
0,059 |
0,0017 |
% от S пищевода |
23±0,003 |
25 |
22,5 |
0,036 |
0,0001 |
|
Грудной отдел |
см² |
6±0,008 |
10 |
2,4 |
0,087 |
0,0013 |
% от S пищевода |
67±0,0009 |
62,5 |
77,5 |
0,009 |
0,000001 |
|
Брюшной отдел |
см² |
1±0,006 |
2 |
0 |
0,1 |
0,0049 |
% от S пищевода |
7±0,004 |
12,5 |
0 |
0,038 |
0,0001 |
|
Достоверность различий p < 0,005.
Вес пищевода в среднем составил 0,341±0,01 кг, а процентное соотношение его массы к массе тела было равно 0,59±0,01%. Длина пищевода в среднем была равна 26±0,35 см, а процентное соотношение его длины к общей длине тела составило 16±0,01%. Объем пищевода в среднем составил 0,007±10×10-8 литров, а его процентное соотношение к объему грудной клетки достигало 0,52±0,00005%. Объем шейного отдела в среднем составил 0,0018±3×10-7 литра, объем грудного отдела – 0,005±2×10-7 литра, объем брюшного отдела в среднем был равен 0,0009±4×10-8 литров.
При микроморфометрическом исследовании стенки пищевода в I возрастной группе (0–10 суток) выявили, что общая толщина стенки пищевода новорожденного составила 497,77±5,2 мкм. В слизистой оболочке визуализировались три пластинки: эпителиальная, собственная и мышечная. По толщине среди всех пластинок превалировала мышечная. Адвентициальная оболочка была представлена отдельными рыхло расположенными коллагеновыми волокнами и содержала сосуды. Во II возрастной группе (от 10 суток до 1 месяца) выявили, что общая толщина стенки пищевода составляла 547,08±5,6 мкм. Увеличение общей толщины стенки пищевода в основном было обусловлено развитием мышечной оболочки, общая толщина которой увеличилась в большей степени за счет внутреннего слоя. В III возрастной группе (от 1 до 3 месяцев) обнаружили, что интенсивно увеличилась толщина всех оболочек, кроме адвентициальной. Именно в эти сроки наблюдался первый интенсивный скачок увеличения толщины стенки пищевода.
При проведении иммуногистохимического исследования экспрессия ЦКР5 и ЦКР14 в эпителии пищевода у детей в возрасте от 1 до 3 месяцев выявлялась во всех слоях многослойного плоского эпителия, исключая отдельные поверхностные клетки. Выраженная экспрессия ЦКР5 и ЦКР14 отмечалась также в клетках, образующих выводные протоки собственных желез пищевода. В концевых отделах желез экспрессия цитокератинов выявлялась в ограниченном количестве эпителиальных клеток.
При гистологическом исследовании стенки пищевода в IV возрастной группе (от 3 до 6 месяцев) определили, что увеличение толщины стенки продолжалось и она составила 1091,22±5,5 мкм. Период характеризовался достаточно равномерным увеличением абсолютно всех оболочек и их слоев. Начиная с трехмесячного возраста в препаратах выявлялась неравномерная экспрессия цитокератинов в эпителиальных клетках: более выраженная экспрессия отмечалась, в основном, в клетках базального и шиповатого слоев. При этом клетки эпителия были более густо заполнены гранулами коричневого цвета в базальном и нижних рядах шиповатого слоя. В вышележащих слоях, в цитоплазме клеток эпителия количество гранул постепенно уменьшалось, и клетки выглядели более бледными. В клетках, образующих выводные протоки собственных желез пищевода, отмечалась выраженная экспрессия ЦКР5 и ЦКР14.
При определении экспрессии антигена Ki-67 установлено, что индекс пролиферации у детей первого полугодия жизни составил – 1,6±1,14%. Для IV возрастной группы характерно значительное увеличение толщины адвентициальной оболочки. В V возрастной группе (от 6 до 8 месяцев) общая толщина стенки пищевода увеличилась в среднем до 1488,89±5,8 мкм. Наиболее прогрессивно увеличилась толщина подслизистой основы, в сравнении с другими слоями, в среднем на 130±3,7 мкм. Индекс пролиферации составил 0,6±0,54%. Особенность развития мышечной оболочки заключалась в более интенсивном утолщении прослойки. Увеличился диаметр отдельных мышечных волокон. Толщина стенки пищевода в VI возрастной группе (от 8 до 10 месяцев) была равна 1898,91±4,9 мкм. Наблюдалось увеличение толщины всех оболочек, за исключением адвентициальной, толщина которой и в этом возрастном периоде не изменилась. Из всех слоев слизистой оболочки в этот период наиболее интенсивно увеличивалась собственная пластинка слизистой. В мышечной оболочке заметно увеличивалась толщина внутреннего слоя мышечных волокон. В VII возрастной группе (от 10 до 11 месяцев) выявили, что общая толщина стенки пищевода составляла 2358,78±5,6 мкм.
В данной возрастной группе отмечалось самое интенсивное увеличение толщины слизистой оболочки пищевода. Это, очевидно, объясняется высоким темпом увеличения размеров каждой пластинки. Увеличение толщины мышечной оболочки в данном периоде происходило преимущественно за счет ее внутреннего слоя. Было отмечено увеличение размеров адвентициальной оболочки. Общая толщина стенки пищевода у младенцев VIII возрастной группы (от 11 до 12 месяцев) достигала 3143,27±5,8 мкм. Толщина слизистой оболочки продолжала увеличиваться, а величина подслизистой основы практически не изменилась. В сравнении со всеми оболочками значительно изменилась в размерах мышечная оболочка, в среднем ее толщина увеличилась на 600±4,8 мкм. Изменения толщины стенки пищевода и толщины мышечной оболочки и ее слоев в течение первого года жизни отражены на рисунках 1 и 2.
Рис. 1. Изменения толщины стенки пищевода и ее оболочек в течение первого года жизни, мкм (n=108) 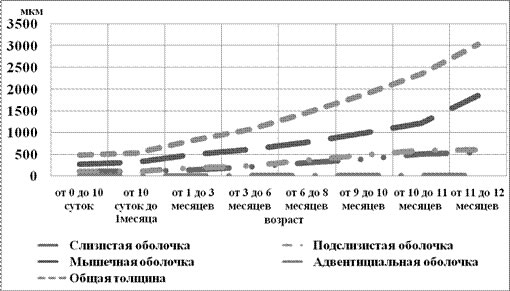
На основании проведенных исследований разработаны нормативные таблицы анатомометрических показателей для различных возрастных периодов первого года жизни.
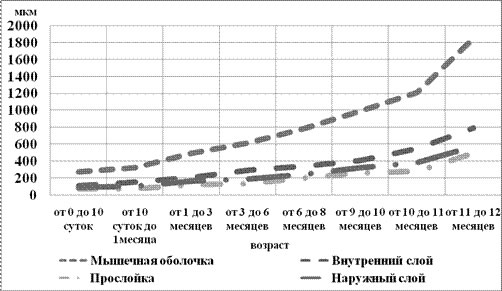
Рис. 2. Изменения толщины мышечной оболочки пищевода и ее слоев в течение первого года
жизни, мкм (n=108)
Таким образом, полученные данные позволяют повысить точность диагностики и оценку патологических изменений в пищеводе для выполнения оптимальных хирургических доступов и оперативных приемов.
ВЫВОДЫ
- Анатомометрические особенности развития грудной клетки и туловища у детей первого года жизни характеризуются следующими периодами: а) период интенсивного роста (от 3 до 6 месяцев), проявляющийся наиболее выраженным увеличением окружности грудной клетки и длины туловища; б) период замедления темпов увеличения окружности на фоне продолжающегося интенсивного роста туловища (от 6 до 8 месяцев); в) период замедления темпов увеличения окружности на фоне умеренного роста туловища (от 10 до 11 месяцев).
- Возрастные особенности макроскопической анатомии пищевода на первом году жизни заключаются в различии длины органа (которая увеличивается с 10,6±0,1 до 19,0±0,1 см) и его отделов, а также вариабельности наружных диаметров и уровней расположения сужений и расширений. Прирост анатомометрических параметров пищевода находится в прямой зависимости от развития грудной клетки и туловища.
- Диафрагмальное сужение (диаметром 4,0±0,05 мм) определяется в периоде новорожденности. Начало формирования бронхиального сужения (диаметром 4,5±0,07 мм) приходится на возрастной период от 10 суток до 1 месяца, фарингеального сужения (диаметром 6,1±0,07 мм) – на период от 1 до 3 месяцев.
- Расширения пищевода выявляются в течение всего первого года жизни: наружный диаметр верхнего расширения возрастает с 7,0±0,07 до 14,0±0,08 мм, нижнего – с 7,0±0,04 до 15,0±0,04 мм.
- Для пищевода и его структурных компонентов характерны топографические изменения, зависящие от возраста ребенка, что является объективным диагностическим критерием оценки его нормального развития.
- Возрастная динамика микроскопической анатомии пищевода детей грудного возраста выражается различиями в строении и величине его оболочек, вариабельностью качественного и количественного состава его структурных компонентов. Толщина стенки пищевода в течение первого года жизни увеличивается с 497,77±5,2 до 3143,27±5,8 мкм.
- В возрасте до шести месяцев жизни выраженная экспрессия цитокератинов 5 и 14 отмечается во всех слоях эпителия пищевода; индекс пролиферации эпителия достигает 1,6±1,14%. В возрасте старше шести месяцев экспрессия цитокератинов 5 и 14 выявляется в базальном и шиповатом слоях эпителия; индекс пролиферации достигает 0,6±0,54%.
- Полученные данные о возрастной анатомии пищевода на первом году жизни позволяют повысить точность диагностики и оценку патологических изменений в пищеводе для выполнения оптимальных хирургических доступов и оперативных приемов.
Практические рекомендации
- При диагностическом инструментальном исследовании пищевода на первом году жизни следует ориентироваться на установленные для каждой возрастной группы анатомометрические параметры грудной клетки.
- Выявленное соответствие (или несоответствие) анатомометрических характеристик пищевода в грудном возрасте необходимо отмечать в протоколе исследования, что является важным для оценки нормального развития данного органа, а также при следующих патологических состояниях пищевода у детей: атрезии, трахео-пищеводный свищ, последствия химического ожога пищевода и некоторые другие.
- Разработанная трехмерная координатная система позволяет выявить особенности пространственного расположения пищевода в грудной и брюшной полостях, установить взаимосвязь этих параметров с возрастом ребенка и использовать как объективный диагностический критерий оценки его нормального развития.
- Установленные анатомометрические параметры пищевода могут являться основой к составлению нормативных таблиц для различных возрастных периодов первого года жизни.
- При планировании оперативных вмешательств на пищеводе в грудном возрасте следует учитывать возрастные особенности его синтопического и скелетотопического расположения, нюансы проекции тех или иных анатомических образований пищевода на кожные покровы и с учетом этих возможностей индивидуализировать хирургические доступы.
- При секционном исследовании пищевода на первом году жизни необходимо учитывать особенности его макроскопической анатомии пищевода, характерные для каждой возрастной группы.
Литература
- Возрастная динамика анатомометрических показателей пищевода у детей младенческого возраста / Н.В. Еремченко // Пермский медицинский журнал. – Пермь, 2009. – С. 117–121.
- Строение мышечной оболочки пищевода младенцев/ И.А. Баландина, Ф.З. Сапегина, Н.В. Еремченко // Материалы научной конференции студентов и молодых ученых, посвященной памяти профессора В.К. Сологуба. – Красноярск, 2008. – С. 46–48.
- Морфометрические данные пищевода детей грудного возраста / И.А. Баландина, Ф.З. Сапегина, Н.В. Еремченко // Материалы Международной дистанционной научно-практической конференции посвященной памяти профессора В.Н. Парина «Внедрение инновационных технологий в хирургическую практику (фундаментальные и прикладные аспекты)». – Пермь, 2008. – С. 23–25.
- Морфологические особенности пищевода детей раннего возраста / И.А. Баландина, Ф.З. Сапегина, Н.В. Еремченко // Материалы Международной научно-практической конференции «Актуальные вопросы морфологии». – Гродно, 2008. – С. 15–16.
- Морфометрическая характеристика пищевода детей грудного возраста / И.А. Баландина, Н.В. Еремченко, Ф.З. Сапегина // Материалы научно-практической конференции «Актуальные вопросы современной хирургии», посвященной 60-летию со дня рождения профессора Ю.С. Винника. – Красноярск, 2008. – С 37–38.
- Особенности строения стенки пищевода у детей раннего возраста / Н.В. Еремченко, В.П. Хоринко // Материалы научной сессии ПГМА им. ак. Е.А. Вагнера Росздрава – Пермь, 2008. С. 124–126.
- Влияние экологии города на морфологию слизистой оболочки и подслизистой основы пищевода у детей грудного возраста / А.Д. Пастухов, И.А. Баландина, Н.В. Еремченко // Материалы XVI Всероссийской научно-практической конференции студентов, аспирантов, молодых ученых «Экология – проблемы и пути решения». – Пермь, 2008 – С. 173–175.
- Гистотопографические особенности пищевода детей раннего возраста / И.А. Баландина, П.В. Косарева, Н.В. Еремченко, Ф.З. Сапегина, В.П. Хоринко // Материалы научно-практической конференции, посвященной 175-летию Пермской краевой клинической больницы. – Пермь, 2008. – С. 58–61.
- Анатомометрическая характеристика пищеводов детей младенческого возраста / И.А. Баландина, Ф.З. Сапегина, Н.В. Еремченко, И.И. Мельников, В.П. Хоринко // Материалы научной сессии ПГМА им. ак. Е.А. Вагнера. – Пермь, 2009. – С. 80–81.
- Анатомометрические особенности пищевода у людей зрелого возраста с различными типами конституции / И.А. Баландина, Ф.З. Сапегина, Н.В. Еремченко. Ф.А. Шилова, П.В. Косарева // Материалы научной сессии ПГМА им. ак. Е.А. Вагнера. Пермь, 2009. – С. 62.
- Морфология нервных сплетений пищевода у детей младенческого возраста / В.П. Хоринко, Н. В. Еремченко, Д. С. Фадеев // Материалы 73-й итоговой студенческой научно-практической конференции с международным участием им. профессора В.Ф. Войно-Ясенецкого, посвящённой 100-летию со дня рождения академика Л.В. Киренского. – Красноярск, 2009. – С. 667–668.
- Интрамуральные нервные ганглии в стенке пищевода у детей младенческого возраста / Н.В. Еремченко, В.П. Хоринко, Д.С. Фадеев // Материалы Международной дистанционной научно-практической конференции, посвященной памяти основателя Уральской научной школы анатомов, гистологов и эмбриологов профессора В.К. Шмидта. – Пермь, 2009. – С. 35–37.
- Строение мышечной оболочки пищевода в грудном возрасте / И.А. Баландина, Н.В. Еремченко, Ф.З. Сапегина // Материалы Международной дистанционной научно-практической конференции, посвященной памяти основателя Уральской научной школы анатомов, гистологов и эмбриологов профессора В.К. Шмидта. – Пермь, 2009. – С. 22–24.
- Микроанатомия мышечной оболочки пищевода младенцев / И.А. Баланидна, Н.В. Еремченко, Ф.З. Сапегина, И.И. Мельников // Клинические и морфологические аспекты хирургических болезней детского возраста: материалы международной научно-практической конференции. – Пермь: изд. Богатырев П.Г., 2009. – С. 3–5.
- Анатомометрические особенности микроциркуляторного русла пищевода в постнатальном онтогенезе / И.А. Баландина, И.И. Мельников, Н.В. Еремченко Н.В., Ф.З. Сапегина // Клинические и морфологические аспекты хирургических болезней детского возраста: материалы международной научно-практической конференции. – Пермь: изд. Богатырев П.Г., 2009. – С. 8–13.
к содержанию | опубликовать статью
КЛИНИЧЕСКИЙ СЛУЧАЙ ПРИМЕНЕНИЯ БИОМАТЕРИАЛОВ СЕРИИ АЛЛОПЛАНТ ПРИ ЛЕЧЕНИИ ПРОБОДНОЙ ЯЗВЫ РОГОВИЦЫ
А. Г. Ямлиханов
Офтальмологическое отделение ГКБ №10, г. Уфа
Пациент Н., 30 лет, поступает в экстренном порядке в офтальмологическое отделение ГКБ №10 10.10.08г. Диагноз при поступлении ОД – Прободная язва роговицы. Из анамнеза: с 08.09.08г. по 08.10.08г. находился на стационарном лечении отделении челюстно-лицевой хирургии ГКБ №21 с диагнозом: Одонтогенный сепсис, правосторонний тромбоз кавернозного синуса, острый гнойный правосторонний гайморит. Флегмона орбиты справа. Проводилось следующее лечение: гайморотомия(10.09.08), вскрытие флегмоны орбиты (11.09.08), интенсивная антибиотикотерапия, противовоспалительное лечение. При первичном осмотре правого глаза: веки отечные, гиперемированы. Глазная щель закрыта, самостоятельно не открывается. Конъюнктива резко отечная и гиперемированная. Роговица в нижнем секторе до центральной оптической зоны практически полностью расплавлена(см. рис. №1).
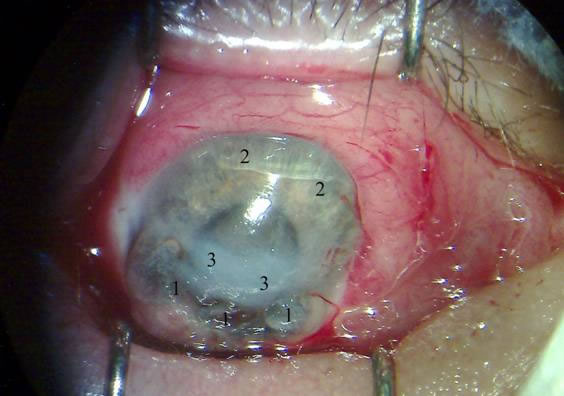
Рис. 1. Прободная язва роговицы. 1 – кератомаляция роговицы, 2 – интактная роговица,
3 – демаркационная зона
В образовавшийся дефект вставлена и ущемлена радужка, за счет чего сохраняется передняя камера в верхнем секторе. Глазное яблоко гипотонично. Движения глазного яблока сохранены в небольшом объеме. В нижнем отделе образовался симблефарон (обнаружился по ходу операции). В сложившейся ситуации было принято решение произвести кератопластику с применением роговичного трансплантата серии Аллоплант Ø 9мм. Операция проводилась под местной анестезией (субтеноновая – 2,0 мл 1% р-ра лидокаина). Также с целью седатации и обезболивания внутривенно вводили трамадол и реланиум. Роговичный трансплантат был смоделирован по форме раны. Учитывая резкий отек тканей, малоподвижность глазного яблока, ограниченность операционного поля удалось подшить трансплантат к склере по лимбу семью узловыми швами №8 (викрил). К роговице трансплантат был подшит непрерывным швом по Пирсу нить №10. также в ходе операции был иссечен симблефарон. На этом операция была завершена. Под конъюнктиву введены гентамицин с дексаметазоном. Назначена общая антибиотикотерапия. При осмотре 14.10.08: роговица в верхнем секторе прозрачная; трансплантат на месте, швы состоятельны. На границе с трансплантатом имеется небольшой перифокальный отек роговицы. В результате иссечения симблефарона и рубцового сокращения конъюнктивы образовался конъюнктивальный дефект в нижнем правом секторе(см. рис. № 2).
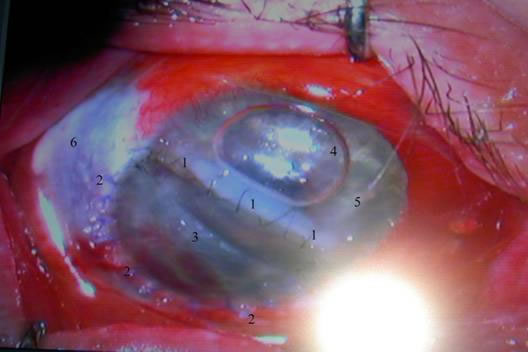
Рис. 2. Состояние после трансплантации (4-ый день). 1 – роговичный шов, 2 – склеральный швы, 3 – роговичный трансплантат, 4 – пузырек воздуха в передней камере, 5 – интактная роговица, 6 – участок обнаженной склеры.
Было принято решение заменить дефект биоматериалом для пластики конъюнктивы серии Аллоплант. Операция проводилась 16.10.08 под местной анестезией. Был выкроен аллотрансплантат по форме дефекта и пошит по периферии к конъюнктиве и по лимбу к склере. В связи с уменьшением отека и увеличением операционного доступа были наложены дополнительные швы на трансплантат по лимбу швами №8(викрил). Также был выкроен конъюнктивальный трансплантат в виде ленты, который был подшит к конъюнктиве и трансплантату, тем самым прикрыв зону лимба на 15:00 – 18:00 часах (см. рис. №№ 3,4).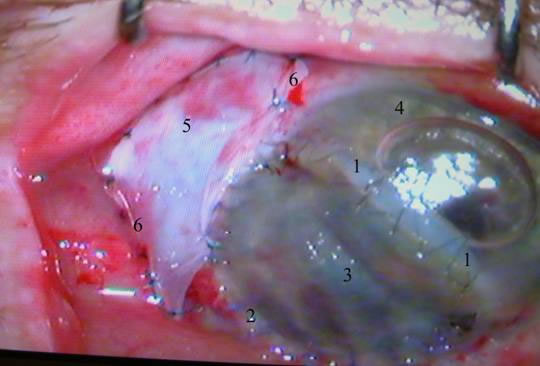
Через несколько дней швы от конъюнктивы начали отходить и конъюнктивальные трансплантаты постепенно отпали. Роговичный трансплантат находился на месте, швы состоятельны. 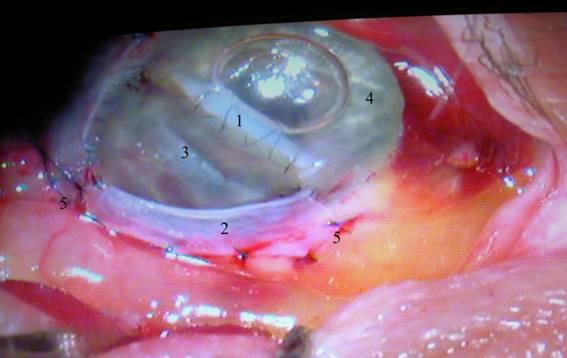
24.10.08 пациент с улучшением был выписан на амбулаторное долечивание. 27.10.08 пациент подошел на контроль. При осмотре было выявлено отхождение трансплантата от склеры на 20:00. В образовавшийся дефект вставилась радужка(см рис. № 5).
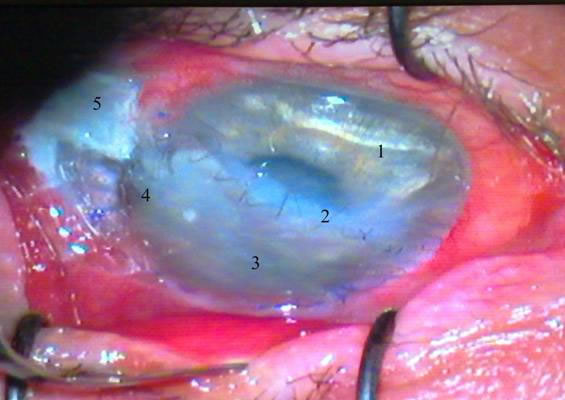 Рис. 5. Состояние после трансплантации (17-ый день). 1 – интактная роговица, 2 – роговичный шов, 3 – роговичный трансплантат, 4 –участок радужки в ране, 5 – конънктивальный трансплантат.
Рис. 5. Состояние после трансплантации (17-ый день). 1 – интактная роговица, 2 – роговичный шов, 3 – роговичный трансплантат, 4 –участок радужки в ране, 5 – конънктивальный трансплантат.
Больной был направлен на консультацию в ВЦГПХ. Было рекомендовано попробовать произвести аппликации диспергированным биоматериалом Аллоплант (ДБА) на проблемные участки(см. рис. № 6, 7). 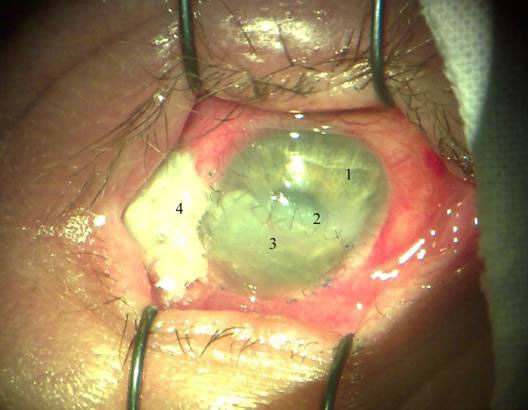
Рис. 6. Состояние после трансплантации (19-ый день). 1 – интактная роговица, 2 – роговичный шов, 3 – роговичный трансплантат, 4 –аппликации диспергированного биоматериала.
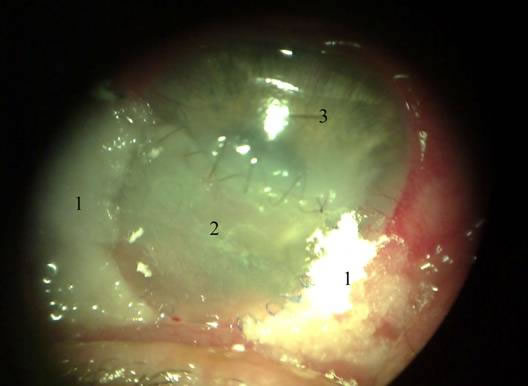
Рис. 7. Состояние после трансплантации (20-ый день). 1 – аппликации диспергированного биоматериала, 2 – роговичный трансплантат, 3 – интактная роговица.
29 и 30 октября были произведены данные аппликации в амбулаторных условиях. При контроле 5.11.08 положительный эффект не был достигнут и было принято решение о пластике дефекта с помощью других материалов серии «Аллоплант(см. рис. № 8).
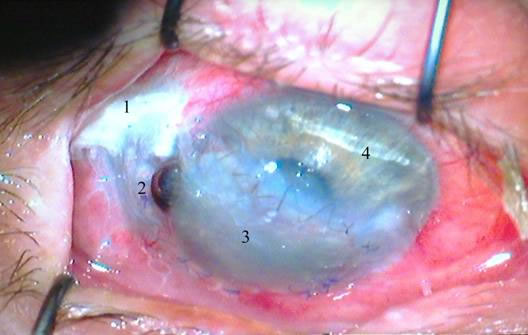
Рис. 8. Состояние после трансплантации (25-ый день). 1 – коньюнктивальный трансплантат, 2 – участок радужки в ране, 3 – роговичный трансплантат, 4 –интактная роговица.
В данной ситуации наиболее подходящим материалом мы сочли аллотрансплантат для склеропластики по Пивоварову, также произведенной в лаборатории ВЦГПХ. 6.11.08 после стандартной обработки операционного поля и анестезии выкроили трансплантат необходимой формы. Трансплантат был подшит в своей центральной зоне двумя узловыми швами к склере. Затем были наложены четыре узловых шва между роговичным и склеральным трансплантатами, что позволило закрыть дефект (см. рис. № 9).
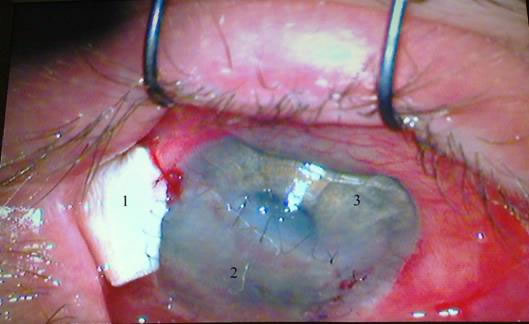
Рис. 9. Состояние после трансплантации (26-ый день). 1 – склеральный трансплантат, 2 – роговичный трансплантат, 3 – интактная роговица.
С верхней части был выкроен лоскут конъюнктивы на ножке. В нижней части удалось немного отсепаровать и подтянуть к верху рубцово-измененную конъюнктиву. Эти два лоскута были подтянуты навстречу друг другу, тем самым прикрыв склеральный трансплантат, и подшиты друг к другу узловыми швами. В верхнем секторе было произведено возмещение дефекта конъюнктивы с помощью аллотрансплантата для пластики(см. рис. № 10).
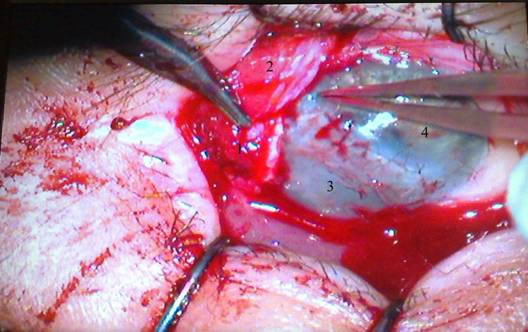
Рис. 10. Состояние после трансплантации (26-ый день). 1 – нижний коньюнкти-вальный лоскут, 2 – верхний коньюнктивальный лоскут, 3 – роговичный трансплантат, 4 - интактная роговица.
Отдаленные результаты через 5 месяцев продемонстрированы на рисунке № 11.
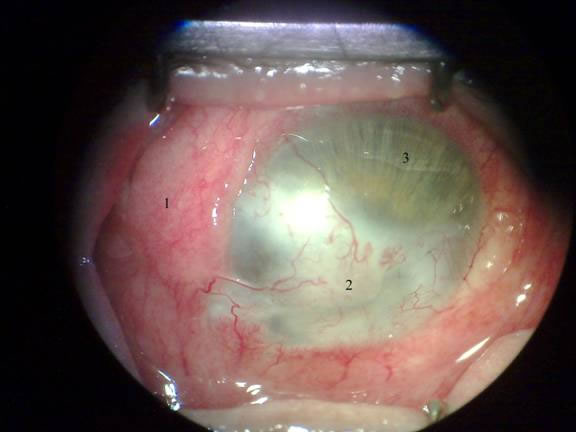
Рис. 11. Состояние после трансплантации (5 месяцев спустя). 1 –конъюнктива, 2 – васкуляризованный роговичный трансплантат, 3 - интактная роговица.
ЗАКЛЮЧЕНИЕ
В данном клиническом случае показана принципиальная возможность использования биоматериалов Аллоплант в практике врача неотложной офтальмологической помощи. Необходимо также отметить биосовместимость, а также ареактивное приживление трансплантатов. Достоинством метода является широкая доступность, длительные сроки хранения, а также возможность создания запаса трансплантатов в ЛПУ.
к содержанию | опубликовать статью
ХИРУРГИЧЕСКОЕ ЛЕЧЕНИЕ ВРОЖДЕННОЙ ГЛАУКОМЫ
С ИСПОЛЬЗОВАНИЕМ БИОМАТЕРИАЛА АЛЛОПЛАНТ
Галимова В.У., Полякова Е.Ю.
ФГУ «Всероссийский центр глазной и пластической хирургии», г.Уфа
ИСПОЛЬЗОВАННЫЕ УСЛОВНЫЕ СОКРАЩЕНИЯ И ОБОЗНАЧЕНИЯ
ВВ – водянистая влага
ВГД – внутриглазное давление
ГПЗ – границы поля зрения
ЗВП – зрительные вызванные потенциалы
КЛО – коэффициент легкости оттока
ОЗ – острота зрения
ПК – передняя камера
ПЭЧ – порог электрической чувствительности
УПК – угол передней камеры
ЭЛ – электрическая лабильность
ЦХО – цилиохориоидальная отслойка
Ро – истинное внутриглазное давление
Актуальность темы. Врожденная глаукома относится к числу редких заболеваний глаза, и встречается в 1 случае из 10 тысяч новорожденных (Сидоров Э.Г. и соавт., 1991; Сидоренко Е.И., 2003; Mandal A. K., 2006). В России уровень детской слепоты и слабовидения составляет 1,6 и 3,5 на 10000 населения соответственно (Хватова А.В. и соавт., 2000; Либман Е.С. и соавт., 2000, 2005). Среди организованных детей в структуре причин слепоты и слабовидения на долю врожденной глаукомы приходится от 2,2 до 12,7% (Ковалевский Е.И., 1995; Хватова А.В. и соавт., 2000; Сидоренко Е.И., 2003; Поспелов В.И., 2003; Либман Е.С. и соавт., 2005; Mandal A. K., 2006); почти каждый 10 ребенок слепнет от врожденной глаукомы (Сидоренко Е.И., 2003). Традиционно хирургическое лечение врожденной глаукомы предусматривает формирование в углу передней камеры (УПК) фистулизирующего компонента на основе операций трабекулотомии, трабекулэктомии, синусотрабекулэктомии в различных модификациях (Ерошевский Т.И., 1985; Сидоров Э.Г., 1986; Качан Н.А., 1997; Хватова А.В. и соавт., 1997; Нурмамедов Н.Н., 2000; Теплинская Л.Е. и соавт., 2003; Khaw P.T., 1996; Mandal A. K., 2004; Catrinu L., 2005). Несмотря на высокий процент положительных результатов фильтрующего типа вмешательств, в 10–60% случаев не удается компенсировать внутриглазное давление (ВГД) по причине рубцевания созданных путей оттока внутриглазной жидкости (Хватова А.В. и соавт., 1997; 2000; Качан Н.А., 2004; Мазанова Е.В., 2004; Shaffer R.N., 1982; Anderson D.R., 1983). Для профилактики процессов рубцевания зоны оперативный вмешательства многие исследователи использовали различные дренажи: ауто-, алло-, ксено- и эксплантодренажи, имплантаты – дренажи с комбинированным типом действия. (Нурмамедов В.П. и соавт., 1991,2000; Азнабаев Р.А. и соавт., 1993; Канюков В.Н. и соавт., 1997, 2003; Галиулина Р.Ш., 2000; Жердецкий А.С. и соавт., 2000; Золотаревский А.В. и соавт., 2000; Зубарева Л.Н. и соавт., 2000; Лапочкин В.И., 2000; Родионова Т. А. и соавт., 2000; Ширин В.В., 2000; Багрова С.Н., 2001;2003; Курышева Н.И., 2005; Мулдашев Э.Р., 2002, 2003; Бакунина Н.А. и соавт., 2005; Мошетова Л.К. и соавт., 2003, 2005). Каждый из предложенных методов хирургического лечения врожденной глаукомы с применением дренажей имеет свои достоинства и недостатки, в настоящее время не существует оптимальной методики, которая позволяет стойко нормализовать офтальмотонус. Поиск новых методов лечения врожденной глаукомы с использованием различных дренажей остается актуальным. Во Всероссийском центре глазной и пластической хирургии накоплен значительный опыт в хирургии как первичной, так и вторичной глаукомы с использованием дренажа из биоматериала Аллоплант губчатой структуры (Мулдашев Э.Р. с соавт., 2002; 2003). Полученные благоприятные результаты позволили использовать данную трансплантационную технологию и в хирургическом лечении врожденной глаукомы. Учитывая изложенное, в настоящей работе авторами поставлена цель - разработать и внедрить антиглаукоматозную операцию с использованием губчатого дренажа из биоматериала Аллоплант при врожденной глаукоме. В ходе исследования были решены следующие задачи: - на модели кортикостероидной глаукомы изучены этапы морфологической перестройки аллогенного губчатого биоматериала, использованного в качестве дренажа при антиглаукоматозной операции. - проведен сравнительный анализ результатов антиглаукоматозных операций с использованием губчатого дренажа из биоматериала Аллоплант и синусотрабекулэктомии при врожденной глаукоме в ближайшие и отдаленные сроки наблюдения. - методом ультразвуковой биомикроскопии изучены пути оттока внутриглазной жидкости, сформированные у больных после антиглаукоматозной операции, с использованием губчатого дренажа из биоматериала Аллоплант в ближайшие и отдаленные сроки наблюдения. - определена эффективность антиглаукоматозной операции с использованием губчатого дренажа из биоматериала Аллоплант при врожденной глаукоме у больных, ранее оперированных другими методами антиглаукоматозных вмешательств. - определены показания и противопоказания к выполнению операции с использованием губчатого дренажа из биоматериала Аллоплант у больных с врожденной глаукомой.
Использованные в работе материалы и методы исследования Для экспериментального моделирования врожденной глаукомы нами использован метод создания кортикостероидной глаукомы, описанной J. Francois (1984). Эксперимент был выполнен на 36 кроликах с соблюдением норм и правил работы с лабораторными животными. Основную группу составил 21 кролик (21 глаз) с кортикостероидной глаукомой, которым была проведена антиглаукоматозная операция с использованием аллогенного губчатого дренажа, изготовленного по технологии Аллоплант. Для динамического изучения этапов морфологической перестройки губчатого биоматериала, в сроки на 7, 14, 21, 30, 60, 90 и 180-е сутки после операции с использованием аллогенного губчатого дренажа, животных выводили из эксперимента (по 3 кролика на каждый срок). Контрольную группу 15 кроликов (15 глаз) составили животные с моделированной глаукомой без хирургического вмешательства, которых выводили из опыта на 21, 30, 60, 90, 180-е сутки. Гистологические препараты энуклеированных глаз исследовались с помощью световой и электронной микроскопии. Для гистологического исследования глазные яблоки кроликов фиксировали в 10% забуференном формалине. Парафиновые срезы окрашивались гематоксилином и эозином и по Ван-Гизону. Ультратонкие срезы контрастировали по Рейнольдсу и изучали под трансмиссионным микроскопом Jeol-100XB (Япония), при увеличениях от 4000 до 8500. Клинический анализ результатов хирургического лечения был проведен у 90 пациентов (103 глаза) с диагнозом врожденная глаукома с некомпенсированным офтальмотонусом. Все пациенты были разделены на две группы: основную и контрольную. Основную группу составили 59 пациентов (71 глаз), которым была проведена антиглаукоматозная операция с использованием губчатого дренажа из биоматериала Аллоплант. Возрастные границы основной группы составляли от 1 года до 52 лет, средний возраст – 19±12 лет. Значения внутриглазного давления (ВГД) по Маклакову составляли 37±5,6 мм рт. ст., истинного ВГД (P0) – 42,8±10,5 мм рт. ст. Начальная стадия определялась в 7 случаях (9,9%), развитая – в 4 (5,6%), далекозашедшая стадия – в 27 (38%), терминальная – в 33 (46,5%). Таким образом, подавляющую часть пациентов (84,5%) составляли случаи с далекозашедшей и терминальной стадиями глаукомы. Доля реопераций в основной группе составила 94,3% (67 глаз у 56 пациентов), в связи с декомпенсацией офтальмотонуса после ранее проведенных антиглаукоматозных вмешательств (от одной до восьми операций) в других клиниках, впервые прооперировано 3 пациента (4 глаза) – 5,7% случаев. Контрольную группу составил 31 пациент (32 глаза) с врожденной глаукомой с некомпенсированным офтальмотонусом, которым была проведена операция синусотрабекулэктомия. Возрастные границы пациентов в контрольной группе составляли 4–53 года, средний возраст – 25±13,4 лет. До операции ВГД по Маклакову составляло 39,5±5,3 мм рт. ст., истинное ВГД (P0) – 40,5±11,2 мм рт. ст. В данной группе пациентов с начальной стадией заболевания не наблюдалось, развитая стадия определялась в 3 (9,4%) случаях, далекозашедшая – в 8 (25%) и терминальная в 21 (65,6%) случае. В 81,2% (26 глаз у 25 пациентов) составляли пациенты с некомпенсированным офтальмотонусом после проведенных ранее антиглаукоматозных вмешательств, 6 пациентов (6 глаз) были прооперированы впервые, что соответствует 18,8% операций от общего числа глаз в этой группе. Сравнительный анализ основной и контрольной групп по стадиям, тяжести течения заболевания и исходному офтальмотонусу значимо не отличался (р > 0,05). Всем пациентам в до- и послеоперационном периоде проводились следующие исследования:визометрия, периметрия, кератометрия, тонометрия по Маклакову, электротонография, электрофизиологические исследования, в том числе зрительные вызванные потенциалы, световая биомикроскопия, офтальмоскопия, ультразвуковая биометрия и биомикроскопия. Офтальмологическая диагностика детям младшего возраста проводилась в палате интенсивной терапии под вводным наркозом. Создание и обработка массивов данных, исследование результатов, а также все расчеты и графическое отображение проводились с помощью современных стандартных пакетов прикладных программ математико-статистической обработки данных. Применялся метод параметрического и непараметрического дисперсионного анализа, кластерный анализ.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
Результаты экспериментально-морфологических методов исследования. При гистологическом изучении срезов глазных яблок кроликов при экспериментальной глаукоме выявлялись признаки дезорганизации коллагеновых волокон отдельных зон роговицы и склеры. В зрительном нерве выявлялись очаги дегенерации части нервных волокон, определялись признаки утолщения соединительнотканных оболочек между нервными волокнами. Электронно-микроскопические исследования показали, что наибольшим деструктивным разрушениям подвергались меланоциты радужки, сосудистой оболочки и структуры угла передней камеры (УПК). Количество стромальных меланоцитов в радужке заметно уменьшалось, в большинстве из них органеллы и пигментные гранулы подвергались деструкции. Изменялась структура УПК глаза кроликов: перегородки между лакунами разрушались, а в углу передней камеры скапливались гранулы и обломки меланина.
Через 21 и 30 суток после прекращения инстилляций дексаметазона без проведения антиглаукоматозной операции восстановления структуры глазных оболочек не наблюдалось.
При исследовании препаратов глазных яблок с моделированной кортикостероидной глаукомой у кроликов после антиглаукоматозной операции с использованием аллогенного губчатого дренажа, было выявлено, что в ранние сроки после операции (7–14 суток), имплантированный кроликам губчатый биоматериал сохранял свое первоначальное строение. Одним концом он свободно располагался в УПК, а другим – в супраувеальном пространстве.
Через месяц после операции, наряду с увеличением инфильтрированной клетками части губчатого трансплантата и замещения его новообразованными волокнами, между ними выявлялись тяжи крупных пролиферирующих эндотелиальных клеток и формировались тонкостенные капилляры. Часть трансплантата, которая находилась в УПК глаза кролика, подвергалась меньшей клеточной инфильтрации, чем участки трансплантата, соприкасающиеся со склерой.
На 90–180-е сутки после операции губчатый аллотрансплантат полностью замещался ячеистой васкуляризированной рыхлой соединительной тканью. Волокнистые балки ячеек новообразованной ткани, расположенные в УПК, были выстланы преимущественно эндотелиальными клетками. В толще средней части регенерата, представляющей собой очень рыхлую сеть новообразованной ткани, выявлялось множество тонкостенных капилляров. В задних отделах биоматериала в супрахориоидальном пространстве обнаруживались более крупные венозные сосуды.
Таким образом, у кроликов с экспериментальной кортикостероидной глаукомой после антиглаукоматозной операции с применением губчатого дренажа, изготовленного по технологии Аллоплант, в результате структурно-морфологических изменений на месте введенного губчатого биоматериала формировалась активная дренажная система, без признаков рубцовой облитерации, способствующая оттоку водянистой влаги из передней камеры (ПК). Восстановление дренажной системы глаз кроликов приводило к исчезновению отек сетчатки и зрительного нерва, восстановлению структуры стромальных меланоцитов радужки.
Результаты клинических исследований
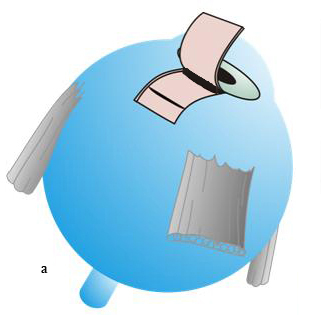
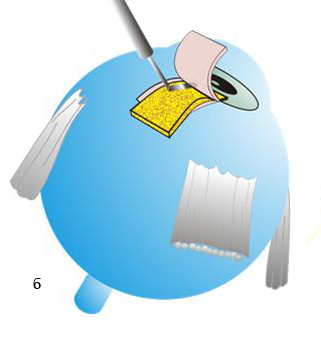
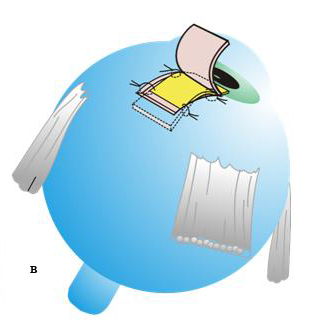
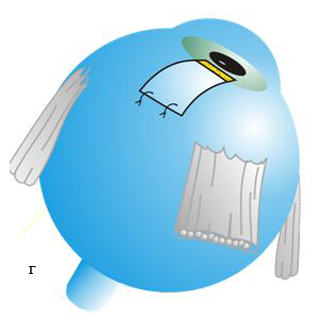
Техника антиглаукоматозной операции при врожденной глаукоме с применением губчатого дренажа из биоматериала Аллоплант (основная группа). Операция выполнялась в любом из доступных секторов глазного яблока между прямыми мышцами. В 5 мм от лимба концентрично ему производили разрез конъюнктивы длиной 7–8 мм с субконъюнктивальной тканью до лимба. На близлежащие прямые мышцы накладывали швы-держалки. Глазное яблоко фиксировали. После предварительного гемостаза из поверхностных слоев склеры на половину ее толщины формировали прямоугольный лоскут размером 5×6 мм основанием к лимбу (рис. 1а). Склеральный лоскут откидывали на роговицу, используя желобоватый шпатель производили сквозной разрез глубоких слоев склеры, отступя от лимба на 5 мм, до супраувеального пространства на всю ширину образовавшегося склерального ложа (рис. 1а). В УПК выполняли синусотрабекулэктомию: у лимба иссекали глубокие слои дренажной зоны вместе с синусом и трабекулой в виде прямоугольника размерами 5×1 мм (рис. 1а). Губчатый дренаж из биоматериала Аллоплант, размерами 8×4 мм и высотой в 1 мм, укладывали на дно склерального ложа, затем передний конец дренажа через зону синусотрабекулэктомии вводили в ПК на 1,5–2 мм (рис. 1б). Задний конец заправляли в супраувеальное пространство через разрез в глубоких слоях склеры. Фиксацию дренажа проводили узловыми швами к краям склерального ложа у лимба и у места введения его в супраувеальное пространство узловыми швами шелком 8/0 (рис. 1в). Поверхностный склеральный лоскут укладывали на место и фиксировали узловыми швами 8/0 (рис. 1г). Конъюнктивальная рана восстанавливалась непрерывным швом.
 |
 |
 |
 |
| a | б | в | г |
а – сформирован поверхностный склеральный лоскут, в глубоких слоях склеры произведен сквозной разрез до супраувеального пространства на всю ширину склерального ложа, у лимба иссечена дренажная зона вместе с синусом и трабекулой в виде прямоугольника (этап синусотрабекулэктомии);
б – передний конец дренажа из биоматериала Аллоплант через зону синусотрабекулэктомии введен в переднюю камеру;
в – задний конец дренажа введен в супраувеальное пространство через разрез в глубоких слоях склеры, наложены фиксирующие узловые швы;
г – поверхностный склеральный лоскут уложен на место и фиксирован узловыми швами.
Сравнительная оценка офтальмотонуса в основной и контрольной группах. Анализ результатов операций в исследуемых группах показал, что динамика истинного внутриглазного давления (P0) и по Маклакову была идентичная в обеих группах (рис. 2).
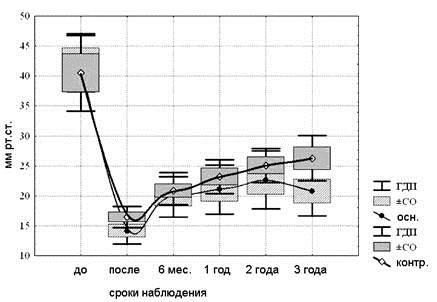
Рис. 2. Динамика изменений внутриглазного давления в основной и контрольной группах
Предоперационные средние значения P0 в обеих группах практически совпадали: 42,8±10,5 мм рт. ст. и 40,5±11,2 мм рт. ст., соответственно, и достоверно не различались (p = 0,54). После операции средний уровень офтальмотонуса в группах резко снижался до 14,1±5,3 мм рт. ст. в основной группе и 16,5±3,1 мм рт. ст. – в контрольной (p = 0,16). Через полгода после операции средний уровень ВГД в обеих группах значимо (p = 0,04) возрастал и составлял 20,8±9,3 мм рт. ст. и 20,6±4,1 мм рт. ст., соответственно, далее в основной группе ВГД стабилизировалось, а в контрольной – наблюдалось его повышение. Средние значения ВГД к трем годам после операции достигли значений 21,6±10,0 мм рт. ст. в основной и 26,1±6,1 мм рт. ст. – в контрольной.
Таким образом, сравнительный анализ показателей ВГД в основной и контрольной группах показал эффективность операции, используемой в основной группе в отдаленные сроки наблюдения в 74,5% случаях, по сравнению с контрольной группой – 46%.
Гидродинамические показатели коррелировали с данными ВГД. Дооперационные значения КЛО составляли в основной группе 0,11±0,08 мм³/мин/мм рт. ст., в контрольной – 0,09±0,01 мм³/мин/мм рт. ст. (р < 0,05). В раннем послеоперационном периоде отмечалось увеличение оттока внутриглазной влаги в обеих группах: до 0,53±0,06 мм³/мин/мм рт. ст. – в основной, и в контрольной до 0,77±0,02 мм³/мин/мм рт. ст. (р < 0,05). Далее КЛО в основной группе держался стабильно в пределах 0,42±0,08 мм³/мин/мм рт. ст. к концу срока наблюдения. В контрольной группе отмечалось снижение КЛО в сроке до 6 мес. до значений 0,30±0,06 мм³/мин/мм рт. ст., с последующим плавным снижением к концу срока наблюдения до 0,20±0,06 мм³/мин/мм рт. ст.
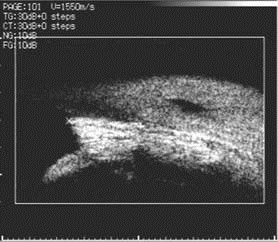
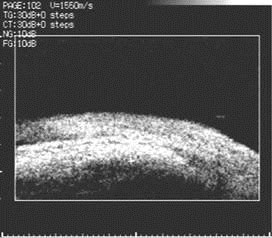
При проведении ультразвуковой биомикроскопии (УБМ) зоны имплантации губчатого дренажа из биоматериала Аллоплант в основной группе в различные сроки наблюдения было выявлено формирование дополнительных путей оттока: субконъюнктивального и увеосклерального. Мы оценивали функциональную состоятельность дренажа в интрасклеральном канале с учетом его качественных характеристик. В исследование были включены следующие параметры топографических характеристик губчатого дренажа: а) положение в ПК (выстояние и акустическая плотность); б) состояние в интрасклеральной полости (размеры и акустическая плотность); в) высота фильтрационной подушки (размеры). Кроме того, определяли степень эхогенности биоматериала в зависимости от плотности ткани, сопоставляя с акустической плотностью склеры, которая, как известно, имеет наибольшую величину при ультразвуковых исследованиях глаза (Волкова Н.В. и соавт., 2008, Тахчиди Х.П. и соавт., 2006). Данное обследование было проведено на 11 глазах (7 пациентов), в сроки наблюдения: до 1 мес., 1 мес. – 1 год и 1–4 года. Полученные результаты представлены в таблице 1, рис. 3, 4, 5, 6.
Таблица 1. УБМ-ПОКАЗАТЕЛИ ЗОНЫ ФИЛЬТРАЦИИ ВОДЯНИСТЙ ВЛАГИ В ОСНОВНОЙ ГРУППЕ В РАЗЛИЧНЫЕ СРОКИ НАБЛЮДЕНИЯ
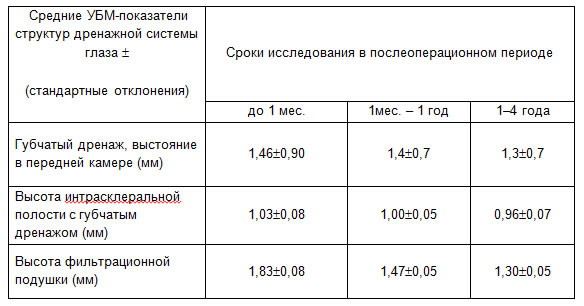
Необходимо отметить, что неоднородность структуры дренажа сохранялась на всем его протяжении. Размеры выстояния дренажа в УПК к концу срока наблюдения составляли 1,30,7 мм. В интрасклеральной полости существенных изменений структуры дренажа мы не наблюдали, средний размер дренажа между слоями склеры составлял 0,960,07 мм. Фильтрационная подушка оставалась плоскоразлитой, с высотой 1,30,05 мм, подтверждающая состоятельность сформированных путей оттока (Волкова Н.В. и соавт., 2008).
 |
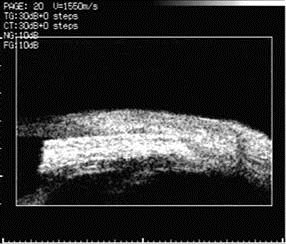 |
| Рис. 3. УБМ (7 дней после операции). Топография губчатого дренажа Аллоплант | Рис. 4. УБМ (1,5 мес. после операции). Формирование системы дренажных канальцев в губчатом дренаже |
 |
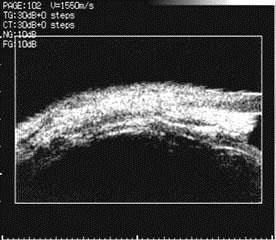 |
| Рис. 5. УБМ (1,5 мес. после операции). Формирование системы дренажных канальцев в губчатом дренаже | Рис. 6. УБМ (4 г. 6 мес.). Сохранность сформированной системы дренажных щелей и полостей после операции |
Таким образом, анализ данных сканограмм показал, что губчатый дренаж из биоматериала Аллоплант сохранял свою губчатую структуру и способствовал сохранению зоны фильтрации ВВ в области оперативного вмешательства в сроки наблюдения до 4 лет. Длительное функционирование сформированных путей оттока подтверждалось нормализованными показателями офтальмотонуса.
Сравнительная оценка показателей функционального состояния зрительной системы. При проведении анализа результатов исследования остроты зрения (ОЗ) в группах мы распределили все случаи исходной ОЗ на три условные категории: 1 – «слепота», 2 – «светоощущение» (соответствовала ОЗ от неправильной светопроекции до счета пальцев у лица до 50 см), 3 – «предметное зрение» (соответствовало от 0,01 и выше). К концу срока наблюдения улучшение ОЗ отмечали в основной группе у пациентов с предметным зрением в 28% случаев, в других подгруппах прослеживалось стабильное состояние ОЗ, что составляло 53% случаев. В контрольной группе у пациентов с предметным зрением улучшения не наблюдалось, стабильные показатели ОЗ отмечались в 64%.
Динамика границ полей зрения (ГПЗ). Обработка данных полей зрения осуществлялась путем распределения их значений на категории и анализ изменений долевого участия в различные сроки наблюдения. Исходя из наличия данных, было сформировано три категории границ полей зрения (ГПЗ): 1 – «0» – поля зрения не обнаруживаются; 2 – значения границ полей зрения «менее 250°»; 3 – значения границ полей зрения «более 250°». Анализ результатов операций по данным ГПЗ в основной группе показал, что поля зрения не обнаруживались, примерно, в половине случаев (от 59 до 52%) (рис. 7). Доля таких случаев медленно снижалась с 59% до операции к 52% к концу срока наблюдения. Доля случаев ГПЗ «более 250°» возросла от 16 до 23% к двум годам после операции и снизилась к концу срока наблюдения до 20%. Таким образом, улучшение состояния полей зрения в основной группе, несомненно, имело место, распространяясь на отдельные категории ГПЗ.
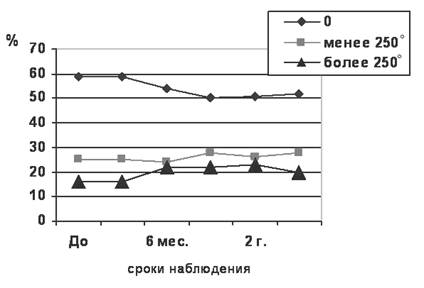
Рис. 7. Динамика ГПЗ в основной группе в исследуемые сроки наблюдения
В контрольной группе сложилась несколько иная картина (рис. 8). Доля случаев отсутствия полей зрения составляла около двух третей (62–68%) и практически не менялась во все сроки наблюдения. В прочих категориях, изменения соотношения их долей закономерности не выявлено.
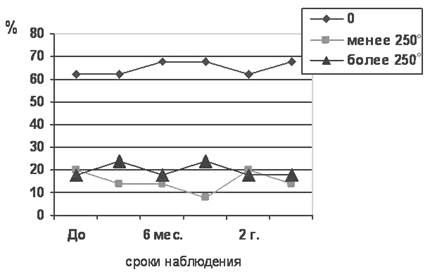
Рис. 8. Динамика ГПЗ в контрольной группе в исследуемые сроки наблюдения
Таким образом, в основной группе при наличии определенных полей зрения после операции наблюдалась тенденция к расширению их границ. В контрольной группе изменений ГПЗ не наблюдалось.
Обработка данных показателей порога электрической чувствительности (ПЭЧ), с формированием трех категорий вариаций: 1 – ПЭЧ «более 750 мкА», 2 – ПЭЧ «от 250 до 750 мкА»; 3 – ПЭЧ «менее 250 мкА» показала следующий результат. Доля случаев уровня ПЭЧ «менее 250 мкА», составляющая до операции 24%, в послеоперационные сроки нарастала, достигая, к трем годам 32%, а доля случаев «более 750 мкА», напротив, снижалась с дооперационных 55 до 43% к концу сроков наблюдения. Таким образом, можно отметить, что в основной группе отчетливо проявлялись тенденции к улучшению показателей ПЭЧ в 55,5% случаев. В контрольной группе доля значений ПЭЧ «менее 250 мкА», составляющая 25% до операции, сохранялась и после нее, и к концу сроков наблюдения уменьшилась до 13%. Доли двух других категорий значимо не изменялись. В целом, в контрольной группе не происходило перераспределения уровней ПЭЧ в сторону улучшения, а наблюдалось стабильное состояние показателей ПЭЧ.
Результаты показателей электрической лабильности (ЭЛ) были разделены так же на три категории: 1 – ЭЛ «менее 6 Гц»; 2 – ЭЛ «от 6 до 20 Гц», 3 – ЭЛ «более 20 Гц». В основной группе отчетливо проявлялись две противоположные тенденции. Показатели ЭЛ «более 20 Гц», составлявшие до операции 43%, увеличились к концу срока наблюдения до 55% случаев. Доля же случаев с показателями ЭЛ «менее 6 Гц», начиная с дооперационных 47% значений, последовательно снижалась, и к трем годам достигала 30%. Доля «от 6 Гц до 20 Гц», составлявшая 10%, к концу срока наблюдения достигла 15% случаев. Таким образом, в основной группе в послеоперационном периоде имел место достоверный рост доли значений ЭЛ, варьирующих в диапазоне «нормы», за счет снижения доли «патологических» и «грубо патологических» значений ЭЛ. Все это свидетельствовало о закономерном улучшении состояния подвижности основных нервных процессов в сетчатке и зрительном нерве.
Анализ результатов операции в контрольной группе по показателям ЭЛ показал увеличение доли «патологических» значений ЭЛ, а нормализация функциональной подвижности нервной ткани глаза носила случайный характер и прекращалась в отдаленные послеоперационные сроки.
С целью динамического контроля электрофизиологических состояний зрительной системы помимо стандартного офтальмологического исследования пациентам в основной группе были проведены исследования зрительно вызванных потенциалов (ЗВП). При анализе ЗВП оценивали амплитудно-временные параметры ответов, получаемых до операции и в отдаленные сроки наблюдения (табл. 2). В результате статистической обработки полученных данных было выявлено уменьшение латентности основного комплекса ЗВП, которое не сопровождалось изменением амплитуды ответа. Данный факт можно было рассматривать как показатель улучшения функционального состояния волокон зрительного нерва, что совпадает с данными литературы (Фильчикова Л.И. с соавт., 1992; Шамшинова А.М., Волков В.В., 1999; Важенков С.Н., 2008).
Таблица 2. ДИНАМИКА АМПЛИТУДНО-ВРЕМЕННЫХ ПАРАМЕТРОВ ЗВП В ОСНОВНОЙ ГРУППЕ
| Параметр | Средние показатели ±стандартное отклонение (до операции) |
Средние показатели ±стандартное отклонение (после операции) |
| Амплитуда N1-P2 (мкВ) |
5,11 ± 4,82 |
5,79 ± 6,55 |
| Пиковое время N1 (мс) |
98,26 ± 8,1 |
83,66 ± 14,62 |
| Пиковое время P2 (мс) |
135,53 ± 13,86 |
122,64 ± 13,46 |
Сравнительная характеристика биометрических показателей в основной и контрольной группах. Оптическая ось глаза (ООГ). По данным литературы, у пациентов с врожденной глаукомой, из биометрических параметров в наибольшей степени по мере прогрессирования процесса увеличивается ООГ (Сидоров Э.Г. и соавт., 1986, 1991; Ковалевский Е.И., 1985; Сидоренко Е.И., 2003). Ультразвуковое исследование ООГ в исследуемых группах проводилось с целью определения стабилизации глаукомного процесса после антиглаукоматозных операций. Как следует из таблицы 3, дооперационные значения показателей ООГ не различались (р = 0,86), в основной группе средние значения ООГ к концу срока наблюдения практически не изменились и составили 26,23±2,4мм, в контрольной же группе наблюдалась тенденция к увеличению ООГ в сравнении с исходными значениями до 28,1±5,2 мм (р = 0,29).
Таблица 3 ДИНАМИКА ООГ В ОСНОВНОЙ И КОНТРОЛЬНОЙ ГРУППАХ
Группы |
Средние показатели ООГ± стандартное отклонение (до операции, мм) |
Средние показатели ООГ ±стандартное (через 3 года после операции, мм) |
Основная (с губчатым дренажом) |
26,85±3,15 мм |
26,23±2,40 мм |
Контрольная (синусотрабекулэктомия) |
26,7± 3, мм |
28,1±5,2 мм |
В исследовательской группе антиглаукоматозная операция с применением губчатого дренажа из биоматериала Аллоплант была проведена в качестве реоперации у 56 пациентов (67 глаз), что составило 94,3% от операций в основной группе, в связи с декомпенсацией ВГД после ранее проведенных антиглаукоматозных вмешательств (от одной до шести операций).
В контрольной группе реоперация синусотрабекулэктомия была проведена в 81,2%, соответственно 25 пациентам (26 глаз). Следует отметить, что в исследуемых группах проводились предшествующие традиционные фистулизирующие операции, операции с комбинированным типом действия и операции с использованием различных дренажей.
Офтальмотонус до операции, в группах реопераций, значимо не различался от такового в предыдущих группах и составлял 38,1±5,6 мм рт. ст. в основной и 37,3±7,2 мм рт. ст. – в контрольной. Динамические изменения офтальмотонуса в группах реопераций не различались от показателей ВГД в соответвующих группах и к концу срока наблюдения составили 22,7±11,2 мм. рт. ст. 28,1±6,2 мм рт. ст, соответственно (р < 0,05). Сравнительный анализ показателей функционального состояния зрительной системы в группе реопераций не различался от результатов в соответствующих группах.
Таким образом, антиглаукоматозная операция с применением губчатого дренажа из биоматериала Аллоплант, используемая в качестве реоперации при врожденной глаукоме, способствовала стойкой нормализации офтальмотонуса в течение всего срока наблюдения, а также стабильному функциональному состоянию зрительных функций.
Возможные осложнения. Анализ частоты ранних послеоперационных осложнений показал, что чаще в обеих группах встречалась гипотония (9,8 и 12,5%), цилиохориоидальная отслойка (ЦХО) (18,3 и 21,8%), гифема (4,2 и 6,25%), однако в основной группе их было меньше (табл. 4). Низкий процент гипотонии и ЦХО в основной группе мы связываем с использованием губчатого дренажа для прикрытия фильтрационной зоны и отсутствия ранней фильтрации влаги передней камеры в субсклеральное и субконъюнктивальное пространство. Снижение резкого послеоперационного перепада давления проявлялось менее выраженными послеоперационными патологическими сосудистыми реакциями. В то время как, при операции синусотрабекулэктомии зона фильтрации водянистой влаги (ВВ) оставалась неприкрытой, и ток камерной влаги осуществлялся непосредственно под поверхностный склеральный лоскут и далее под конъюнктиву.
Таблица 4 ХАРАКТЕРИСТИКА РАННИХ ПОСЛЕОПЕРАЦИОННЫХ ОСЛОЖНЕНИЙ ПОСЛЕ АНТИГЛАУКОМАТОЗНЫХ ОПЕРАЦИЙ В ОСНОВНОЙ И КОНТРОЛЬНОЙ ГРУППАХ 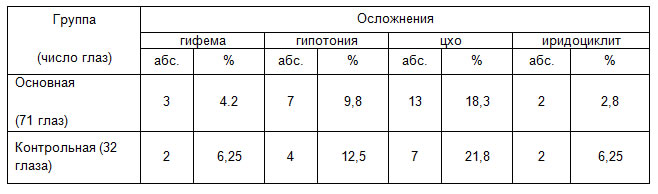
Таким образом, анализ результатов проведенных исследований показал, что антиглаукоматозная операция с использованием губчатого дренажа из биоматериала Аллоплант эффективна при лечении различных стадий врожденной глаукомы, позволяет нормализовать внутриглазное давление и стабилизировать зрительные функции. Предложенный дренаж из биоматериала Аллоплант препятствует избыточному рубцеванию зоны фильтрации и способствует формированию двух путей оттока ВГЖ: субконъюнктивального и увеосклерального. Разработанная антиглаукоматозная операция является эффективным методом реоперации врожденной глаукомы с некомпенсированным офтальмотонусом.
Заключение
Таким образом, нами разработана антиглаукоматозная операция с использованием губчатого дренажа из биоматериала Аллоплант у больных с врожденной глаукомой с целью снижения, и в последующем, стойкой стабилизации внутриглазного давления и зрительных функций.
Предложен губчатый дренаж из биоматериала Аллоплант для профилактики рубцовых изменений путей оттока, сформированных при хирургическом лечении врожденной глаукомы. Разработан и внедрен в практику эффективный метод хирургического лечения врожденной глаукомы – антиглаукоматозная операция с применением губчатого дренажа из биоматериала Аллоплант.
В эксперименте: на модели кортикостероидной глаукомы показано, что аллогенный губчатый дренаж, изготовленный по технологии Аллоплант, имплантированный в переднюю камеру и далее в супраувеальное пространство, к 180 суткам замещается пористой соединительной тканью с ячеистой структурой, с преимущественной эндотелиальной выстилкой микропор, без признаков рубцевания в области оперативного вмешательства.
При сравнительном анализе результатов антиглаукоматозных операций: с использованием губчатого дренажа из биоматериала Аллоплант (основная группа) и операции синусотрабекулэктомии (контрольная группа) выявлена нормализация внутриглазного давления в отдаленные сроки наблюдения (до 3 лет) в 74,5% случаев (в контрольной группе – в 46%), что способствовало сохранению и улучшению остроты зрения в 81%, (в контрольной – в 64%), а также расширению полей зрения в 19% случаев (в контрольной – в 7%).
Ультразвуковая биомикроскопия зоны оперативного вмешательства в послеоперационном периоде в различные сроки наблюдения показала, что губчатый биоматериал способствовал формированию двух путей оттока внутриглазной жидкости: увеосклерального и субконъюнктивального.
Антиглаукоматозная операция с применением губчатого дренажа из биоматериала Аллоплант, используемая в качестве реоперации при врожденной глаукоме, способствовала стойкой нормализации офтальмотонуса в течение всего срока наблюдения и стабильному функциональному состоянию глаза.
Показанием к проведению операции с губчатым дренажом из биоматериала Аллоплант является некомпенсированная врожденная глаукома различных стадий, данная операция может быть рекомендована в качестве эффективного метода реоперации после предшествующих гипотензивных вмешательств с рецидивами повышения офтальмотонуса.
Операция с использованием губчатого дренажа из биоматериала Аллоплант рекомендуется для хирургического лечения врожденной глаукомы при некомпенсированном офтальмотонусе с целью стойкой нормализации внутриглазного давления и сохранения зрительных функций. Губчатый дренаж из биоматериала Аллоплант рекомендуется для профилактики рубцевания путей оттока внутриглазной жидкости, сформированных в результате антиглаукоматозной операции.
Литература
1. Морфология путей оттока внутриглазной жидкости в дренажной зоне, сформированной в губчатом аллогенном биоматериале «Аллоплант» [Текст] / Г.Г. Корнилаева, С.А. Муслимов, М.П. Корнилаева, Е.Ю. Полякова, Э.В. Галимова // Вестник Оренбургского государственного университета. – 2005. – Спец. Вып.: Новое в экспериментально-морфологическом изучении глаза: материалы Российской научной конференции с международным участием (21-23 сентября 2005 г., Оренбург). – С. 74–75.
2. Профилактика рубцевания послеоперационной зоны губчатым биоматериалом «Аллоплант» при хирургическом лечении первичной глаукомы [Текст] / Э.Р. Мулдашев, Г.Г. Корнилаева, Э.В. Галимова, Е.Ю. Полякова [и др.] // Вестник Оренбургского государственного университета. – 2004. – Спец. Вып.: Новые технологи микрохирургии глаза: материалы юбилейной 15 Российской научно-практической конференции, посвященной 15-летию Оренбургского филиала ГУ МНТК «Микрохирургия глаза» им. Академика С.Н. Федорова. – С. 41–42.
3. Хирургическое лечение врожденной глаукомы с использованием биоматериала Аллоплант [Текст] / Э.Р. Мулдашев, Г.Г. Корнилаева, Е.Ю. Полякова, М.П. Корнилаева, Э.В. Галимова // Вестник Оренбургского государственного университета. – 2004. – Спец. Вып.: Новые технологи микрохирургии глаза: материалы 15 Российской научно-практической конференции, посвященной 15-летию Оренбургского филиала ГУ МНТК «Микрохирургия глаза» им. Академика С.Н. Федорова. – С. 56.
4. Комбинированное хирургическое лечение врожденной глаукомы в сочетании с круговыми стафиломами склеры биоматериалом Аллоплант [Текст] / Э.Р. Мулдашев, Г.Г. Корнилаева, В.У. Галимова, Е.Ю. Полякова // Новые технологии микрохирургии глаза: 14 Российская ежегодная научно–практическая конференция. – Оренбург, 2003. – С. 111–113.
5. Морфофункциональные изменения в оболочках глазного яблока при кортикостероидной глаукоме [Текст] / Г.Г. Корнилаева., Э.В. Галимова., Е.А Волгарева, Е.Ю. Полякова [и др.] // Роль природных факторов и туризма в формировании здоровья населения: материалы IV Российской научной конференции. – Уфа, 2006. – С. 20–21.
6. Мулдашев, Э.Р. Реконструктивные подходы к хирургическому лечению врожденной глаукомы на основе губчатого биоматериала Аллоплант [Текст] / Э.Р. Мулдашев, Г.Г. Корнилаева, Е.Ю. Полякова // VIII съезд офтальмологов России: тезисы докладов. – М., 2005. – С. 202–203.
7. Полякова, Е.Ю. Состояние зрительных функций после операции губчатого дренирования при врожденной глаукоме [Текст] / Е.Ю. Полякова // Материалы I научно-практической конференции офтальмологов Южного Федерального Округа, посвященной 130-летию со дня рождения основателя Ростовской школы офтальмологии профессора Константина Хрисановича Орлова. – Ростов н/Д, 2005. – С. 105.
8. Реконструктивная хирургия вторичной глаукомы с использованием губчатого биоматериала Аллоплант [Текст] / Э.Р. Мулдашев, Г.Г. Корнилаева, М.П. Корнилаева, Е.Ю. Полякова // Глаукома: проблемы и решения: Всероссийская научно-практическая конференция. – М., 2004. – С. 318–320.
9. Структурные изменения диспергированного биоматериала Аллоплант, введенного в субтеноново пространство глаза при глаукоме [Текст] / Г.Г. Корнилаева, С.А. Муслимов, М.П. Корнилаева, Е.Ю. Полякова [и др.] // Роль природных факторов и туризма в формировании здоровья населения: материалы IV Российской научной конференции. – Уфа, 2006. – С. 20–21.
к содержанию | опубликовать статью
Применение диспергированного биоматериала Аллоплант для лечения поражений переднего сегмента глазного яблока
Булатов Р.Т., Белова Е.А.
ФГУ «Всероссийский центр глазной и пластической хирургии», г.Уфа
Актуальность
В офтальмологической практике остаются актуальными поражения роговицы и конъюнктивы, которые сопровождаются их деэпитализацией: термические и химические ожоги различной степени и другие травмы органа зрения, эрозии роговицы, некоторые острые и хронические воспалительные заболевания переднего сегмента глазного яблока.
Так, по данным А.М. Южакова с соавторами (1991) в общей структуре глазной патологии у населения России по обращаемости одно из первых мест занимают воспалительные заболевания (25%) и травмы (7.3%). Данный факт объясняет повышенный интерес представителей теоретической и практической медицины указанным проблемам. Так, теоретические проблемы регенерации эпителия конъюнктивы и роговицы изучались в работах П.В. Дунаева (1970), О.А. Жукова (1998), С.А. Муслимова (1985) и других авторов.
Разработке консервативных хирургических методов лечения рассматриваемых поражений органа зрения посвящены публикации Ю.Е. Батманова и др. (1920), В.У. Галимова (1981) и других авторов.
Несмотря на значительное число публикаций, настоящая проблема далека от своего разрешения. Остаются неизученными многие факторы, влияющие на процессы репаративной регенерации роговицы и конъюнктивы. Как следствие этого, в клинической практике зачастую отсутствуют доступные для применения в условиях каждого офтальмологического отделения или кабинета лечебные средства. Большинство рекомендуемых препаратов импортные, возможность создания их запасов для ургентной помощи ограничены.
В связи с изложенным, мы проанализировали возможности применения биоматериалов АЛЛОПЛАНТ, производимых в лаборатории трансплантатов ВЦГиПХ, для лечения поражения роговицы и конъюнктивы. Указанные биоматериалы разработаны под руководством Э.Р. Мулдашева (1970-1994), из которых мы обратили внимание на два:
- Аллоплант для послойной кератопластики (обоснован в диссертации Р.З. Кадырова, 1998).
- Аллоплант для пластики конъюнктивы (обоснован в работах В.У. Галимовой и С.А. Муслимова, 1981)
В отмеченных работах доказано, что биоматериалы АЛЛОПЛАНТ обладают низкими антигенными свойствами и после пересадки в дефекты роговицы или конъюнктивы, стимулируют регенерацию собственных структурных адекватных тканей, избегая рубцовых деформаций. Примечательно, что применение данных аллотрансплантатов приводит к быстрой эпителизации их поверхности.
Однако авторами (Р.З. Кадыров,В.У. Галимов, С.А. Муслимов) разработаны только хирургические способы пересадки аллотрансплантатов серии АЛЛОПЛАНТ. По нашему мнению значительный контингент больных с поражениями роговицы и конъюнктивы могут получать лечение на основе диспергированных форм биоматериалов АЛЛОПЛАНТ (Р.А. Хасанов, 1998).
Диспергированный материал аллоплант (ДБА) обладает выраженным противовоспалительным действием, эффективно стимулирует регенерацию эпителия и соединительнотканных структур внутренних органов, кожных покровов (С.А. Муслимов, 2000; В.М. Соколов, 1987). Однако до настоящего времени не разработаны его лекарственные формы для лечения патологии переднего сегмента глазного яблока, не определены схемы применения, показания и противопоказания.
Цель исследования:
Определить возможности применения диспергированных биоматериалов алоплант для лечения поражений конъюнктивы и роговицы.
Материалы и методы исследований
В данной работе мы задались целью разработать биоматериал, избирательно стимулирующий восстановление эпителиального покрова указанных анатомических образований.
Для этой цели нами разработана диспергированная форма биоматериала Аллоплант (ДБА) с размерами частиц от 80 до 100 мкм, содержащая в своей структуре фрагменты коллагеновых и эластических волокон, комплекс протеогликанов внеклеточного матрикса плотной волокнистой соединительной ткани. Обработку трансплантатов осуществляли по технологии аллоплант, разработанной Э.Р. Мулдашевым (1988,1994). В данной работе мы изучали процесс формирования конъюнктивального эпителия.
Эксперимент был проведен на 16 кроликах "Шиншилла". Под местным обезболиванием иссекали участок бульбарной конъюнктивы размерами 10х10 мм, с последующим покрытием дефекта ДБА. Трансплантаты и прилежащие участки конъюнктивы исследовали через 7, 14 и 30 суток. После забивки экспериментальных кроликов отсепаровывалась бульбарная конъюнктива в виде тотальной пленки с последующей импрегнацией нитратом серебра. Микроскопию поверхности конъюнктивы проводили в отраженном свете, окончательное формирование эпителия оценивали по гистологическим срезам окрашенным гематоксилин-эозином, по ван-Гизон.
Сводные данные о методах морфологических исследований:
Уровень исследования |
Методика |
Цель применения |
Органный |
1.Макро-микорпрепарирование с докраской пикрофуксином по А. П. Сорокину 2. Испытание на линейное растяжение с помощью разрывных машин | 1. Изучение поверхности эпителия конъюнктивы |
Тканевой Клеточный |
Окраска гистологических срезов: -гематоксилин-эозином -по Ван-Гизону, по Маллори, -импрегнация метамином серебра -поляризационная микроскопия - импрегнация нитратом серебра | -изучение общей морфологии -изучение волокнистых структур -изучение органного сосудистого русла |
| Субклеточный | Сканирующая электронная микроскопия | -изучение архитектоники волокнистого остова |
Для лечения были выбраны пациенты со следующими нозологическими формами:
химический ожог роговицы 2 степени – 8 пациентов,
химический ожог конъюнктивы 2-3а степени- 8 пациентов,
эрозия роговицы – 2 пациента,
язва роговицы – 1 пациент,
рана роговицы –1 пациент,
птеригиум (после иссечения) –3 пациента,
травматический кератит – 2 пациента,
состояние после лечебной кератопластики - 1 пациент,
базалиома века (после резекции) – 1 пациент,
состояние после удаления пингвикулы – 1 пациент
Была разработана и использована следующая схема применения ДБА для лечения поражений роговицы и конъюнктивы.
1. Применение ДБА в нативном виде для закладывания в конъюнктивальную полость. Процедура выполняется 3-4 раза в день. Применяется при наиболее поверхностных поражениях эпителия с целью создания гелеобразного пленочного покрытия.
2. Лекарственная форма ДБА на основе тетрациклиновой мази в пропорции 1:1. Применяется при более глубоких поражениях конъюнктивы и роговицы в первые 2-3 суток для профилактики инфекционных осложнений.
3. Лекарственная форма ДБА на основе облепихового масла в пропорции 1:1. Применяется через 3 суток после начала лечения для стимуляции регенерации соединительнотканных структур и эпителия конъюнктивы и роговицы.
Результаты исследования и их обсуждение:
Результаты проведенных исследований показали, что восстановление эпителия на фоне действия ДБА происходит по тем же закономерностям, что и при пластике структурированным биоматериалом Аллоплант.
Независимо от размеров трансплантата в первые 7 суток происходит формирование первичного эпителия по всей поверхности трансплантата. Распределены они не сплошным слоем, а неравномерно как по площади трансплантата, так и по количеству слоев в их скоплениях.
Во всех случаях применения ДБА отмечался выраженный противовоспалительный эффект уже через сутки после начала лечения. Раннее купирование отека приводило также к снятию болевого синдрома. Следует отметить, что данный эффект достигался без применения лекарственных препаратов специального назначения ( анальгетики, противоотечные и др.).
Используемый трансплантат можно рассматривать как эффективный стимулятор регенерации тканей. Это проявлялось в относительно быстром формировании соединительнотканной основы конъюнктивы и стромы роговицы и их эпителизации. Особенно демонстративно описанные свойства ДБА проявляются при лечении химических ожогов конъюнктивы 2-3а степени. Для сравнения нами выбрана контрольная группа пациентов с данной патологией, у которых лечение проведено в нашей клинике ранее традиционными способами. Подобные поражения в контрольной группе заканчивались чаще всего рубцеванием конъюнктивы в области ожога или формированием симблефарона. В опытной группе лечение с применением ДБА начиналось с первых суток. Отторжение некротических масс происходило на 3-4 сутки. Размеры открытого дефекта составляли 4*5 мм. После образования открытого раневого дефекта лечение продолжалось комбинацией ДБА- облепиховое масло.
Полная эпителизация дефекта происходит на 9 сутки лечения. Ни в одном случае мы не наблюдали деформаций конъюнктивы или формирования симблефарона. Отмечалось значительное улучшение зрения по сравнению с контрольными группами. Удалось добиться некоторого сокращения длительности пребывания пациентов в стационаре. У 5 из 7 пациентов отмечалось восстановление прозрачности роговицы, что значительно превышало показатели в контроле.
У пациентов с кератитами после применения ДБА в 1,5 раза сократилась длительность роговичного синдрома, у 10 пациентов из 16 полностью восстановилась прозрачность роговицы, сократилась длительность пребывания пациентов в стационаре в среднем с 13 до 11суток. Удалось добиться значительного улучшения зрения.
Диспергированный биоматериал аллоплант можно рассматривать как эффективный стимулятор репаративной регенерации эпителиальной ткани роговицы. Об этом свидетельствуют клинические данные, полученные после применения ДБА пациентам с травматической эрозией роговицы. Результаты лечения весьма обнадеживающие: отмечается значительное улучшение зрения, случаи помутнения в опыте составляют 25 %, что в два раза превышает показатели контрольных групп, отмечается сокращение роговичного синдрома.
Заключение и практические рекомендации
Экспериментальные исследования и клинические исследования показали, что ДБА стимулирует развитие двух типов регенерации эпителия конъюнктивы: островковая и краевая. Краевая эпителизация происходит за счет активации и пролиферации клеток по краю раневого дефекта. Островкоая эпителизация происходит путем адгезии эпителиальных клеток на поверхность раневого дефекта. При этом факторы, имеющиеся в составе ДБА (гепаран-сульфат, коллаген) способствуют росту эпителия по краю дефекта, выступают как индукторы ангиогенеза, обеспечивая репаративные процессы
Разработаны следующие лекарственные формы ДБА:
- ДБА в нативном виде для закладывания в конъюнктивальную полость.
- Лекарственная форма ДБА на основе тетрациклиновой мази в пропорции 1:1.
- Лекарственная форма ДБА на основе облепихового масла в пропорции 1:1.
Противопоказаниями являются глубокие поражения стромы роговицы и конъюнктивы, требующие замещения целостности ткани при помощи мембранного трансплантата.
Показаниями для применения указанных форм ДБА являются:
1. Кератиты различной этиологии
2. Химические, термические ожоги роговицы и конъюнктивы 1, 2, 3а, 3б степени.
3. Эрозии роговицы
4. Первичный и рецидивирующий птеригиум различной степени зрелости
5. Язва роговицы
Полученные нами экспериментальные и клинические данные позволяют использовать ДБА в офтальмологической практике в разработанных нами 3-х лекарственных формах. При поверхностных поражениях достаточно применения нативной формы ДБА. При более глубоких поражениях, открытом раневом дефекте более 5 мм в диаметре рекомендуется применение ДБА на мазевой основе (в комбинации с облепиховым маслом). При присоединении инфекции целесообразно сочетание ДБА с антибиотиками. В настоящее время утверждены технические условия на серийное производство ДБА, которое организовано на базе лаборатории трансплантатов Всероссийского центра глазной и пластической хирургии.
Указанные лекарственные формы могут использоваться при различных поражениях роговицы и конъюнктивы с учетом тяжести поражения, независимо от этиологии.